
����Ŀ��ijС����COCl26H2O��NH4Cl��H2O2 �� Ũ��ˮΪԭ�ϣ��ڻ���̿���£��ϳɳȻ�ɫ����X��Ϊȷ������ɣ���������ʵ�飮
��1�����ⶨ����ƷX���ܣ������ȵ����ʵ���֮��Ϊ1��6��3���ܵĻ��ϼ�Ϊ��֪X�Ļ�ѧʽ���������л�ѧʽ����������������Ag��NH3��2 OH �����İ���ͭ[Cu��NH3��4]SO4 �� �Ʊ�X�Ļ�ѧ����ʽ
��2�����IJⶨ����ȷ��ȡwgX��������ˮ�ܽ⣬ע����ͼ��ʾ������ƿ�У�Ȼ����μ�������10%NaOH��Һ��ͨ��ˮ����������ƷҺ�еİ�ȫ����������V1mL c1molL��1���������Һ���գ�����������ȡ�½���ƿ����c2molL��1NaOH����Һ�ζ���ʣ��HCl�����յ�ʱ����V2mL NaOH��Һ�� 
�ٷŢݣ������Һ������������
��װ���а�ȫ�ܵ�����ԭ��
����Ʒ�е���������������ʽ ��
���𰸡�
��1��+3��2CoCl2+2NH4Cl+10NH3+H2O2 ![]() 2[Co��NH3��6]Cl3+2H2O
2[Co��NH3��6]Cl3+2H2O
��2����ʽ�ζ��ܣ�ʹAƿ��ѹǿ�ȶ���![]() ��100%
��100%
���������⣺��1�����ⶨ����ƷX���ܡ������ȵ����ʵ���֮��Ϊ1��6��3�����仯ѧʽΪ[Co��NH3��6]Cl3 �� ���ݻ������и�Ԫ�ػ��ϼ۵Ĵ�����Ϊ0��CoԪ�ػ��ϼ�Ϊ+3�ۣ��÷�Ӧ��Coʧ���ӡ�˫��ˮ�õ��ӣ�CoCl26H2O��NH4Cl��H2O2��NH3������Ӧ����[Co��NH3��6]Cl3��ˮ����Ӧ����ʽΪ2CoCl2+2NH4Cl+10NH3+H2O2 ![]() 2[Co��NH3��6]Cl3+2H2O�����Դ��ǣ�+3��2CoCl2+2NH4Cl+10NH3+H2O2
2[Co��NH3��6]Cl3+2H2O�����Դ��ǣ�+3��2CoCl2+2NH4Cl+10NH3+H2O2 ![]() 2[Co��NH3��6]Cl3+2H2O����2���ټ�ֻ��ʢ���ڼ�ʽ�ζ����У�������Һֻ��ʢ������ʽ�ζ����У�����ʢ����Һ���������Ϊ��ʽ�ζ��ܣ����Դ��ǣ���ʽ�ζ��ܣ� ����������ƿ��ѹǿ������С�����������Σ�գ�������A�ڵ�����Һ�����ߣ�������ѹ��������С��������ͨ�����ܽ�����ƿ��Ҳ������ɵ�������ȫ���õ�ԭ����ʹA��ѹǿ�ȶ������Դ��ǣ�ʹAƿ��ѹǿ�ȶ������백����Ӧ��n��HCl��=V1��10��3L��C1molL��1��C2molL��1 ��V2��10��3L=��C1V1��C2V2����10��3mol�����ݰ�����HCl�Ĺ�ϵʽ֪��n��NH3��=n��HCl��=��C1V1��C2V2����10��3mol��������������=
2[Co��NH3��6]Cl3+2H2O����2���ټ�ֻ��ʢ���ڼ�ʽ�ζ����У�������Һֻ��ʢ������ʽ�ζ����У�����ʢ����Һ���������Ϊ��ʽ�ζ��ܣ����Դ��ǣ���ʽ�ζ��ܣ� ����������ƿ��ѹǿ������С�����������Σ�գ�������A�ڵ�����Һ�����ߣ�������ѹ��������С��������ͨ�����ܽ�����ƿ��Ҳ������ɵ�������ȫ���õ�ԭ����ʹA��ѹǿ�ȶ������Դ��ǣ�ʹAƿ��ѹǿ�ȶ������백����Ӧ��n��HCl��=V1��10��3L��C1molL��1��C2molL��1 ��V2��10��3L=��C1V1��C2V2����10��3mol�����ݰ�����HCl�Ĺ�ϵʽ֪��n��NH3��=n��HCl��=��C1V1��C2V2����10��3mol��������������= ![]() ��100%�����Դ��ǣ�
��100%�����Դ��ǣ� ![]() ��100%��
��100%��


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����꣬�й�Ů��ѧ�������ϻ��ŵ�����������������ǣ�����Ϊ�������Ϳ�űҩ���������غ�˫�����أ������ȫ���ر��Ƿ�չ�й��ҵ��������˵�����������֪�ṹ��ͼ��ʾ��������˵����ȷ���ǣ� �� 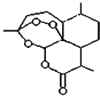
A.��������ά����Cһ��������ˮ����
B.����̼ԭ�Ӷ�������ͬһƽ����
C.�����ؾ���Ϊ���Ӿ��壬�仯ѧʽΪC15H22O5
D.������������θ����������ˮ�⣬��ˮ�������ʹ�Ȼ�����Һ����ɫ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������SO2�������Ƿ����CO2�ķ�����(����)
A.��ͨ����������ʯ��ˮ����ͨ������Ʒ����Һ
B.��ͨ����������NaHCO3��Һ����ͨ������ʯ��ˮ
C.��ͨ������NaOH��Һ����ͨ������ʯ��ˮ
D.��ͨ����������KMnO4��Һ����ͨ������ʯ��ˮ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ���ҳ����ļ������巢��װ����ͼA��B��C��ʾ��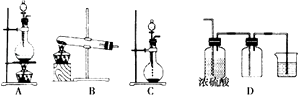
��1��ʵ���ҿ�����B��Cװ����ȡ�����������Bװ����ȡ�����仯ѧ��Ӧ����ʽΪ ��
��2�������������ѡ�������ռ���������Ҫ���ݣ������������ռ������ص���������ţ���ͬ�������ܶ� ����ɫ ���ܽ��� �����ȶ��� ����������Ӧ
��3������Aװ����Dװ��������ȡ���ռ�X���壬��X���������������е� �� ��CO2 ��NO��Cl2 ��H2��HCl
������Dװ��������С�ձ���Ŀ���� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Na2CO3������������ǶԴ�����ò�ͬ���෨�ķ��࣬����ȷ����(����)
A. Na2CO3��̼���� B. Na2CO3����
C. Na2CO3������ D. Na2CO3�Ǽ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijԪ��B�ĺ˵����ΪZ����֪Bn����Am+�ĺ��������ͬ�ĵ���������AԪ�ص�ԭ��������Z��n��m����ʾ��ӦΪ
A. Z+m+nB. Z��n+mC. Z��n��mD. Z+n��m
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з�Ӧ�У�ˮֻ����ԭ������
A. 2Na2O2+2H2O��4NaOH+O2�� B. 2Na+2H2O��2NaOH+H2��
C. 2F2 + 2H2O = 4HF + O2 D. 2H2O![]() 2H2��+O2��
2H2��+O2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪AΪ�������ʣ���ͼ��ʾ�����еĸ�����Ӧ�����������E�ǰ�ɫ������
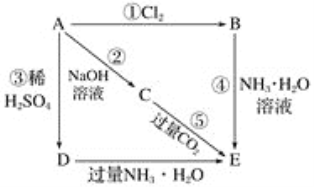
��1��д���������ʵĻ�ѧʽ��
A��________��B��________��C��________��D��________��E��________��
��2��д�����б仯�Ļ�ѧ����ʽ��
��A��NaOH��Һ��Ӧ�Ļ�ѧ����ʽ��_____________________________��
��A����������NaOH��Һ��Ӧ�����ӷ���ʽ��__________________________��
����C����E���̵Ļ�ѧ����ʽ��_____________________________��
��3����һ������A���뵽NaOH��Һ�У������������ڱ�״���µ����Ϊ3.36 L�������ĵ�A�����ʵ���Ϊ________��ת�Ƶ��ӵ����ʵ���Ϊ________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com