
����Ŀ��ij̼�ظֹ�¯��ˮ������Ҫ�ɷ���̼��ơ�����ơ�������þ�����⡢��������ȡ�ˮ�����γɰ�ȫ�������輰ʱ��ϴ��ȥ����ϴ�������£�
����NaOH��Na2CO3���Һ�����ȣ�������Сʱ��
�ų�ϴ�ӷ�Һ����ˮ��ϴ��¯������ϡ���������NaF��Һ�����ݣ�
����ϴҺ�м���Na2SO3��Һ��
������ϴ��꣬��NaNO2��Һ�ۻ���¯��
��1����NaOH�ܽ��������Ļ�ѧ����ʽ��__________________________________��
��2����֪��20��ʱ�ܽ��/g
CaCO3 | CaSO4 | Mg(OH)2 | MgCO3 |
1.4��10-3 | 2.55��10-2 | 9��10-4 | 1.1��10-2 |
�������ݣ���ϻ�ѧƽ��ԭ��������ϴCaSO4�Ĺ���________________________��
��3���ڲ�����У�
�� ��������ˮ���������⣬����_______________________________________��
�� ��ϴ�����У��ܽ���������ٹ�¯��ʴ�������ӷ���ʽ������ԭ��________��
��4��������У�����Na2SO3��Ŀ����_______________________��
��5��������У��ۻ���Ĺ�¯����Ḳ��һ�����ܵ�Fe2O3����Ĥ��
�� ��ɲ���ƽ�䷴Ӧ�����ӷ���ʽ��______
![]()
��������ۻ�Ч���ķ�����������______��
a����¯���ϵμ�ŨH2SO4���۲���Һ�����ػ�ɫ��ʱ��
b����¯���ϵμ�����CuSO4��Һ���۲���ɫ��ʧ��ʱ��
c����¯���ϵμ�����K3[Fe(CN)6]��Һ���۲������ɫ������ʱ��
d����¯���ϵμ�ŨHNO3���۲���ֺ���ɫ�����ʱ��
���𰸡�SiO2 +2NaOH��Na2SiO3+H2O CaSO4��ˮ�д���ƽ��CaSO4��s)![]() Ca2+��aq)+ SO42-��aq)����Na2CO3��Һ���ݺ�Ca2+��CO32-��ϳɸ����ܵ�CaCO3��ʹ����ƽ�����ƣ�CaSO4ת����CaCO3��Ȼ���������ȥ CaCO3��Mg��OH)2��SiO2 2Fe3++Fe��3Fe2+ ��Fe3+��ԭ��Fe2+����ֹFe3+��ʴ��¯ 2 2 1 1 1Fe2O3 2OH- b c
Ca2+��aq)+ SO42-��aq)����Na2CO3��Һ���ݺ�Ca2+��CO32-��ϳɸ����ܵ�CaCO3��ʹ����ƽ�����ƣ�CaSO4ת����CaCO3��Ȼ���������ȥ CaCO3��Mg��OH)2��SiO2 2Fe3++Fe��3Fe2+ ��Fe3+��ԭ��Fe2+����ֹFe3+��ʴ��¯ 2 2 1 1 1Fe2O3 2OH- b c
��������
��1�����������������������NaOH��Ӧ�Ļ�ѧ����ʽ��SiO2 2NaOH��Na2SiO3 + H2O��
��2��CaSO4��ˮ�д���ƽ��CaSO4��s)![]() Ca2+��aq)+ SO42-��aq)����Na2CO3��Һ���ݺ��ݱ������ݿ��ж�Ca2+��CO32-��ϳɸ����ܵ�CaCO3��ʹ����ƽ�����ƣ�CaSO4ת����CaCO3��������������ȥ̼��Ƽ��ɡ�
Ca2+��aq)+ SO42-��aq)����Na2CO3��Һ���ݺ��ݱ������ݿ��ж�Ca2+��CO32-��ϳɸ����ܵ�CaCO3��ʹ����ƽ�����ƣ�CaSO4ת����CaCO3��������������ȥ̼��Ƽ��ɡ�
��3���ٷ����������ᷴӦ����HF��HF����������跴Ӧ�����Ա�������ˮ���������⣬����CaCO3��Mg��OH)2��SiO2��
����ϴ�����У��ܽ���������ٹ�¯��ʴ���������������Ӿ��������ԣ���������Ӧ����Ӧ�����ӷ���ʽΪ2Fe3+ + Fe��3Fe2+��
��4�������������ܸ�ʴ���������������ƾ��л�ԭ�ԣ����Բ�����У�����Na2SO3��Ŀ���ǽ�Fe3+��ԭ��Fe2+����ֹFe3+��ʴ��¯��
��5���ٸ��ݷ���ʽ��֪��Ԫ�صĻ��ϼ۴�0�����ߵ�+3�ۣ�ʧȥ3�����ӡ���Ԫ�صĻ��ϼ۴�+3�۽��͵�0�ۣ��õ�3�����ӣ����Ը��ݵ��ӵ�ʧ�غ��֪��Ӧ�ķ���ʽΪ2Fe+2NO2- +H2O��N2��+ Fe2O3+ 2OH-��
��a. ��¯���ϵμ�ŨH2SO4��Ũ������ʹ���ۻ������Բ���ͨ���۲���Һ�����ػ�ɫ��ʱ����ۻ�Ч����a����b. ����ͭ�����������û���Ӧ��������¯���ϵμ�����CuSO4��Һ��ͨ���۲���ɫ��ʧ��ʱ����Լ��ۻ�Ч����b��ȷ��c. ��������������Ӧ�����������ӣ���������������K3[Fe��CN)6]��Ӧ������ɫ���������ͨ���۲������ɫ������ʱ����Լ��ۻ�Ч����c��ȷ��d. ��¯���ϵμ�ŨHNO3��Ũ���������ۻ������Բ���ͨ���۲���ֺ���ɫ�����ʱ����ۻ�Ч����d����ѡbc��


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij����ɱ���ܱ�������ʢ��������A��B�Ļ�����壬��һ�������·�����Ӧ��A+3B![]() 2C����ά���¶Ⱥ�ѹǿ���䣬������ƽ��ʱ�����������ΪVL������C��������ռ10%�������ƶ���ȷ���ǣ� ��
2C����ά���¶Ⱥ�ѹǿ���䣬������ƽ��ʱ�����������ΪVL������C��������ռ10%�������ƶ���ȷ���ǣ� ��
��ԭ����������Ϊ1.2VL
��ԭ�����������Ϊ1.1VL
�۷�Ӧ��ƽ��ʱ����A����0.05VL
�ܷ�Ӧ��ƽ��ʱ����B���ĵ�0.05VL
A.�ڢ�B.�ڢ�C.�٢�D.�٢�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������(ClO2)��һ�ֹ��ס���Ч����������������ˮ��������ˮ�����ȷ����й㷺Ӧ�á�������ijУ��ѧ�о�С�����ʵ����ȡClO2�Ĺ�������ͼ�������й�˵����ȷ����(����)

A.���ʱ������Ӧ�Ļ�ѧ����ʽΪ2HCl![]() Cl2����H2��
Cl2����H2��
B.��NaClO2��Һ��ȡ0.6 mol ClO2ʱ����������0.1 mol NCl3
C.�������Ļ������ͨ��ʢ�м�ʯ�ҵĸ������Գ�ȥClO2�е� NH3
D.��ҺX�ijɷ�ΪNaClO3��NaOH
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ӧ2A��B = 3C��4D(���ʾ�Ϊ����)�У���ʾ�÷�Ӧ����������(����)
A.v(A)��0.5 mol��L��1��s��1B.v(B)��0.3 mol��L��1��s��1
C.v(C)��0.8 mol��L��1��s��1D.v(D)��4 mol��L��1��min��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ����CO��H2����ȼ�ϼ״�(CH3OH)��һ���������ܱ������з�����Ӧ���������������ͼ��ʾ(��Ӧ����������̬)������˵���������
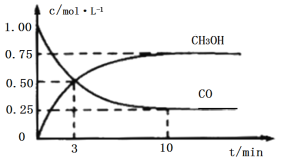
A.��Ӧ�Ļ�ѧ����ʽ��CO+2H2CH3OH
B.��Ӧ������3����ʱ�������淴Ӧ�������
C.��Ӧ��10���ӣ�(CO)=0.075mol/(L��min1)
D.��Ӧ��3���ӣ��ü״�����ʾ��Ӧ��ƽ������Ϊ![]() mol/(L��min1)
mol/(L��min1)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijʵ��С���ù�ҵ�Ϸ������壨��Ҫ�ɷ�Cu2S��Fe2O3���������ȡ��ͭ��Fe2��SO4��3���壬��ƵIJ����������£�
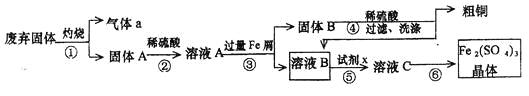
��1�����ƾ��ƺ�����̨�������żܣ��⣬�������������Ϊ_____���ٺ͢��ж��õ��IJ�������Ϊ_______��
��2����֪�Լ�xΪ�������⣬д��H2O2����ҺB��Ӧ�����ӷ���ʽ___________��
��3��ijͬѧȡ��������ҺB�����м��������ij��ǿ���������ٵμ�KSCN��Һ��������Һ���ɫ������һ��ʱ�����Һ��ɫ����ͬѧ�²���Һ��ɫ��ԭ������Һ�е�SCN-���������������������¡�
�ָ��������Լ���1.0 mol��L-1���ᡢ1.0 mol��L-1NaOH��Һ��0.1 mol��L-1Fe2��SO4��3.����Һ��20��KSCN��Һ������ˮ��������ƺ���ʵ����֤��ͬѧ�IJ²��Ƿ��������Ҫ˵��ʵ�鲽�������_______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������X������(��ͨ��)Y��Һ�����ɳ������������Y�����ʵ�����ϵ��ͼ��ʾ���±��з���ͼʾ�������

A | B | C | D | |
X | CO2 | HCl | NaOH | AlCl3 |
Y | Ca(OH)2 | NaAlO2 | AlCl3 | NaOH |
A.AB.BC.CD.D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ҫ����գ�
��һ��ij��ͬѧ������ʵ��̽��Fe2+��Fe3+�����ʡ��ش��������⣺
��1������ͬѧȡ2mLFeCl2��Һ�����뼸����ˮ���ټ���1��KSCN��Һ����Һ��죬˵��Cl2�ɽ�Fe2+������FeCl2��Һ����ˮ��Ӧ�����ӷ���ʽΪ_______��
��2������ͬѧ��Ϊ�����ʵ�鲻���Ͻ�������ͬѧ��2mLFeCl2��Һ���ȼ���0.5mLú�ͣ�����Һ�������μ��뼸����ˮ��1��KSCN��Һ����Һ��죬ú�͵�������________��
����������ҵ����ij����������Cu2O��Al2O3��Fe2O3��SiO2����ȡͭ�IJ����������£���������E������ҺC��ȡ����
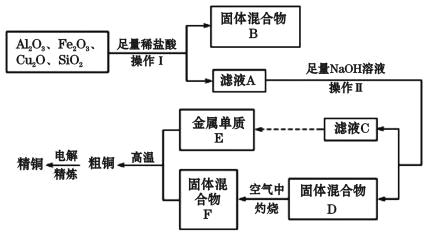
��֪��Cu2O+2H+ =Cu+Cu2+ +H2O��
��3����������B�ijɷ���____��
��4����ҺA����Ԫ�صĴ�����ʽΪ____�������ӷ��ţ������ɸ�������FeԪ�ص��йط�Ӧ�����ӷ���ʽΪ_________��_____��
��5������ҺC��ͨ������CO2���壬����CO2+OH-=HCO3-����Ҫ�����ӷ���ʽ��________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���״�����Ϊȼ�ϵ�ص�ԭ�ϡ�ͨ�����з�Ӧ�����Ʊ��״���CO ( g ) + 2H2 ( g ) ![]() CH3OH ( g ) ��H ����90.8 kJ��mol��1����һ�ݻ��ɱ���ܱ������г���10 mol CO ��20 mol H2��CO ��ƽ��ת�������¶���T����ѹǿ��P���ı仯��ͼ��ʾ�����ﵽƽ��״̬A ʱ�����������Ϊ20 L��
CH3OH ( g ) ��H ����90.8 kJ��mol��1����һ�ݻ��ɱ���ܱ������г���10 mol CO ��20 mol H2��CO ��ƽ��ת�������¶���T����ѹǿ��P���ı仯��ͼ��ʾ�����ﵽƽ��״̬A ʱ�����������Ϊ20 L��
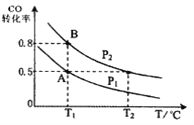
��1��T1����Ӧ��ƽ�ⳣ��Ϊ_______________��
��2��ͼ��P1 _______ P2������>������<������=������
��3���練Ӧ��ʼʱ�Գ���10 mol CO��20 mol H2������ƽ��״̬Bʱ���������V(B)=__________L��
��4�����ڷ�ӦCO(g)+2H2(g)![]() CH3OH(g)�ڻ�ѧƽ��״̬Bʱ��������ȷ����___
CH3OH(g)�ڻ�ѧƽ��״̬Bʱ��������ȷ����___
A��CO�ĺ������ֲ���
B��������CH3OHŨ����COŨ�����
C��2v��(CH3OH)= v��(H2)
D�������л�������ƽ����Է����������ֲ���
��5����֪CO2(g)+H2(g) ![]() CO(g) + H2O(g) ��H = + 41.3 kJ��mol��1 ����д����CO2��H2��ȡ�״����Ȼ�ѧ����ʽ___________________________________��
CO(g) + H2O(g) ��H = + 41.3 kJ��mol��1 ����д����CO2��H2��ȡ�״����Ȼ�ѧ����ʽ___________________________________��
��6����CH3OH��O2��ϡH2SO4���ȼ�ϵ�أ�д���õ�������ĵ缫��Ӧʽ��__��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com