
����Ŀ�������һ�����ܱ�����������������A��B��C��������һ�������·�����Ӧ������������ѧƽ�⣺aA(g) + bB(g)![]() xC(g)��������ͼ��ʾ�Ĺ�ϵ��c%��ʾƽ�������в���C�İٷֺ�����T��ʾ�¶ȣ�p��ʾѹǿ������ͼ�У�Y����ָ( )
xC(g)��������ͼ��ʾ�Ĺ�ϵ��c%��ʾƽ�������в���C�İٷֺ�����T��ʾ�¶ȣ�p��ʾѹǿ������ͼ�У�Y����ָ( )

A����Ӧ��A�İٷֺ���
B����Ӧ��B��ƽ��ת����
C��ƽ���������ܶ�
D��ƽ�������������ʵ���
���𰸡�B
��������
�����������ͼ��֪����ͬ�¶�T1ʱ������ѹǿ��P2��P1����C�İٷֺ�������˵������ѹǿƽ��������Ӧ�����ƶ�������a+b��x����ͬѹǿP2ʱ�������¶ȣ�T1��T2����C�İٷֺ������ͣ���˵�������¶�ƽ�����淴Ӧ�����ƶ����÷�Ӧ������ӦΪ���ȷ�Ӧ����ͼ��Y���¶ȡ�ѹǿ�ı仯��֪����ͬ�¶��£�Y��ѹǿ�����������ͬѹǿ�£�Y���¶��������С��A������ѹǿƽ��������Ӧ�����ƶ���A��ת�������������¶�ƽ�������ƶ���A��ת���ʼ�С����ͼ����Y�ɱ�ʾA��ת���ʣ�����B������ѹǿƽ��������Ӧ�����ƶ���B�İ�ת����������ͼ���������ȷ��C�����ڷ�Ӧ������������䣬������������䣬���¶ȡ�ѹǿ�仯��ƽ���������ܶȲ��䣬����D�������¶ȣ�ƽ�����淴Ӧ�����ƶ���������������ʵ������࣬������ͼ����



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijʵ��С���һ����Al3+��δ֪��Һ���������·������ٵ�����������������Һ�������Ա仯���ڼ����μ�����������Һ����ʼ������ɫ�������۵������������������Һ����ɫ�������Լ��١�ʵ��С�龭����������������������ʵ��������������������Ĺ�ϵͼ��������˵���д�����ǣ� ��

A. ��δ֪��Һ�����ٺ���3��������
B. �μӵ�NaOH��Һ�����ʵ���Ũ��Ϊ5 mol/L
C. ����һ������Ϊ���������ӣ���a=5
D. ���յõ��ij�������ɷ���ȷ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ȡ16.8 g̼�����ƹ������һ��ʱ���ʣ���������13.7 g����ʣ�������뵽100 mL2 mol/L��ϡ�����У���ַ�Ӧ����Һ�������ӵ�Ũ��ԼΪ
A.1.4 mol/LB.3 mol/LC.0.5 mol/LD.2 mol/L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£�����Ũ�ȵ�NaOH��Һ�ֱ�μӵ���pH���������HA��HB����������Һ�У���Һ��pH������Ũ�ȱ�ֵ�Ķ�����ϵ��ͼ��ʾ�����������������

A.��pH���������Ũ�ȣ�c(HA) < c(HB)
B.����ƽ�ⳣ����10Ka(HA)= Ka(HB)
C.b����Һ��c(B)=c(HB)>c(Na+)>c(H+)>c(OH)
D.��HB��Һ�еμ�NaOH��Һ��pH=7ʱ��c(B)> c(HB)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��25�棬����ˮ��Һ�� HCl ���� FeCl3 ���� KOH ���� Na2CO3 ����ˮ��Һ��PH����Ϊ 4��4 ��10 ��10 ������Һ��ˮ�ĵ���̶ȴ�С��ϵ��ȷ���� ��������
A.��=��=��=��B.�٣��ۣ��ڣ���C.��=�ڣ���=��D.��=�ۣ��ڣ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼΪһ�������²��ö���Ե缫�Ĵ����س��װ�ã����������л������֪����װ�õĵ���Ч��![]() ��100%������˵������ȷ����
��100%������˵������ȷ����
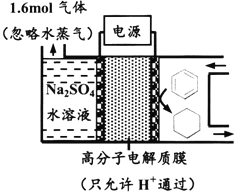
A. ���ö�缫�����˽Ӵ�������ɽ��͵��������ʧ
B. ������ͨ��C-H���Ķ���ʵ����Ĵ���
C. ����Ŀ�����ĵ缫��ӦʽΪC6H6+6e-+6H+===C6H12
D. ��![]() =75%����μӷ�Ӧ�ı�Ϊ0.8mol
=75%����μӷ�Ӧ�ı�Ϊ0.8mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��2018��9��26�գ�������������ڶ�ʩ���Ļ����Ĵ��Ժ��Ļ�����������������Ϊ�������й�����������������(Se)�ǵ������ڵ�VI A��Ԫ�أ��������ڲ��ɻ�ȱ����Ԫ�أ�H2Se���Ʊ������̫���ܵ�ء��뵼����Ϻͽ������������Ҫԭ�ϡ�
(1)��֪:��2H2Se(g)+O2(g) ![]() 2Se(s)+2H2O(l) ��H =a kJ��mol-1
2Se(s)+2H2O(l) ��H =a kJ��mol-1
��2H2 (g)+O2(g![]() 2H2O(l) ��H=b kJ��mol��1
2H2O(l) ��H=b kJ��mol��1
��ӦH2(g)+ Se(s) ![]() H2Se(g)�ķ�Ӧ�ȡ�H=______kJ��mol-1(�ú�a��b�Ĵ���ʽ��ʾ)��
H2Se(g)�ķ�Ӧ�ȡ�H=______kJ��mol-1(�ú�a��b�Ĵ���ʽ��ʾ)��
(2)T��ʱ����һ�����ܱ������м���3molH2��1 mol Se��������ӦH2 (g)+Se(s)![]() H2Se(g),
H2Se(g),
������������жϷ�Ӧ�ﵽƽ��״̬����_______(����ĸ����)��
a. ������ܶȲ��� b. v(H2) =v(H2Se)
c. �����ѹǿ���� d.�����ƽ��Ħ����������
�ڵ���Ӧ�ﵽƽ���ƽ��������ͨ������Һ��������ʹH2Se����ת��ΪH2SeҺ�壬�����������H2�ٴ�ͨ�뷢����Ӧ���ܱ������м�����Se��Ӧʱ��Se��ת���ʻ���ߡ����û�ѧƽ�����۽���:________________________________________________��
����5Сʱ�ڵõ���H2SeΪ����ָ�꣬���¶ȡ�ѹǿ��H2Se���ʵ�Ӱ����ͼ��ʾ:

���Ʊ�H2Se������¶Ⱥ�ѹǿΪ________��
(3)��֪������H2Se�ĵ���ƽ�ⳣ��![]() ����NaHSe��Һ��_______(��������������������)������Һ�е������غ��ϵʽΪ_____________��
����NaHSe��Һ��_______(��������������������)������Һ�е������غ��ϵʽΪ_____________��
(4)��ҵ�ϴӺ�����������ȡ���ķ�����������������ƵĻ����Һ����������������������ᣬ�������Ṳ�ȣ�����ת��Ϊ�����ᣬ���������ᷴӦ�Ļ�ѧ����ʽΪ___________�����ͨ��SO2���������ʡ�
(5) H2 Se��һ�������¿����Ʊ���CuSe����֪����ʱCuSe��Ksp=7.9![]() ,CuS��
,CuS��![]() ����ӦCuS(s)+Se2-(aq)
����ӦCuS(s)+Se2-(aq)![]() CuSe(s)+S2-(aq)�Ļ�ѧƽ�ⳣ��K=_____ (����2λ��Ч����)��
CuSe(s)+S2-(aq)�Ļ�ѧƽ�ⳣ��K=_____ (����2λ��Ч����)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ü�������ȼ�ϵ��Ϊ��Դ���е���ʵ��װ��ʾ��ͼ��ͼ��ʾ������˵������ȷ���ǣ� ��

A.ȼ�ϵ�ع���ʱ������ӦΪ��H2=2H++2e-
B.��Ҫʵ�����϶�ͭ����a��������b����ͭ
C.��Ҫʵ�ֵ�⾫����ͭ����a������������Ӧ��b������ͭ����
D.a��b��������ʯīʱ������ͬ�����£������������H222.4L����״����ʱ��a������ͭ64g
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��25��ʱ����0��100 mol��L-1����ֱ�ζ�20��00 mL 0��100 mol��L-1�İ�ˮ��20��00 mL 0��100 mol��L-1NaOH��Һ������Һ��pH�������������(V)�Ĺ�ϵ��ͼ��ʾ������˵����ȷ���� ( )

A. Kb(NH3��H2O)��������Ϊ10��4
B. 10 < a < 20
C. P����Һ�У�c(NH4+)>c(Clһ)
D. ˮ�ĵ���̶ȣ�M > N > P
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com