
【题目】取16.8 g碳酸氢钠固体加热一段时间后,剩余固体质量13.7 g,把剩余固体加入到100 mL2 mol/L的稀硫酸中,充分反应后溶液中氢离子的浓度约为
A.1.4 mol/LB.3 mol/LC.0.5 mol/LD.2 mol/L
【答案】D
【解析】
发生2NaHCO3![]() Na2CO3+CO2↑+H2O,加热一段时间后,剩余固体质量13.7g,利用差量法确定固体的成分,加盐酸发生HCO3-+H+=H2O+CO2↑、CO32-+2H+=H2O+CO2↑,以此计算反应后溶液中氢离子的浓度。
Na2CO3+CO2↑+H2O,加热一段时间后,剩余固体质量13.7g,利用差量法确定固体的成分,加盐酸发生HCO3-+H+=H2O+CO2↑、CO32-+2H+=H2O+CO2↑,以此计算反应后溶液中氢离子的浓度。
16.8g碳酸氢钠的物质的量n(NaHCO3)=![]() =0.2 mol,将该固体加热,发生反应:2NaHCO3
=0.2 mol,将该固体加热,发生反应:2NaHCO3![]() Na2CO3+CO2↑+H2O,根据方程式可知:每有168 gNaHCO3发生分解反应,固体质量会减少(44+18) g=62 g,加热一段时间后,剩余固体的质量为13.7 g,分解的NaHCO3质量为16.8 g-13.7 g=3.1g,所以反应的NaHCO3的物质的量n(NaHCO3)=
Na2CO3+CO2↑+H2O,根据方程式可知:每有168 gNaHCO3发生分解反应,固体质量会减少(44+18) g=62 g,加热一段时间后,剩余固体的质量为13.7 g,分解的NaHCO3质量为16.8 g-13.7 g=3.1g,所以反应的NaHCO3的物质的量n(NaHCO3)=![]() =0.1mol,反应产生的Na2CO3的物质的量为0.05 mol,因此反应后剩余固体中含Na2CO30.05 mol,含有NaHCO30.1 mol,100 mL 2 mol/L的稀硫酸中n(H+)=0.1 L×2 mol/L×2=0.4 mol,由CO32-+2H+=H2O+CO2↑可知0.05 mol Na2CO3反应消耗0.1 mol H+,由HCO3-+H+=H2O+CO2↑可知0.1 mol NaHCO3反应消耗0.1 mol H+,所以溶液中剩余H+物质的量为0.4 mol-0.1 mol-0.1 mol=0.2 mol,故充分反应后溶液中氢离子的浓度约为c(H+)=
=0.1mol,反应产生的Na2CO3的物质的量为0.05 mol,因此反应后剩余固体中含Na2CO30.05 mol,含有NaHCO30.1 mol,100 mL 2 mol/L的稀硫酸中n(H+)=0.1 L×2 mol/L×2=0.4 mol,由CO32-+2H+=H2O+CO2↑可知0.05 mol Na2CO3反应消耗0.1 mol H+,由HCO3-+H+=H2O+CO2↑可知0.1 mol NaHCO3反应消耗0.1 mol H+,所以溶液中剩余H+物质的量为0.4 mol-0.1 mol-0.1 mol=0.2 mol,故充分反应后溶液中氢离子的浓度约为c(H+)=![]() =2 mol/L,故合理选项是D。
=2 mol/L,故合理选项是D。


 高效智能课时作业系列答案
高效智能课时作业系列答案科目:高中化学 来源: 题型:
【题目】下列各表述与示意图一致的是
A. 如图表示向含
如图表示向含![]() 、
、![]() 、
、![]() 的盐溶液中滴加NaOH溶液时,沉淀的量与NaOH的体积关系图.则三种离子的物质的量之比为:
的盐溶液中滴加NaOH溶液时,沉淀的量与NaOH的体积关系图.则三种离子的物质的量之比为:![]() :
:![]() :
:![]()
![]() :1:2,其中使用的NaOH的浓度为2
:1:2,其中使用的NaOH的浓度为2![]()
B. 如图中曲线表示某反应过程的能量变化,当物质
如图中曲线表示某反应过程的能量变化,当物质![]() 与
与![]() 反应生成物质
反应生成物质![]() 是,
是,![]() ,若使用正催化剂,E值会减小
,若使用正催化剂,E值会减小
C.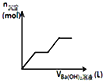 如图可用来表示向盐酸酸化的
如图可用来表示向盐酸酸化的![]() 溶液中加入
溶液中加入![]() 溶液时,产生沉淀的物质的量
溶液时,产生沉淀的物质的量![]() 与加入
与加入![]() 溶液体积
溶液体积![]() 之间的关系图
之间的关系图
D. 如图表示向一定质量的明矾溶液中滴加
如图表示向一定质量的明矾溶液中滴加![]() 溶液时,产生沉淀的质量
溶液时,产生沉淀的质量![]() 与加入
与加入![]() 溶液体积
溶液体积![]() 之间的关系图
之间的关系图
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将盛有12mLNO2和O2的混合气体的量筒倒立于水槽中,充分反应后,还剩余2 mL无色气体,则原混合气体中O2的体积和剩余的2mL气体可能分别是
A.1.2mL,NOB.2.4mL,O2
C.3.5mL,O2D.4mL,NO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下述转化关系,回答问题:

已知:①+CH3Br![]() CH3+HBr;
CH3+HBr;
②C物质苯环上一卤代物只有两种。
(1)写出B物质的名称__________;D物质的结构简式________。
(2)写出反应②的类型________;反应⑤的条件________。
(3)写出反应⑥的化学方程式:________________________________。
(4)写出D+E反应的化学方程式:_______________。
(5)反应②还有可能生成一种C16H18的有机物,其苯环上一卤代物也只有两种,写出它的结构简式:_______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室常用亚硫酸钠固体和70%的浓硫酸制备SO2气体,反应方程式为Na2SO3+H2SO4=Na2SO4+SO2↑+H2O,请设计一套实验装置,收集一试管干燥的SO2气体。
(1)在下面方框中,A表示由分液漏斗和锥形瓶组成的气体发生器,请在答题卡上的A后完成该反应的实验装置示意图(夹持装置、连接胶管不必画出,尾气处理部分必须画出,需要加热的仪器下方用△标出),按气流方向在每件仪器下方标出字母B、C…;其它可选用的仪器(数量不限)简易表示如下:___

(2)根据方框中的装置图甲,在答题卡上填写下表(可不填满)___
仪器标号 | 仪器中所加物质 | 作用 |
A | 亚硫酸钠、浓硫酸 | 产生SO2 |
(3)某实验小组用如图乙装置测定收集到的气体中SO2的含量,反应管中装有酸性高猛酸钾溶液。
①SO2和酸性高猛酸钾溶液发生反应的离子方程式为:___。
②反应管内溶液紫红色消失后,若没有及时停止通气,则测得的SO2含量___(选填:“偏高”、“偏低”或“无影响”)
③若酸性高猛酸钾溶液体积为V1mL,浓度为cmol/L,量气管内增加的水的体积为V2mL(已折算成标准状况下的体积)。用c、V1、V2表示SO2的体积百分含量为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
我国科学家最近成功合成了世界上首个五氮阴离子盐(N5)6(H3O)3(NH4)4Cl(用R代表)。回答下列问题:
(1)氮原子价层电子对的轨道表达式(电子排布图)为_____________。
(2)元素的基态气态原子得到一个电子形成气态负一价离子时所放出的能量称作第一电子亲和能(E1)。第二周期部分元素的E1变化趋势如图(a)所示,其中除氮元素外,其他元素的E1自左而右依次增大的原因是___________;氮元素的E1呈现异常的原因是__________。
(3)经X射线衍射测得化合物R的晶体结构,其局部结构如图(b)所示。
①从结构角度分析,R中两种阳离子的相同之处为_________,不同之处为__________。(填标号)
A.中心原子的杂化轨道类型 B.中心原子的价层电子对数
C.立体结构 D.共价键类型
②R中阴离子N5-中的σ键总数为________个。分子中的大π键可用符号![]() 表示,其中m代表参与形成的大π键原子数,n代表参与形成的大π键电子数(如苯分子中的大π键可表示为
表示,其中m代表参与形成的大π键原子数,n代表参与形成的大π键电子数(如苯分子中的大π键可表示为![]() ),则N5-中的大π键应表示为____________。
),则N5-中的大π键应表示为____________。
③图(b)中虚线代表氢键,其表示式为(NH4+)N-H┄Cl、____________、____________。

(4)R的晶体密度为d g·cm-3,其立方晶胞参数为a nm,晶胞中含有y个[(N5)6(H3O)3(NH4)4Cl]单元,该单元的相对质量为M,则y的计算表达式为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在体积一定的密闭容器中,给定物质A、B、C的量,在一定条件下发生反应,建立如下化学平衡:aA(g) + bB(g)![]() xC(g),符合下图所示的关系(c%表示平衡混合气中产物C的百分含量,T表示温度,p表示压强)。在图中,Y轴是指( )
xC(g),符合下图所示的关系(c%表示平衡混合气中产物C的百分含量,T表示温度,p表示压强)。在图中,Y轴是指( )

A.反应物A的百分含量
B.反应物B的平衡转化率
C.平衡混合气的密度
D.平衡混合气的总物质的量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以菱锰矿![]() 主要成分
主要成分![]() ,还含有
,还含有![]() 、
、![]() 等杂质
等杂质![]() 为原料制备二氧化锰的工艺流程如下:
为原料制备二氧化锰的工艺流程如下:
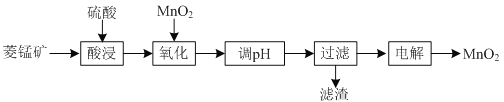
已知部分金属离子开始沉淀及沉淀完全时的pH如下表所示:
金属离子 |
|
|
|
|
开始沉淀时的pH |
|
|
|
|
沉淀完全时的pH |
|
|
|
|
(1)①“酸浸”时![]() 发生反应的离子方程式为________________________________________。
发生反应的离子方程式为________________________________________。
②“酸浸”过程中加入过量硫酸的目的除了加快酸浸的速率、_____________、___________。
③要提高“酸浸”的速率,还可以采取的方法是________________________________________。
(2)“氧化”时发生反应的离子方程式为________________________________________。
(3)“调pH”的目的是除去溶液中的杂质金属离子,“调pH”的范围应为_______________。
(4)当溶液中c(Al3+)≤10-5mol/L时,则认为![]() 沉淀完全,则
沉淀完全,则![]() ______________。
______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com