
【题目】下列有关化学与自然的开发利用描述中不正确的是
A. 可用热分解法冶炼氧化汞得到水银
B. 从自然界中提炼金属要经过矿石的富集、冶炼、精炼三步
C. 铝热法炼铁的反应需要高温的条件,所以是吸热反应
D. 金属单质被发现和应用得越早,其活动性一般越弱
科目:高中化学 来源: 题型:
【题目】下到分析错误的是
A.酸性:HClO4>H3PO4B.离子半径:F- >Mg2+
C.阴离子还原性:Cl->S2-D.H、N、O三种元素可形成离子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)已知2NO2(红棕色)![]() N2O4(无色)可以同时相互转化,①在密封有NO2的玻璃瓶中,升高温度,颜色加深,问NO2转化为N2O4是一个__________(填“吸热”或“放热”)反应;②在一个恒温恒压容器中,通入稀有气体。颜色_______(填“变深”、“变浅”或“不变”),平衡________移动(填“正向”、“逆向”或“不”下同);③在一个密闭恒容体系中,增大NO2的量,会引起NO2转化率________(填“增大”、“减小”或“不变”),颜色_______,再通入稀有气体增大压强,平衡________移动,颜色_________。
N2O4(无色)可以同时相互转化,①在密封有NO2的玻璃瓶中,升高温度,颜色加深,问NO2转化为N2O4是一个__________(填“吸热”或“放热”)反应;②在一个恒温恒压容器中,通入稀有气体。颜色_______(填“变深”、“变浅”或“不变”),平衡________移动(填“正向”、“逆向”或“不”下同);③在一个密闭恒容体系中,增大NO2的量,会引起NO2转化率________(填“增大”、“减小”或“不变”),颜色_______,再通入稀有气体增大压强,平衡________移动,颜色_________。
(2)用焦炭还原NO2的反应为:2NO2(g)+2C(s)![]() N2(g)+2CO2(g),在恒温条件下,1 mol NO2和足量C发生该反应,测得平衡时NO2和CO2的物质的量浓度与平衡总压的关系如图所示:
N2(g)+2CO2(g),在恒温条件下,1 mol NO2和足量C发生该反应,测得平衡时NO2和CO2的物质的量浓度与平衡总压的关系如图所示:
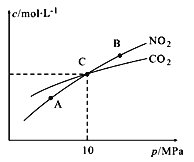
①A、B两点的浓度平衡常数关系:Kc(A)_______Kc(B) (填 “﹥”、“<”或“﹦”)。
②A、B、C三点中NO2的转化率最高的是_____(填“A”或“B”或“C”)点。
③计算C点时该反应的压强平衡常数Kp(C)=______(Kp是用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实不能用平衡移动原理解释的是( )
A. 红棕色的NO2,加压后颜色先变深后变浅,但比原来要深
B. 高压比常压有利于SO2合成SO3的反应
C. 500 ℃时比室温更利于合成氨
D. 氯水在光照条件下颜色变浅,最终变为无色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组微粒,在溶液中能大量共存的是( )
A. Ca2+、Cl﹣、CO32-、K+ B. Cu2+、Cl﹣、SO42-、OH﹣
C. K+、Cl﹣、NO3-、H+ D. H+、Cl﹣、CO32-、Na+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】运用碳及其化合物的性质,完成下列小题:
(1)长期存放石灰水的瓶子内会出现一层白色固体,请分析这层白色固体产生的原因(用化学方程式表示);用完石灰水后,怎样除去瓶壁上的白色固体,(用化学方程式表示).
(2)除去碳酸钠固体中少量碳酸氢钠的方法是(用化学方程式表示):
(3)向碳酸氢钠溶液滴加NaOH溶液,发生反应的离子方程式为: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏德罗常数,下列叙述正确的是( )
A.标准状况下,22.4L H2O含有的分子数为NA
B.2L物质的量浓度为0.5mol/L的MgCl2溶液中,含有Cl﹣ 个数为 NA
C.常温下,NA个CO2分子占有的体积为22.4L
D.1.06g Na2CO3含有的Na+离子数为0.02 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于阿伏加德罗常数的说法正确的是
A.阿伏加德罗常数是一个纯数,没有单位
B.阿伏加德罗常数就是6.02×1023mol-1
C.阿伏加德罗常数数值上等于0.012Kg C所含的碳原子数
D.阿伏加德罗常数是指1mol的任何粒子集合体中含有的粒子数
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com