
| A. | 30min时降低温度,40min时升高温度 | |
| B. | 8min前A的平均反应速率为0.16mol/(L•min) | |
| C. | 反应方程式中的x=1,正反应为吸热反应 | |
| D. | 20min~40min间该反应的平衡常数均为4 |
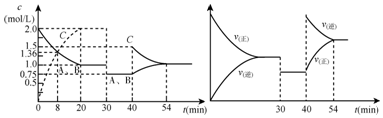
分析 从该题图1可知,0-20min是反应:A(g)+xB(g)?2C(g)达到平衡的过程,20min时各浓度保持不变,正逆反应速率相等,反应达到平衡状态,20-30min,是保持平衡状态过程;反应物和生成物的浓度都减少,结合图象2知,正逆反应速率相等且减小平衡不移动;40-54min,图1知,反应物浓度增大生成物浓度减小,图2知正逆反应速率都增大,且与原平衡点无接触点,逆反应速率大于正反应速率,当正逆反应速率相等时,再次达到平衡状态,
A、由图象可知,由开始到达到平衡,A、B的浓度减少的量相同,由此可知X=1.30min时只有反应速率降低了,反应物与生成物的浓度瞬时降低,反应仍处于平衡状态,故不能是温度变化,而是降低了压强;40min时,正逆反应速率都增大,且逆反应速率大于正反应速率,平衡向逆向进行,则增大压强平衡不移动,应是升高温度;
B.反应从开始到8min内A浓度减少了0.64mol/L,根据v=$\frac{△c}{△t}$计算v(A);
C、由开始到达到平衡,A、B的浓度减少的量相同,由此可知X=1.则增大压强平衡不移动,40min时,正逆反应速率都增大,且逆反应速率大于正反应速率,平衡向逆向进行,应是升高温度,则正反应为放热反应;
D、平衡常数随温度变化,由图象可知,30min时只有反应速率降低了,反应物与生成物的浓度瞬时降低,反应仍处于平衡状态,故不能是温度变化,而是降低了压强;
解答 解:A、从图2可知,30min时正反应速率和逆反应速率同时降低.降低反应温度,正反应速率和逆反应速率同时降低,但降低反应温度,平衡向放热反应方向移动.该反应无论正反应方向放热还是吸热,平衡均移动与图中30-40min改变条件后,平衡不移动矛盾,故A错误.
B、0~8min内,C的反应速率v=$\frac{1.36mol/L}{8min}$=0.17mol/(L•min)-1,化学反应速率之比等于方程式的系数之比,所以A的平均反应速率为0.085mol/(L•min)-1,故B错误;
C.由开始到达到平衡,A、B的浓度减少的量相同,由此可知X=1,则增大压强平衡不移动,40min时,正逆反应速率都增大,且逆反应速率大于正反应速率,平衡向逆向进行,应是升高温度,则正反应为放热反应,故C错误;
D、由图象可知,30min时只有反应速率降低了,反应物与生成物的浓度瞬时降低,反应仍处于平衡状态,故不能是温度变化,而是降低了压强,所以平衡常数不变,20~30 min间,各物质的浓度为:c(A)=c(B)=1mol/L,c(C)=2mol/L,所以K=$\frac{{2}^{2}}{1×1}$=4,故D正确.
故选D.
点评 本题考查化学平衡图象问题,题目难度较大,本题注意根据图象浓度的变化以及反应速率的变化判断化学反应状态以及影响化学反应速率的条件,掌握基础是解题关键.


 应用题点拨系列答案
应用题点拨系列答案 状元及第系列答案
状元及第系列答案 同步奥数系列答案
同步奥数系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 向200mL稀硫酸和稀硝酸的混合溶液中逐渐加入铁粉至过量,产生气体的量随铁粉质量增加的变化如图所示(假定硝酸只被还原为NO).则下列说法中,正确的是( )
向200mL稀硫酸和稀硝酸的混合溶液中逐渐加入铁粉至过量,产生气体的量随铁粉质量增加的变化如图所示(假定硝酸只被还原为NO).则下列说法中,正确的是( )| A. | OA段产生的是NO和H2的混合气 | B. | BC段产生的全部是NO | ||
| C. | Fe2(SO4)3是最终的溶质 | D. | H2SO4的物质的量浓度是2 mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若a≥2b,发生的反应化学方程式为:2C2H2+O2═4C+2H2O | |
| B. | 若($\frac{2}{5}$)b<a<($\frac{2}{3}$)b,燃烧后在密闭容器中加入含amolCa(OH)2的石灰水,发生反应的离子方程式为:OH-+CO2═HCO3- | |
| C. | 若a<($\frac{2}{5}$)b,燃烧过程中转移的电子的物质的量为10amol | |
| D. | 若a=($\frac{1}{2}$)b,燃烧产物既有CO2又有CO,且n(CO2):n(CO)=1 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 四种元素均为非金属元素 | |
| B. | W与X、Y形成的最简单分子的沸点:X>Y | |
| C. | Y、Z形成的化合物中只含离子键 | |
| D. | W、Y、Z形成的化合物的电子式为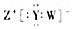 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
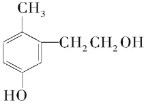
| A. | 它是苯酚的同系物 | |
| B. | 1 mol该物质能与溴水反应消耗2molBr2发生取代反应 | |
| C. | 1 mol该有机物能与足量金属钠反应生成0.5mol H2 | |
| D. | 1 mol该有机物能与2molNaOH反应 | |
| E. | 该物质在加热条件下可以与铜反应生成一种具有醛基的化合物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com