
【题目】糖尿病是由于体内胰岛素紊乱导致的代谢紊乱综合症,以高血糖为主要标志。长期摄入高热量食品和缺少运动都易导致糖尿病。
(1)血糖是指血液中的葡萄糖(C6H12O6)。下列说法正确的是________。
A.葡萄糖属于碳水化合物,其分子式可表示为C6(H2O)6,则每个葡萄糖分子中含6个H2O
B.糖尿病人尿糖高,可用新制的氢氧化铜悬浊液来检测病人尿液中的葡萄糖
C.葡萄糖为人体提供能量
D.淀粉水解的最终产物是葡萄糖
(2)木糖醇[CH2OH(CHOH)3CH2OH]是一种甜味剂,糖尿病人食用后血糖不会升高。请预测木糖醇的一种化学性质:___________________________________________________。
(3)糖尿病人不可饮酒,酒精在肝脏内可被转化成有机物A。A的有关性质实验结果如下:
Ⅰ.通过样品的质谱测得A的相对分子质量为60。
Ⅱ.核磁共振氢原子光谱能对有机物分子中同效氢原子给出相同的峰值(信号),根据峰值(信号)可以确定分子中氢原子的种类和数目。例如:乙醇(CH3CH2OH)有三种氢原子(图甲)。经测定,有机物A的核磁共振氢谱示意图如图乙所示。

Ⅲ.将A溶于水,滴入石蕊试液,发现溶液变红。试写出A的结构简式:_________________________________________________。
(4)糖尿病人宜多吃蔬菜和豆类食品。蔬菜中富含纤维素,豆类食品中富含蛋白质。下列说法错误的是________(填序号)。
A.蛋白质都属于天然有机高分子化合物,且都不溶于水
B.用灼烧闻气味的方法可以区别合成纤维和羊毛
C.人体内不含纤维素水解酶,人不能消化纤维素,因此蔬菜中的纤维素对人没有用处
D.紫外线、医用酒精能杀菌消毒,是因为它们能使细菌的蛋白质变性
E.用天然彩棉制成贴身衣物可减少染料对人体的副作用
(5)香蕉属于高糖水果,糖尿病人不宜食用。乙烯是香蕉的催熟剂,它可使溴的四氯化碳溶液褪色,试写出该反应的化学方程式:__________________________________。
【答案】 BCD 能与羧酸发生酯化反应(或其他合理的答案均可) CH3COOH AC CH2===CH2+Br2―→CH2Br—CH2Br
【解析】(1)A.葡萄糖的化学式为C6H12O6,不含有水,故A错误;B.葡萄糖中含有醛基,醛基能与新制的氢氧化铜反应生成砖红色沉淀,故B正确;C.葡萄糖在人体内会发生氧化反应放出能量,为人体提供需要的能量,故C正确;D.淀粉水解最终生成葡萄糖,故D正确.故答案为:BCD;
(2)木糖醇中含有羟基,羟基能发生酯化反应,故答案为:能与羧酸发生酯化反应;
(3)核磁共振氢谱中有几个峰就有几中氢原子,图乙有2个峰,说明有2种氢原子,将A溶于水,滴入石蕊试液,发现溶液变红,溶液呈酸性,说明含有羧基,根据相对分子质量为60,60-45=13,另一个基团为甲基,A为CH3COOH,故答案为:CH3COOH;
(4)A.蛋白质均属于天然高分子化合物,它们的相对分子质量在10000万以上,部分蛋白质可溶于水,如血清蛋白、酶等,故A错误; B.羊毛是蛋白质,因蛋白质灼烧时有烧焦羽毛的特殊气味,所以可用灼烧来鉴别合成纤维和羊毛,故B正确;C.人类膳食中的纤维素主要含于蔬菜和粗加工的谷类中,虽然不能被消化吸收,但有促进肠道蠕动,利于粪便排出等功能,故C错误;D.细菌的成分是蛋白质,紫外线、医用酒精能使蛋白质变性,能杀菌消毒,故D正确;E.天然彩棉对人体无不良反应,用天然彩棉制成贴身衣物可减少染料对人体的副作用,故E正确;故答案为:AC;
(5)乙烯含有碳碳双键,与溴发生加成反应,生成1,2-二溴乙烷,使溴的四氯化碳溶液褪色.反应生成1,2-二溴乙烷,反应方程式为CH2=CH2+Br2→CH2Br-CH2Br,故答案为:CH2=CH2+Br2→CH2Br-CH2Br。


科目:高中化学 来源: 题型:
【题目】氮气是制备含氮化合物的重要原料,而含氮化合物的用途广泛。回答下列问题:
(1)两个常见的固氮反应为:
N2(g)+O2(g)![]() 2NO(g)…………(Ⅰ)
2NO(g)…………(Ⅰ)
N2(g)+3H2(g)![]() 2NH3(g)…………(Ⅱ)
2NH3(g)…………(Ⅱ)
①气相反应中,某物质A 的组成习惯用分压p(A)代替浓度c(A),相应的平衡常数用Kp表示。反应(Ⅰ)的平衡常数表达式Kp=_________________。
②反应(Ⅱ)在不同温度下的平衡常数Kp如下表:
温度/K | 298 | 473 | 673 |
Kp | 62(KPa)-2 | 6.2×10-5(KPa)-2 | 6.0×10-8(KPa)-2 |
则反应(Ⅱ) 的ΔH________0(填“>”、“<”或“=”)
(2)合成氨工业中原料气所含的少量CO对合成塔中的催化剂有害,可由“铜洗”工序实现对原料气精制。有关反应的化学方程式如下:
[Cu(NH3)2]Ac(aq)+CO(g) +NH3(g)![]() [Cu(NH3)3] ]Ac·CO(aq)
[Cu(NH3)3] ]Ac·CO(aq)
ΔH=-35 kJ·mol-1,用化学平衡移动原理分析该工序生产的适宜条件为________________________。
(3)氨气是工业制硝酸的主要原料。T℃时,NH3和O2可能发生如下反应:
①4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g) △H= -907kJmol-1
4NO(g)+6H2O(g) △H= -907kJmol-1
②4NH3(g)+3O2(g)![]() 2N2(g)+6H2O(g) △H= -1269kJmol-1
2N2(g)+6H2O(g) △H= -1269kJmol-1
其中②是副反应。若要减少副反应,提高NO的产率,最合理的措施是___________________;
T℃时N2和O2反应生成NO的热化学方程式为________________________________。
(4)生产和实验中常采用甲醛法测定铵盐的含氢量。反应原理如下:
4NH4++6HCHO==(CH2)6N4H+(一元酸)+3H++6H2O
实验步骤如下:
①取铵盐样品溶液a mL,加入稍过量的甲醛溶液(已除去其中的酸),静置1分钟;
②滴入1-2滴酚酞溶液,用cmol·L-1的氢氧化钠溶液滴定至溶液呈粉红色且半分钟内不褪去为止,记录消耗氢氧化钠溶液的体积;
③重复以上操作2 次,三次实验平均消耗氢氧化钠溶液VmL。
则样品中的含氮量为____mg·L-1;下列铵盐不适合用甲醛法测定含氮量的是____________(填标号)。
a.NH4HCO3 b. (NH4)2SO4 c.NH4Cl d.CH3COONH4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2008年诺贝尔化学奖授予美籍华裔钱永健等三位科学家,以表彰他们发现和研究了绿色荧光蛋白。荧光素是发光物质的基质, 5-羧基荧光素与5-羧基二乙酸荧光素在碱性条件下有强烈的绿色荧光,它们广泛应用于荧光分析等。

![]()
下列说法不正确的是
A. 5-FAM转变为5-CFDA属于取代反应
B. 5-FAM的分子式为C21H12O7
C. 5-FAM和5-CFDA 各1mol分别与足量NaOH溶液反应,消耗NaOH 物质的量相同
D. 实验室鉴别5-FAM与5-CFDA可用NaHCO3 溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO(NH2)2(尿素)在制备氢气,碳酸二甲酯及烟气脱硫、脱硝等方面有着广泛的应用。回答下列问题:

(1)电解尿素的碱性溶液制备氢气的装置如右图所示,a极是________;通电时,阴极周围溶液的pH________(填“增大”或“减小”);阳极的电极反应式为________。
(2)尿素合成碳酸二甲酯的相关反应及平衡常数的对数值与温度的关系如下:
(Ⅰ)2CH3OH(l)+CO(NH2)2(1)![]() CH3OCOOCH3(l)+2NH3(g)△H1
CH3OCOOCH3(l)+2NH3(g)△H1
(Ⅱ)CH3OH(l)+CO(NH2)2(l)![]() CH3OCONH2(l)+NH3(g)△H2
CH3OCONH2(l)+NH3(g)△H2
(Ⅲ)CH3OCONH2(l)+CH3OH(l)![]() CH3OCOOCH3(l)+NH3(g)△H3
CH3OCOOCH3(l)+NH3(g)△H3

①△H1=_______(用△H2和△H3表示);平衡常数的对数lnK(Ⅰ)=________[用lnK(Ⅱ)和lnK(Ⅲ)表示]。
②对于反应(Ⅱ),升高温度,化学平衡向________(“正”或“逆”)反应方向移动。
③为提高CH3OCOOCH3的产率,可采取的措施有________________________________(列举2点)。
(3)尿素中添加NaClO2所得混合溶液可用于烟气脱硫、脱硝。用含NO和SO2的混合烟气进行实验。混合液中NaClO2的质量分数与NO和SO2的脱除率关系如图所示。

①含SO2的烟气(含O2)通过尿素溶液得到的盐为_________;NO2与尿素溶液反应。生成N2和另外两种氧化物,写出该反应的化学方程式:_______________________________。
②若用纯尿素溶液,则NO的脱除率仅约为15%,说明NaClO2的作用是_____________。
③SO2的脱除率总是比NO的大,其原因是____________________________(列举2点)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】使1mol乙烯与氯气完全发生加成反应,然后使该加成反应的产物与氯气在光照条件下发生取代反应,则取代反应过程中消耗氯气的总物质的量最多为( )
A.3molB.4molC.5molD.6mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列属于物理变化的是( )
①石油的分馏 ②煤的干馏 ③石油的裂化 ④铝热反应 ⑤由乙烯制备聚乙烯
⑥将氧气转化为臭氧 ⑦乙烯催熟果实 ⑧蛋白质的盐析 ⑨海水蒸馏制取淡水
A.①②③④B.①②⑤⑦
C.①⑧⑨D.①②⑥⑨
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验探究是化学学科的重要特征。
Ⅰ.根据下列装置图,回答有关问题:
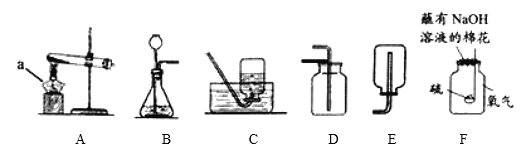
(1)a仪器的名称是________。
(2)如用装置A制取氧气,其反应的化学方程式为_______________________________;如用装置B制取氧气,往长颈漏斗中倒入的液体药品是__________;如用装置D收集氧气,则验满的方法是_____________________________。
(3)小明用装置F做硫在氧气中燃烧的实验,该改进实验最大优点是________________。
Ⅱ.粗盐提纯中得到的“精盐”常还含有可溶性杂质(假设只有CaCl2一种),为得到更纯净的氯化钠,同学们做了如下处理:
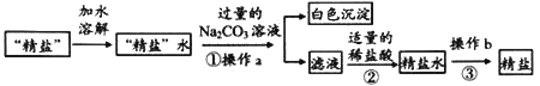
(1)操作b的名称是_________。
(2)步骤①加入过量的Na2CO3溶液的目的是________________。
(3)步骤②反应的化学方程式:___________________________。
(4)如何证明经过步骤②后过量的Na2CO3已除尽?_________________________(写出实验操作、现象、结论)。
(5)若不考虑损耗,经过上述处理得到的精盐质量_______(填“大于”、“小于”或“等于”)原“精盐”质量,原因是__________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】—定温度下,将2 mol SO2和1mol O2充入10 L恒容密闭容器中,发生反应2SO2(g) +O2(g)![]() 2SO3(g) △H =-196 kJ mol-1。5 min时达到平衡,测得反应放热166. 6 kJ。下列说法错误的是
2SO3(g) △H =-196 kJ mol-1。5 min时达到平衡,测得反应放热166. 6 kJ。下列说法错误的是
A. 0~5 min内,用O2表示的平均反应速率V(O2)=0.017 mol·L-1·min-1
B. ![]() 的值不变时,该反应达到平衡状态
的值不变时,该反应达到平衡状态
C. 若增大O2的浓度,SO2的转化率增大
D. 条件不变,若起始时充入4 mol SO2和2 mol O2,平衡时放出的热量小于333.2 kJ
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com