
(1 5分)
世界环保联盟建议全面禁止使用氯气用于饮用水的消毒,而建议采用高效“绿色”消毒剂二氧化氯。二氧化氯是一种极易爆炸的强氧化性气体,易溶于水、不稳定、呈黄绿色,在生产和使用时必须尽量用稀有气体进行稀释,同时需要避免光照、震动或受热。实验室以电解法制备ClO2的流程如下: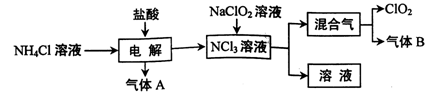
(1)ClO2中所有原子 (填“是”或“不是”)都满足8电子结构。上图所示方法制得的混合气中杂质气体B能使石蕊试液显蓝色,除去该杂质气体可选用 __;
A.饱和食盐水 B.碱石灰 C.浓硫酸 D.蒸馏水
(2)稳定性二氧化氯是为推广二氧化氯而开发的新型产品。下列说法正确的是 ;
A.二氧化氯可广泛用于工业和饮用水处理
B.应用在食品工业中能有效地延长食品贮藏期
C.稳定性二氧化氯的出现大大增加了二氧化氯的使用范围
D.在工作区和成品储藏室内,要有通风装置和监测及警报装置
(3)欧洲国家主要采用氯酸钠氧化浓盐酸制备,但该方法缺点是产率低、产品难以分离,还可能污染环境。写出该方法发生的化学方程式 ;
(4)我国广泛采用经干燥空气稀释的氯气与固体亚氯酸钠(NaClO2)反应制备,化学方程式是
,此法相比欧洲方法的优点是 。
(5)科学家又研究出了一种新的制备方法,利用硫酸酸化的草酸(H2C2O4)溶液还原氯酸钠,化学反应方程式为 ,此法提高了生产及储存、运输的安全性,原因是____ 。
(1)不是; C;(2)A、B、C、D ;(3)2NaClO3+4HCl(浓) === 2NaCl+Cl2↑+2ClO2↑+2H2O ;
(4)2NaClO2+Cl2 ="==" 2NaCl+2ClO2 ; 产率高,易于分离,没有产生毒副产品 ;
(5)H2C2O4+2NaClO3+H2SO4="==" Na2SO4+2CO2↑+2ClO2↑+2H2O ;
反应过程中生成的二氧化碳起到稀释作用
解析试题分析:(1)ClO2中所有原子不是都满足8电子的稳定结构;上图所示方法制得的混合气中杂质气体B能使石蕊试液显蓝色,则B是氨气,由于其水溶液显碱性,所以除去该杂质气体可选用酸性除杂试剂浓硫酸来除去,选项是C。(2)A.根据题意可知:二氧化氯可广泛用于工业和饮用水处理,正确;B.由于该物质有强氧化性,可以起到杀菌、消毒的作用,所以应用在食品工业中能有效地延长食品贮藏期,正确;C.由于二氧化氯是一种极易爆炸的强氧化性气体,所以稳定性大大影响其使用范围,因此稳定性二氧化氯的出现大大增加了二氧化氯的使用范围,正确;D.由于二氧化氯是一种极易爆炸的强氧化性气体,不稳定、呈黄绿色,在生产和使用时必须尽量用稀有气体进行稀释,同时需要避免光照、震动或受热。在工作区和成品储藏室内,要有通风装置和监测及警报装置,正确;(3)欧洲国家主要采用氯酸钠氧化浓盐酸制备,该反应的方程式是:2NaClO3+4HCl(浓) === 2NaCl+Cl2↑+2ClO2↑+2H2O;(4)我国广泛采用经干燥空气稀释的氯气与固体亚氯酸钠(NaClO2)反应制备,化学方程式是2NaClO2+Cl2 ="==" 2NaCl+2ClO2 ;此法相比欧洲方法的优点是产率高,易于分离,没有产生毒副产品;(5)科学家又研究出了一种新的制备方法,利用硫酸酸化的草酸(H2C2O4)溶液还原氯酸钠,化学反应方程式为H2C2O4+2NaClO3+H2SO4="==" Na2SO4+2CO2↑+2ClO2↑+2H2O ;此法提高了生产及储存、运输的安全性,原因是反应过程中生成的二氧化碳起到稀释作用。
考点:考查ClO2的结构、性质及制取方法的知识。


 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案科目:高中化学 来源: 题型:单选题
已知NaCN溶液呈碱性;(CN)2与卤素单质的性质相似;CN-的还原性介于Br-、I-之间。下列变化不能发生的是
A.HCN H++CN- H++CN- | B.(CN)2 + CH2=CH2→ NC—CH2—CH2—CN |
| C.(CN)2+2Br-→ 2CN-+Br2 | D.(CN)2 + 2OH-→CN- + CNO- + H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
已知R有多种化合价,其最高正价为+7价。在一定条件下,RO3-与R-可发生反应:RO3-+5R-+6H+=3R2+3H2O,下列关于R元素的叙述中,正确的是( )
| A.元素R位于周期表中第VA族 |
| B.RO3-中的R只能被还原 |
| C.R-离子的最外层电子数为8 |
| D.若1 mol RO3-参与该反应,则转移的电子的物质的量为5mol |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
ClO2气体是一种常用的消毒剂,我国从2 000年起逐步用ClO2代替氯气对饮用水进行消毒。
(1)消毒水时,ClO2还可将水中的Fe2+、Mn2+等转化成Fe(OH)3和MnO2等难溶物除去,在这个过程中,Fe2+、Mn2+的化合价升高,说明ClO2具有______性。
(2)工业上可以通过下列方法制取ClO2,请完成该化学反应方程式:
2KClO3+SO2===2ClO2+__________。
(3)自来水厂用ClO2处理后的水中,要求ClO2的浓度在0.1~0.8 mg·L-1之间。碘量法可以检测水中ClO2的浓度,步骤如下:
Ⅰ.取一定体积的水样,加入一定量的碘化钾,再用氢氧化钠溶液调至中性,并加入淀粉溶液,溶液变蓝。
Ⅱ.加入一定量的Na2S2O3溶液。(已知:2S2O +I2===S4O
+I2===S4O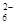 +2I-)
+2I-)
Ⅲ.加硫酸调节水样pH至1~3。
操作时,不同pH环境中粒子种类如下图所示: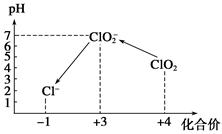
请回答:
①操作Ⅰ中反应的离子方程式是______________________________。
②确定操作Ⅱ完全反应的现象是______________________________。
③在操作Ⅲ过程中,溶液又呈蓝色,反应的离子方程式是__________________。
④若水样的体积为1.0 L,在操作Ⅱ时消耗了1.0×10-3 mol·L-1的Na2S2O3溶液10 mL,则水样中ClO2的浓度是________mg·L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(10分)有三份不同质量的铁粉样品①②③,甲、乙、丙三位同学各取一份样品分别与含有0.8molHNO3的稀硝酸反应,反应后硝酸和铁均无剩余,且硝酸的还原产物只有NO。据此回答下列问题:
(1)甲取样品①,反应后的溶液中铁只以Fe3+离子的形式存在,则样品①的质量为 g。
(2)乙取样品②,反应后的溶液中既含有Fe3+、又含有Fe2+离子,则样品②的质量(设为ag)范围是 。
(3)丙取样品③,将其慢慢加入到稀硝酸中,并不断搅拌,反应过程中溶液里Fe3+、Fe2+、NO3—三种离子中的两种离子的物质的量的变化曲线如下图所示,则该曲线表示的是 物质的量变化的曲线,请你在此图中再画出另外种离子的物质的量的变化曲线。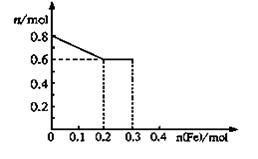
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(13分)某研究性学习小组利用废旧铅蓄电池阴、阳极填充物------铅膏(含PbO、PbO2、PbSO4)制备电绝缘材料三盐基硫酸铅(3PbO?PbSO4?H2O),进行资源回收研究,设计实验流程如下: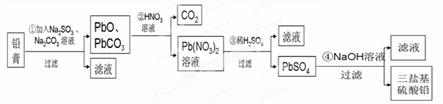
(1)步骤①铅膏中PbSO4与Na2CO3溶液反应转化为PbCO3,说明溶解度:PbSO4 (填“>”或“<”)PbCO3。
(2)步骤①中PbO2转化为PbCO3的离子方程式是(请配平此离子方程式):
(3)将步骤①和④的滤液合并,加入 PH=7,再经过 、冷却结晶、
、洗涤、干燥,可获得Na2SO4?10H2O晶体。
(4)若铅膏的质量为78g,步骤①中PbO2和PbSO4全部转化为PbCO3,且PbO未发生反应;步骤②中共收集到5.6LCO2(标准状态),步骤③中获得90.9 g PbSO4,则铅膏中PbO的质量分数为 (假设流程中原料无损失)。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(15分)在航天发射时,肼(N2H4)及其衍生物常用作火箭推进剂。
⑴液态肼作火箭燃料时,与液态N2O4混合发生氧化还原反应,已知每1g肼充分反应后生成气态水放出热量为a KJ,试写出该反应的热化学方程式 。
⑵实验室用N2H4·H2O与NaOH颗粒一起蒸馏,收集114~116℃的馏分即为无水肼。
①在蒸馏过程中不需要的仪器是 (填序号字母)。
| A.酒精灯 | B.长直玻璃导管 | C.锥形瓶 | D.直型冷凝管 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
有M、R、Q、V、W、X、Y、Z八种物质,它们之间存在如下关系:
①M+Y R ②R+H2O→NaOH+Y ③Q+NaOH→V+W+H2O ④X
R ②R+H2O→NaOH+Y ③Q+NaOH→V+W+H2O ④X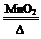 W+Y
W+Y
⑤X+W+H2SO4 Q+Z+H2O。其中M、Q、Y是单质,Q、Y在常温、常压下为气体,Z是硫酸盐,钠、钾化合物性质相似。
Q+Z+H2O。其中M、Q、Y是单质,Q、Y在常温、常压下为气体,Z是硫酸盐,钠、钾化合物性质相似。
回答下列问题:
(1)写出各代号的化学式(或分子式) M , R ,Q ,V ,W ,X ,Y ,Z 。
(2)写出下列有关化学反应的方程式和离子方程式,并标出电子转移方向和总数
反应③ , ;
反应⑤ , 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com