
����Ŀ��ij±�����Ҫ�ɷ���MgCl2�������Fe3+��Fe2+��Mn2+�����Ӻ�����������[CO(NH2)2]�����ø�±��Ϊԭ��������������þ�Ĺ���������ͼ��

����ؽ�������[c0(Mn+)��0.1molL��1]ʱ���γ��������������pH��Χ�����
�������� | Fe2+ | Fe3+ | Mn2+ | Mg2+ |
��ʼ������pH | 7.6 | 2.7 | 8.3 | 9.6 |
������ȫ��pH | 8.3 | 3.7 | 9.8 | 11.1 |
�ش��������⣺
(1)NaClO����Ԫ�صĻ��ϼ�Ϊ_____��NaClOΪƯ��Һ����Ҫ�ɷ֣�д���Ʊ�Ư��Һ�����ӷ���ʽ_____��
(2)����Һb���������ӵ�Ũ�Ⱦ�Ϊ0.1molL��1����Ҫʹ�������ӳ�����ȫ�������Ӧ��Һ��pH������_____��������A����Mn(OH)2��_____��
(3)����ʵ��������ɲ���ޣ��������CӦ��_____(����������)�����ա�д������Ļ�ѧ����ʽ_____��
(4)����ڼ���NaClO���ܳ�ȥ±���е�����[CO(NH2)2]������һ���κ����������弰ˮ���仯ѧ����ʽΪ_____������ȥ±���к��е�0.02molCO(NH2)2��������NaClO������Ϊ_____��
���𰸡�+1 Cl2+2OH����Cl��+ClO��+2H2O 9.8 Fe(OH)3��Mg(OH)2 ���� Mg(OH)2![]() MgO+H2O CO(NH2)2+3NaClO��3NaCl+N2��+CO2��+2H2O 4.47g
MgO+H2O CO(NH2)2+3NaClO��3NaCl+N2��+CO2��+2H2O 4.47g
��������
±���ˮ�ܽ⣬����NaClO��Fe2+������Fe3+��ͬʱ������ȥ±���е�����[CO(NH2)2]������pH��9.8������Mn2+��Fe3+��������Mg2+Ҳ����������Գ�����A����Mn(OH)2��Fe(OH)3��Mg(OH)2��Ȼ������Һ�м��봿�Mg2+����Һ����MgCO3����������Ȼ���ˮ��пɵõ�Mg(OH)2�����պ�õ�MgO���ݴ˷�������
(1)NaClO����Ԫ��+1�ۣ���Ԫ�ة�2�ۣ�����Ԫ��+1�ۣ�NaClOΪƯ��Һ����Ҫ�ɷ֣�һ������������NaOH��Һ��Ӧ�Ʊ������ӷ���ʽΪ��Cl2+2OH����Cl��+ClO��+2H2O��
(2)����Һb���������ӵ�Ũ�Ⱦ�Ϊ0.1molL��1������۵�����ҺpH��Ŀ���dz�ȥMn2+��Fe3+��Ҫʹ�������ӳ�����ȫ�����ݱ���֪����pH������9.8��ͬʱþ������9.6��ʼ����������þ����Ҳ�������ʳ�����A����Mn(OH)2��Fe(OH)3��Mg(OH)2��
(3)�����Ϊ���գ������������н��У���ӦΪ��Mg(OH)2![]() MgO+H2O��
MgO+H2O��
(4)����ڼ���NaClO���ܳ�ȥ±���е�����[CO(NH2)2]������һ���κ����������弰ˮ��ΪNaCl�������Ͷ�����̼�����ݵ����غ��Ԫ���غ�ɵ÷�ӦΪ��CO(NH2)2+3NaClO��3NaCl+N2��+CO2��+2H2O�����ݷ���ʽ��֪������ȥ±���к��е�0.02molCO(NH2)2��������NaClO�����ʵ���Ϊ0.06mol������Ϊ0.06mol��74.5g/mol��4.47g��


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͼʾ���Ӧ������������ǣ� ��

A.ͼ1����a��b������������������Һ����ζ��ĵζ����ߣ�P��ʱ����ǡ�÷�Ӧ��ȫ����Һ������
B.ͼ2��ʾ![]() ��
��![]() ��Ӧ����
��Ӧ����![]() ��
��![]() ʱ�������仯�Ĺ�ϵ
ʱ�������仯�Ĺ�ϵ
C.ͼ3��ʾ��![]() ��Һ�е���NaOH��Һʱ���ó��������ı仯
��Һ�е���NaOH��Һʱ���ó��������ı仯
D.��ͼ4��ʾ�ķ�Ӧ�������¶ȱ仯�Ĺ�ϵ��֪�÷�Ӧ��![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ͼ1Ϊij��ʵ��װ�õ�ʾ��ͼ�����м���װ�úͲ���ҩƷ�Ⱦ���ʡ�ԣ�װ�â��װ�â�Ϊ���巢��װ�ã���
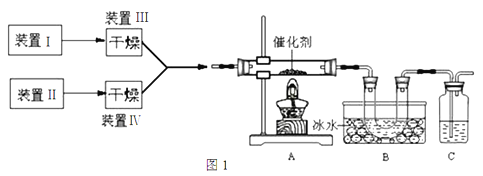
��1����ͬѧ�ô�װ�ã���A��B������һʢ��Ũ�����ϴ��ƿ��
�Ʊ�NO2����֤�����ʡ�
��װ�â�����ʵ�����Ʊ�NH3��װ�â��Ʊ�����O2��װ�â��з�����Ӧ�Ļ�ѧ����ʽΪ_____________________��
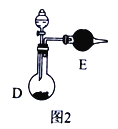
��Ҳ���Խ�������װ�â��ϲ�Ϊһ��װ�ã���ͼ2��ʾ������Һ©����ʢװŨ��ˮ����D�еĹ����Լ�Ϊ_______���ѧʽ����E�е��Լ�Ϊ____________��
��2����ͬѧ�ô���װ�úϳ�SO3��Bװ��U�ι����й�����֡�
��ʵ���ҿ���ͭ��Ũ������Ȼ�������������Ʒ�Ӧ��ȡ�������� ����������������Ʒ�Ӧ��ȡ3.36L����״�������������������25.0%���������ƣ�����������������Ϊ�����ƣ����������ȡ���������Ƶ�����Ϊ______g������һλС������
�������Ƶô��������SO3����ͼ1װ��C��ʢ��NaOH��Һ�����װ���д������Բ��㣺
a.C�е�ˮ�������ܽ���B����SO3��Ӧ��b.____________________________________��
Ӧ��θĽ���______________________________������ͼ������ʵ��װ����ѡ����ĸ��Ų�����滻�����ü�Ҫ����˵��������滻��λ�ã���
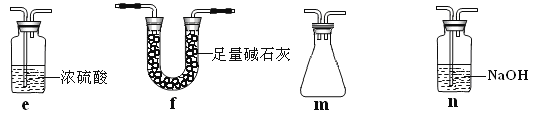
��3����ͬѧ����֤NO�ܱ�������ԭ��������ת���ʣ�װ�â�װ�â�ֱ���ȡNO��NH3)����ͼ1װ����A��B��C�ֱ�ͼ5��װ�â�����������
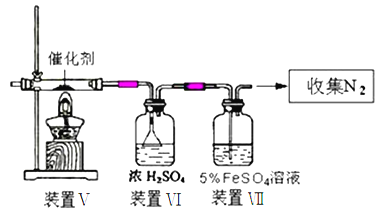
��д��������NO�����Ļ�ѧ����ʽ��___________________________��
��װ�â������ÿ�����__________________________��
��������װ�â���NO��22.4L��������Ϊ��״������ͬ������������������ռ���11.2LN2����NO��ת������__________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ���ǣ�������
A. ʯ�ͷ������������Ʊ�����ϩ����ȡ���¶ȼƵ�λ�ö�����ͬ
B. �����ʵ������Һ�м�ˮ���ɹ۲쵽��Һ������Ϊ�б��㡢ˮ����屽��
C. ±������±ԭ�ӵļ��飬������±����ˮ���IJ�����ֱ�ӵμ�![]() ��Һ
��Һ
D. �Ҵ���Ũ���ᷴӦ���Ƶõ�����ͨ�뵽��ˮ�У�����ˮ��ɫ����֤������ϩ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵������ȷ���ǣ� ��
A. �����������£�CH3CO18OC2H5��ˮ�������CH3CO18OH��C2H5OH
B. ��ȩ�ͱ�ϩȩ����ͬϵ�������H2��ַ�Ӧ��IJ�����ͬϵ��
C. ����ˮ���Լ��𱽷���Һ��2��4-����ϩ���ױ���CCl4
D. ���ᱡ�ɴ�����![]() ���ܷ���ˮ�ⷴӦ��������Ӧ����ȥ��Ӧ��ȡ����Ӧ
���ܷ���ˮ�ⷴӦ��������Ӧ����ȥ��Ӧ��ȡ����Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ԭ�������������������Ԫ��A��B��C��D�ֱ��ڵ�һ���������ڣ���Ȼ���д��ڶ���A�Ļ����Bԭ�Ӻ��������6�ֲ�ͬ���˶�״̬��B��C���γ����������η��ӣ�D�Ļ�̬ԭ�ӵ������ܲ�ֻ��һ�����ӣ������ܲ���ѳ������ӡ�
��ش��������⣺
(1)������Ԫ���е縺������Ԫ�أ����̬ԭ�ӵļ۵����Ų�ͼΪ________����һ��������С��Ԫ����________(��Ԫ�ط���)��
(2)C���������ǰ����Ԫ�طֱ���A�γɵĻ�����е��ɸߵ��͵�˳����________(�ѧʽ)��������˵ݱ���ɵ�ԭ����___________________��
(3)BԪ�ؿ��γɶ��ֵ��ʣ�һ�־���ṹ��ͼһ��ʾ����ԭ�ӵ��ӻ�����Ϊ________����һ�ֵľ�����ͼ����ʾ�����˾����е��ⳤΪ356.6 pm����˾������ܶ�Ϊ________________________________________________g��cm��3(������λ��Ч����)��(![]() ��1.732)
��1.732)

��ͼһ������������ͼ����������������ͼ��
(4)DԪ���γɵĵ��ʣ��侧��Ķѻ�ģ��Ϊ________��D�Ĵ����ξ���ֲ��ṹ��ͼ�����þ����к��еĻ�ѧ����________(��ѡ�����)��
�ټ��Լ������ڷǼ��Լ���������λ�������ܽ�����
(5)��D����������Һ�еμӹ�����ˮ���۲쵽��������________����д���������̵����ӷ���ʽ��_________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ����������������������Ҵ��Ʊ�1��2���������װ����ͼ��ʾ��

�й������б����£�
�Ҵ� | 1��2�������� | ���� | |
״̬ | ��ɫҺ�� | ��ɫҺ�� | ��ɫҺ�� |
�ܶ�/gcm3 | 0.79 | 2.2 | 0.71 |
�е�/�� | 78.5 | 132 | 34.6 |
�۵�/�� | -l30 | 9 | -116 |
�ش��������⣺
��1��д����ʵ������з�����������Ҫ��Ӧ�Ļ�ѧ����ʽ____��
�ڴ��Ƹ�ʵ���У�Ҫ������Ѹ�ٵذѷ�Ӧ�¶�170�����ң�������ҪĿ����___(����ȷѡ��ǰ����ĸ����ͬ)
a.������Ӧ b.�ӿ췴Ӧ�ٶ� c.��ֹ�Ҵ��ӷ� d.���ٸ�������������
��2����װ��C��Ӧ����__����Ŀ�������շ�Ӧ�п������ɵ��������塣
a.ˮ b.Ũ���� c.����������Һ d.����̼��������Һ
��3����1��2��������ֲ�Ʒ���ڷ�Һ©���м�ˮ�����ã�����Ӧ��___�㣬��������������δ��Ӧ��Br2�������____ϴ�ӳ�ȥ��
a.ˮ b.����������Һ c.�⻯����Һ d.�Ҵ�
��4�������������������������ѡ�����____�ķ�����ȥ�����ȷ�ʽΪ____��
��5����Ӧ������Ӧ��___��ȴװ��D
A.��ˮ����� B.�����µ�ˮ C.60�� D.100��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ǻ������������㷺����ʳƷ����ױƷ��ҽҩ������ij��ѧ��ȤС��ͨ���������ף��Ʊ��ǻ��������������ش��������⣺
(һ)���ǻ������������ĺϳ�
ʵ��ԭ����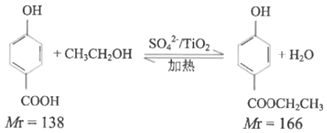
ʵ�鲽�裺ȡ0.4mol�Ҵ��ʹ������ڸ��������A�У�0.1mol���ǻ����������ں�ѹ��Һ©��C�У�ʵ��װ����ͼ��ʾ(���Ⱥͼг�װ��ʡ��)�����Ȼ�������ַ�Ӧ��
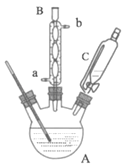
(1)����A��������_____������B������ˮ������Ϊ��_____(��a����b��)ͨ�롣
(2)ijͬѧ��������A������������֮���һ����ˮװ�ã��û�ѧƽ��ԭ���������������ŵ���_____��
(3)ȡ����2g�����ǻ�������0.1mol���Ҵ�0.4mol����Ӧ���������IJ����뷴Ӧʱ��Ĺ�ϵ���±���ʾ��
��Ӧʱ��/Сʱ | 1 | 3 | 4 | 5 | 6 |
���IJ���/% | 45.6 | 88 | 91.8 | 91.1 | 90.8 |
���ݱ������ݿ�֪����ѷ�Ӧ��ʱ��ӦΪ_____����Ӧʱ����������������½��Ŀ���ԭ����_____��
(��)���ǻ������������ľ���
ʵ�鷽�����ٷ�Ӧ��Ϻ�����˳���������Һ������ˮ�У��������壬���ˡ�
�ڹ����Ⱥ���5%��Na2CO3��Һ��ˮϴ�ӣ������õ��ֲ�Ʒ��
����װ�������ܵ�Բ����ƿ�У�����һ�����������Ʒ�����Ҵ���ˮ�ͻ���̿�����Ȼ���0.5Сʱ�����ȳ��ˣ���Һ��ȴ��������ɫ���壬��80���ɡ�
(4)�ڢ�����5%��Na2CO3��Һϴ�ӵ�Ŀ����_____���ܲ�����NaOH��Һ�����_____(��ܡ����ܡ�)��
(5)�ڢ۳��ȳ�����Ҫ��ȥ������Ϊ_____�������ȡ���Ŀ����_____��
(6)��С��ͬѧ��(3)������Ͷ�ϣ����õ����ǻ�����������14.9g�����ʵ��IJ���Ϊ_____%��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��0.1mol/L��NH4Cl��Һ�У�����Ũ�ȹ�ϵ��ȷ����
A.c(![]() )>c(Cl��)>c(H+)>c(OH��)
)>c(Cl��)>c(H+)>c(OH��)
B.c(![]() )>c(OH��)>c(Cl��)>c(H+)
)>c(OH��)>c(Cl��)>c(H+)
C.c(OH��)=c(Cl��)+c(H+)
D.c(![]() )+c(H+)=c(Cl��)+c(OH��)
)+c(H+)=c(Cl��)+c(OH��)
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com