
【题目】化合物X(仅含三种短周期元素)是一种络合氢化物的储氢材料,在400℃下分解,放出氢气。X中某种元素的单质常用来制造信号弹和烟火,某研究小组为了探究A的组成和性质,设计并完成了如下实验。(金属互化物--全部由金属元素组成的化合物)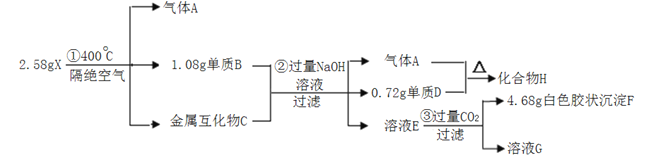
(1)写出单质D对应的阳离子结构示意图:_____。
(2)X在400℃下分解的化学方程式:_____。
(3)写出单质B与NaOH溶液反应的离子方程式:____。
(4)化合物H___(填“可能”或“不可能”)与水发生反应产生H2,判断理由_____。
【答案】![]() 3Mg(AlH4)2=12H2+4Al+Mg3Al2 2H2O+2Al+2OH-=2AlO2- +3H2 可能 MgH2中H元素为-1价,H2O中H元素为+1价,发生氧化还原反应(归中反应)生成H2
3Mg(AlH4)2=12H2+4Al+Mg3Al2 2H2O+2Al+2OH-=2AlO2- +3H2 可能 MgH2中H元素为-1价,H2O中H元素为+1价,发生氧化还原反应(归中反应)生成H2
【解析】
化合物(仅含三种短期元素)是一种络合氢化物的储氢材料,在400℃下分解,放出氢气,则A为H2,X中某种元素的单质常用来制造信号弹和烟火,含有Mg元素,溶液E通入二氧化碳生成白色胶状沉淀,则F应为Al(OH)3,可知X含有Mg、Al、H三种元素,由转化关系可知D为Mg,H为MgH2,B为Al,由题中数据可知n(Mg)=0.72g/24g·mol-1=0.03mol,n(Al)=1.08g/27g·mol-1=0.04mol,n(Al(OH)3)=4.68g/78g·mol-1=0.06mol,X中含有Al的物质的量为0.06mol,C为Mg3Al2,则n(H)=(2.58g-0.03mol×24g·mol-1-0.06mol×27g·mol-1)/1g·mol-1=0.24mol,则X的化学式为Mg(AlH4)2。
(1)D为Mg,单质D对应的阳离子结构示意图:![]() 。
。
(2)X在400℃下分解的化学方程式:3Mg(AlH4)2=12H2+4Al+Mg3Al2。
(3)B为Al,单质B与NaOH溶液反应生成偏铝酸钠和氢气,离子方程式:2H2O+2Al+2OH-=2AlO2- +3H2。
(4)化合物H可能与水发生反应产生H2,判断理由:MgH2中H元素为-1价,H2O中H元素为+1价,发生氧化还原反应(归中反应)生成H2,则可反应。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】化学键的键能是形成(或拆开)1 mol化学键时释放(或吸收)的能量。已知白磷和P4O6的分子结构如图所示,现提供以下化学键的键能(kJ/mol) P—P:198,P—O:360,O=O:498,则反应P4(白磷)+3O2![]() P4O6
P4O6
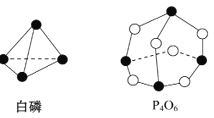
A. 放出1 638 kJ热量
B. 吸收1 638 kJ热量
C. 放出126 kJ热量
D. 吸收126 kJ热量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国科技工作者运用DFT计算研究HCOOH在不同催化剂(Pd和Rh)表面分解产生H2的部分反应历程如图所示,其中吸附在催化剂表面的物种用*表示。下列说法错误的是( )
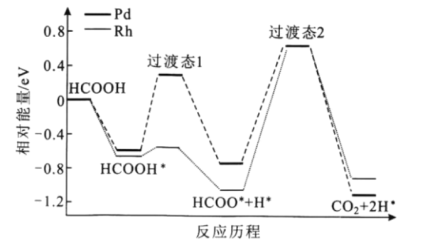
A.HCOOH吸附在催化剂表面是一个放热过程
B.Pd、Rh作催化剂时HCOOH分解产生H2的反应热不同
C.该反应过程中有C-H键的断裂,还有C=O键的生成
D.HCOO*+H*=CO2+2H*是该历程的决速步骤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用如图装置可以验证非金属性的变化规律。
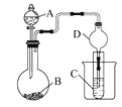
(1)仪器A的名称为________,干燥管D的作用是________________。
(2)已知在常温下,高锰酸钾和浓盐酸反应能生成氯气。实验室中现有药品Na2S溶液、KMnO4、浓盐酸、MnO2,请选择合适药品设计实验验证氯的非金属性大于硫的;装置A、B、C中所装药品分别为________、________、________,装置C中的实验现象为_________________,离子方程式为______。
(3)若要证明非金属性:S>C>Si,则A中加________、B中加Na2CO3、C中加________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮和氮的化合物在工农业生产、国防和生活中都有极其广泛的用途。请回答下列与氮元素有关的问题:
(1)亚硝酸氯(结构式为Cl-N=O)是有机合成中的重要试剂,可由Cl2和NO在通常反应条件下制得,反应方程式为2NO(g)+Cl2(g) 2ClNO(g)。已知几种化学键的键能数据如表所示:

当Cl2与NO反应生成ClNO的过程中转移了4mol电子,理论上放出的热量为___kJ。(用数字和字母表示)
(2)温度一定时,在一个体积为1L的密闭容器中通入2moNO和1molCl2,10min时ClNO体积占气体总体积40%,反应开始到10min内NO的平均V(NO)=____mol·L-1·min-1。
(3)利用电化学原理,将NO2、O2和熔融KNO3制成燃料电池,装置如图所示:
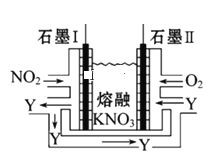
电池工作时,NO2转变成绿色硝化剂Y(N2O5),可循环使用,则石墨Ⅱ为电源___极,石墨Ⅱ附近发生的电极反应式为____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值,下列叙述正确的是
A.1mol 铁和高温水蒸气完全反应转移的电子数为2NA
B.常温常压下,1mol 氦气含有的原子数为NA
C.标准状况下,11. 2 L 乙醇含有的分子数目为0. 5NA
D.物质的量浓度为0.5 mol/L的MgCl2溶液中,含有Cl- 个数为 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】普通水泥在固化过程中其自由水分子减少并形成碱性溶液。根据这一物理化学特点,科学家发明了电动势法测水泥的初凝时间。此法的原理如图所示,反应的总方程式为:2Cu+Ag2O=Cu2O+2Ag。下列有关说法正确的是
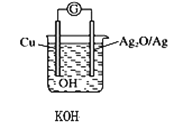
A.2molCu与1 molAg2O的总能量低于1 molCu2O与2molAg具有的总能量
B.负极的电极反应式为2Cu+2OH--2e-=Cu2O+H2O
C.测量原理示意图中,电流方向从Cu流向Ag2O
D.电池工作时,OH-向Ag电极移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电炉加热时用纯氧气氧化管内样品,根据产物的质量确定有机物的组成,下图装置是用燃烧法确定有机物M分子式的常用装置。
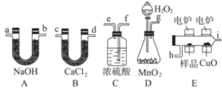
(1)产生的氧气按从左到右方向流动,所选装置各导管的连接顺序是______________________;
(2)C装置中浓硫酸的作用是___________________;
(3) 若准确称取有机物M (只含C、H、O三种元素中的两种或三种) 0.70 g,经充分燃烧后,A管质量增加2.2 g,B管质量增加0.9 g,则该有机物的实验式为__________________;
(4)已知在相同条件下该M蒸气相对氢气的密度为35,则M的分子式为_____________。若有机物M不能使溴水褪色,且其核磁共振氢谱只有一个吸收峰,则M的结构简式为________________。若该有机物M分子中所有碳原子一定都在同一平面内,且能使溴水褪色,在催化剂作用下能与H2加成,其加成产物分子中含有3个甲基,则M的结构简式为_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知H2SO3、H2CO3分别属于中强酸和弱酸,H2SO3![]() H++HSO3-,HSO3-
H++HSO3-,HSO3-![]() H++SO32-;H2CO3
H++SO32-;H2CO3![]() H++HCO3-;HCO3-
H++HCO3-;HCO3-![]() H++CO32-;电离平衡常数分别为K1、K′1、K2、K′2,已知K1>K′1≈K2>K′2,则溶液中不可以大量共存的离子组是 ( )
H++CO32-;电离平衡常数分别为K1、K′1、K2、K′2,已知K1>K′1≈K2>K′2,则溶液中不可以大量共存的离子组是 ( )
A. SO32-、HCO3-B. HSO3-、CO32-C. SO32-、CO32-D. HSO3-、HCO3-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com