
【题目】根据实验室制备氯气的装置(如下),回答下列问题;

(1)仪器A 和 B名称___________ ;____________
(2)写出B中发生反应的离子方程式_____________________________________
(3)装置C的作用__________________________________________
(4)装置D的作用________________________________________________
(5)检验E中氯气已经收集满的方法_________________________________________
(6)写出F中发生的反应方程式______________________________________________
(7)每生成0.5mol氯气转移________________个电子
【答案】分液漏斗 圆底烧瓶 MnO2+4H++2Cl-![]() Mn2++Cl2↑+2H2O 除去氯气中的HCl 除去氯气中的水蒸气 E装置右端的导管口放置湿润的淀粉碘化钾试纸,试纸变蓝,则证明氯气收集满 Cl2+2NaOH=NaCl+NaClO+H2O NA
Mn2++Cl2↑+2H2O 除去氯气中的HCl 除去氯气中的水蒸气 E装置右端的导管口放置湿润的淀粉碘化钾试纸,试纸变蓝,则证明氯气收集满 Cl2+2NaOH=NaCl+NaClO+H2O NA
【解析】
(1)根据装置图示判断仪器名称;
(2)浓盐酸与二氧化锰在加热条件下反应制取氯气;
(3)制取的氯气中含有挥发出来的氯化氢;
(4)制取的氯气中含有水蒸汽;
(5)氯气可使湿润的淀粉碘化钾试纸变蓝;
(6)氯气和氢氧化钠溶液反应生成氯化钠、次氯酸钠和水;
(7)根据反应MnO2+4H++2Cl-![]() Mn2++Cl2↑+2H2O,结合氧化还原反应规律分析计算。
Mn2++Cl2↑+2H2O,结合氧化还原反应规律分析计算。
(1)由图可知,A为分液漏斗,B为圆底烧瓶;
(2)用二氧化锰和浓盐酸制取氯气的离子方程式为:MnO2+4H++2Cl-![]() Mn2++Cl2↑+2H2O;
Mn2++Cl2↑+2H2O;
(3)制取的氯气中混有HCl和水蒸气,装置C中饱和食盐水的作用是除去氯气中的HCl;
(4)制取的氯气中含有水蒸汽,装置D中浓硫酸的作用是除去氯气中的水蒸气;
(5)氯气可使湿润的淀粉碘化钾试纸变蓝,E装置右端的导管口放置湿润的淀粉碘化钾试纸,试纸变蓝,则证明氯气收集满;
(6)氯气和氢氧化钠溶液反应生成氯化钠、次氯酸钠和水,方程式为:Cl2+2NaOH=NaCl+NaClO+H2O;
(7)根据离子反应方程式:MnO2+4H++2Cl-![]() Mn2++Cl2↑+2H2O,生成1mol氯气反应中转移2mol电子,则每生成0.5mol氯气转移1mol电子,则电子数目为NA个。
Mn2++Cl2↑+2H2O,生成1mol氯气反应中转移2mol电子,则每生成0.5mol氯气转移1mol电子,则电子数目为NA个。


 课时训练江苏人民出版社系列答案
课时训练江苏人民出版社系列答案科目:高中化学 来源: 题型:
【题目】室温下,将0.05molCH3COONa固体溶于水配成100mL溶液,向溶液中加入下列物质充分混合后,有关结论不正确的是( )
加入的物质 | 结论 | |
A | 0.05molCH3COONa固体 |
|
B | 0.05molNaHSO4固体 | c(CH3COO﹣)+c(CH3COOH)=c(Na+)﹣c(SO42﹣) |
C | 0.05molNH4Cl固体 | 水电离程度增大 |
D | 50mLH2O | 由水电离出的c(H+)·c(OH﹣)减小 |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上制备相关物质,涉及的反应原理及部分流程较为合理的是
A. 制取镁:海水![]() Mg(OH)2
Mg(OH)2![]() MgO
MgO![]() Mg
Mg
B. 冶炼铝:铝土矿![]() NaAlO2
NaAlO2![]() 无水AlCl3
无水AlCl3![]() Al
Al
C. 制硝酸:N2、H2 ![]() NH3
NH3![]() NO
NO![]() 50%HNO3
50%HNO3 ![]() 浓HNO3
浓HNO3
D. 海带![]() 海带灰
海带灰![]()
![]() I2(aq)
I2(aq)![]() I2
I2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】含镍(Ni)质量分数约20%废料,主要成分是铁镍合金,还含有铜、钙、镁、硅的氧化物。由该废料制备纯度较高的氢氧化镍,工艺流程如下:
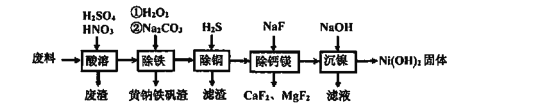
回答下列问题:
(1)合金中的镍难溶于稀硫酸,“酸溶”时除了加入稀硫酸,还要边搅拌边缓慢加入稀硝酸,反应有N2生成。写出金属镍溶解的化学方程式______________________
(2)“除铁”时H2O2的作用是________________,为了证明添加的H2O2已足量,应选择的试剂是_______________ (填序号:“①铁氰化钾K3[Fe(CN)6]”或“②硫氰化钾KSCN”)溶液.黄钠铁矾[NaxFey(SO4)m(OH)n]具有沉淀颗粒大、沉淀速率快、容易过滤等特点,则x:y:m:n=1:____:2:6
(3)“除铜”时,反应的离子方程式为________________
(4)已知Ksp(MgF2)=7.35×10-11、Ksp(CaF2)=1.05×10-10,当加入过量NaF“除钙镁”后,所得滤液中![]() ________________(保留1位小数)。已知除杂过程在陶瓷容器中进行,NaF的实际用量不宜过大的原因是__________
________________(保留1位小数)。已知除杂过程在陶瓷容器中进行,NaF的实际用量不宜过大的原因是__________
(5)100kg废料经上述工艺制得Ni(OH)2固体的质量为31kg,则镍回收率为______________(保留1位小数)
(6)镍氢电池已成为混合动力汽车的主要电池类型,其工作原理如下:M+Ni(OH)2![]() MH+NiOOH(式中M为储氢合金)。写出电池充电过程中阳极的电极反应式___________
MH+NiOOH(式中M为储氢合金)。写出电池充电过程中阳极的电极反应式___________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:PCl3的熔点为-112℃,沸点为75.5℃,遇水生成H3PO3和HCl;2PCl3+O2=2POCl3。某化学学习小组用装置甲合成PCl3,并用装置乙采取PCl3氧化法制备POCl3

(1)氯元素在周期表中的位置是_____________
(2)H3PO3中所含元素原子半径由小到大的顺序为_____________
(3)能比较出氯的非金属性比磷的非金属性强的是______________
A.HCl酸性比H3PO4的强 B.HCl稳定性比PH3的强
C.HClO4的酸性比H3PO3的强 D.PCl3中P显正三价,C1显负一价
(4)图甲碱石灰的作用除了处理尾气外还有防止_____________进入烧瓶,影响产品纯度的作用
(5)图乙A装置中化学反应方程式是_____________
(6)POCl3水解的化学反应方程式为______________
(7)C中反应温度控制在60~65℃,其原因是____________________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关反应速率的说法正确的是:
A. 用铁片和稀硫酸反应制氢气时,改用98%的硫酸可以加快反应速率
B. 100 mL 2 molL﹣1的盐酸跟锌片反应,加入适量的氯化钠溶液,反应速率不变
C. 反应C(s)+H2O(g) ![]() CO(g)+H2(g)在一可变容积的密闭容器中进行,增加C的量 , 其反应速率增大
CO(g)+H2(g)在一可变容积的密闭容器中进行,增加C的量 , 其反应速率增大
D. 汽车尾气中的NO和CO可以缓慢反应生成N2和CO2,减小压强反应速率变慢:
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于Zn(s)+H2SO4(aq)=ZnSO4(aq)+H2(g)的化学反应,能量关系如下图,下列叙述正确的是( )

A.该反应为吸热反应
B.1 mol锌的能量高于1 mol H2所含的能量
C.若将该反应设计成原电池,锌为负极
D.若将其设计为原电池,当有32.5 g锌溶解时,正极放出气体一定为11.2 L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮氧化合物是目前造成大气污染的主要气体,而汽车尾气中就含有NO 等多种污染气体。汽车尾气里含有的NO气体是由于内燃机燃烧的高温引起氮气和氧气反应所致。请结合所学知识回答下列问题:
(1) 已知:N2(g)+2O2(g)![]() 2NO2(g) △H1=+67.8 kJ/mol
2NO2(g) △H1=+67.8 kJ/mol
2NO2(g)![]() O2(g)+2NO(g) △H2=+116.2 kJ/mol
O2(g)+2NO(g) △H2=+116.2 kJ/mol
则N2(g)+O2(g)![]() 2NO(g) △H=_________kJ/mol;汽车启动后,气缸温度越高,单位时间内NO 的排放量越大,分析其原因为_____________
2NO(g) △H=_________kJ/mol;汽车启动后,气缸温度越高,单位时间内NO 的排放量越大,分析其原因为_____________
(2) 若反应N2(g)+O2(g)![]() 2NO(g)是在恒容条件下进行,下列能说明该反应已达到平衡状态的是________
2NO(g)是在恒容条件下进行,下列能说明该反应已达到平衡状态的是________
a.2υ正(N2)= υ逆(NO) b.混合气体密度不变
c.生成1molO2的同时生成2molNO d.混合气体平均相对分子质量不变
(3) 汽车尾气净化反应:2NO(g)+2CO(g)![]() N2(g)+2CO2(g) △H= -746.5 kJ/mol,若将0.20molNO和0.10molCO充入一个容积恒定为1L 的密闭容器中,在不同条件下,反应过程中部分物质的浓度变化状况如图所示:
N2(g)+2CO2(g) △H= -746.5 kJ/mol,若将0.20molNO和0.10molCO充入一个容积恒定为1L 的密闭容器中,在不同条件下,反应过程中部分物质的浓度变化状况如图所示:
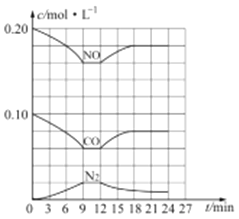
①该反应能自发进行的条件为_____ (填“高温”、“低温”或“任意温度”);
②在6~9 min 内,以CO 表示的平均反应速率 υ(CO)=________mol·L-l·min-1;
③第12min时改变的反应条件为_________ (填“升高温度”或“降低温度”);
④反应在第24min时的平衡常数K=____________(只列出计算式,无需计算结果),若保持温度不变,再向容器中充入CO、N2 各0.060mol,平衡将_________移动(填“正向”、“逆向”或“不”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】标准状况下有以下四种气体:①6.72L CH4 ②3.01×1023 HCl分子③13.6g H2S ④0.2mol NH3。下列对四种气体的关系从小到大表示不正确的是( )
A.物质的量:④<①<③<②B.体积:④<①<②<③
C.质量:④<①<③<②D.氢原子个数:②<④<③<①
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com