
下列有机化合物中均含有酸性杂质,除去这些杂质的方法中正确的是
A.苯中含苯酚杂质:加入溴水,过滤
B.乙醇中含乙酸杂质:加入碳酸钠溶液洗涤,分液
C.乙醛中含乙酸杂质:加入氢氧化钠溶液洗涤,分液
D.乙酸丁酯中含乙酸杂质:加入碳酸钠溶液洗涤,分液
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案科目:高中化学 来源: 题型:
Ⅰ.实验室有一瓶失去标签的某白色固体X,已知其成分可能是碳酸或亚硫酸的钠盐或钾盐,且其成分单一。现某化学小组通过如下步骤来确定其成分:
(1)阳离子的确定:
实验方法及现象:________________________________________________________。
结论:此白色固体是钠盐。
(2)阴离子的确定:
①取少量白色固体于试管中,然后向试管中加入稀盐酸,白色固体全部溶解,产生无色气体,此气体能使溴水褪色。
②要进一步确定其成分需补做如下实验:取适量白色固体配成溶液,取少许溶液于试管中,加入BaCl2溶液,出现白色沉淀。
Ⅱ.确认其成分后,由于某些原因,此白色固体部分被空气氧化,该化学小组想用已知浓度的酸性KMnO4溶液来确定变质固体中X的含量,具体步骤如下:
步骤Ⅰ 称取样品1.000 g。
步骤Ⅱ 将样品溶解后,完全转移到250 mL容量瓶中,定容,充分摇匀。
步骤Ⅲ 移取25.00 mL样品溶液于250 mL锥形瓶中,用0.01 mol·L-1KMnO4标准溶液滴定至终点。
按上述操作方法再重复2次。
(1)写出步骤Ⅲ所发生反应的离子方程式_____________________________________
________________________________________________________________________。
(2)在配制0.01 mol·L-1KMnO4溶液时若仰视定容,则最终测得变质固体中X的含量________(填“偏大”、“偏小”或“无影响”)。
(3)滴定结果如下表所示:
| 滴定次数 | 待测溶液的体积/mL | 标准溶液的体积 | |
| 滴定前刻度/mL | 滴定后刻度/mL | ||
| 1 | 25.00 | 1.02 | 21.03 |
| 2 | 25.00 | 2.00 | 21.99 |
| 3 | 25.00 | 2.20 | 20.20 |
则该变质固体中X的质量分数为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列水解 的离子方程式正确的是
的离子方程式正确的是
A.HCO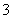 +H2O
+H2O CO2↑+OH-
CO2↑+OH-
B.S2-+2H2O H2S+2OH-
H2S+2OH-
C.Fe3++3H2O Fe(OH)3↓+3H+
Fe(OH)3↓+3H+
D.CO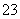 +H2O
+H2O HCO
HCO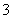 +OH-
+OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
(Ⅰ)常温下,将某一元酸HA(甲、乙、丙、丁代表不同的一元酸)和NaOH溶液等体积混合,两种溶液的物质的量浓度和混合溶液的pH如表所示:
| 实验 编号 | HA的物质的量 浓度(mol·L-1) | NaOH的物质的量 浓度(mol·L-1) | 混合后溶 液的pH |
| 甲 | 0.1 | 0.1 | pH=a |
| 乙 | 0.12 | 0.1 | pH=7 |
| 丙 | 0.2 | 0.1 | pH>7 |
| 丁 | 0.1 |
| pH=10 |
(1)从甲组情况分析,如何判断HA是强酸还是弱酸?
________________________________________________________________________。
(2)乙组混合溶液中c(A-)和c(Na+)的大小关系是________。
A.前者大 B.后者大
C.二者相等 D.无法判断
(3)从丙组实验结果分析,该混合溶液中离子浓度由大到小的顺序是________________________________________________________________________。
(4)分析丁组实验数据,写出该混合溶液中下列算式的精确结果(列式):c(Na+)-c(A-)=________ mol·L-1。
(Ⅱ)某二元酸(化学式用H2B表示)在水中的电离方程式是:H2B===H++HB- HB-H++B2-。
(5)在0.1 mol·L-1的Na2B溶液中,下列粒子浓度关系式正确的是_____ ___。
___。
A.c(B2-)+c(HB-)=0.1 mol·L-1
B.c(B2-)+c(HB-)+c(H2B)=0.1 mol·L-1
C.c(OH-)=c (H+)+c(HB-)
(H+)+c(HB-)
D.c(Na+)+c(OH-)=c(H+)+c(HB-)
查看答案和解析>>
科目:高中化学 来源: 题型:
苯甲酸广泛应用于制药和化工行业。某同学尝试用甲苯的氧化反应制备苯甲酸。
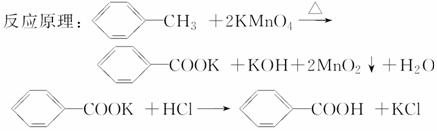
实验方法:一定量的甲苯和KMnO4溶液在100 ℃反应一段时间后停止反应,按如下流程分离出苯甲酸和回收未反应的甲苯。

已知:苯甲酸相对分 子质量122,熔点122.4 ℃,在25 ℃和95 ℃时溶解度分别为0.3 g和6.9 g;纯净固体有机物一般都有固定熔点。
子质量122,熔点122.4 ℃,在25 ℃和95 ℃时溶解度分别为0.3 g和6.9 g;纯净固体有机物一般都有固定熔点。
(1)操作Ⅰ为________,操作Ⅱ为________。
(2)无色液体A是____________,定性检验A的试剂是________,现象是________________________________________________________________________。
(3)测定白色固体B的熔点,发现其在115 ℃开始熔化,达到130 ℃时仍有少量不熔。该同学推测白色固体B是苯甲酸与KCl的混合物,设计了如下方案进行提纯和检验,实验结果表明推测正确。请完成表中内容。
| 序号 | 实验方案 | 实验现象 | 结论 |
| ① | 将白色固体B加入水中,加热溶解,________ | 得到白色晶体和无 | |
| ② |
| 生成白色沉淀 | 滤液含Cl |
| ③ | 干燥白色晶体,________ | 白色晶体是苯甲酸 |
(4)纯度测定:称取1.220 g产品,配成100 mL甲醇溶液,移取25.00 mL溶液,滴定,消耗KOH的物质的量为2.40×10-3 mol。产品中苯甲酸质量分数的计算表达式为________,计算结果为________(保留二位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
2丁烯是石油裂解的产物之一,回答下列问题:
(1)在催化剂作用下,2丁烯与氢气反应的化学方程式为
________________________________________________________________________,
反应类型为____________。
(2)烯烃A是2丁烯的一种同分异构体,它在催化剂作用下与氢气反应的产物不是正丁烷,则A的结构简式为______________________________________________________________;
A分子中能够共平面的碳原 子个数为________,A与溴的四氯化碳溶液反应的化学方程式为_______________________________________________________________________。
子个数为________,A与溴的四氯化碳溶液反应的化学方程式为_______________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
有关溶液中所含离子的检验,下列判断中正确的是( )
A.加入硝酸酸化,再滴加KSCN溶液后有红色物质生成,则原溶液中一定有Fe3+存在
B.加入盐酸有能使澄清石灰水变浑浊的气体生成,则原溶液中一定有大量的CO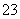 存在
存在
C.用某溶液做焰色反应实验时火焰为黄色,则该溶液中一定有钠元素,可能有钾元素
D.分别含有Mg2+、Cu2+、Fe2+和Na+的四种盐酸盐溶液,只用NaOH溶液是不能一次鉴别开的
查看答案和解析>>
科目:高中化学 来源: 题型:
下列金属冶炼的反应原理,错误的是( )
A.2NaCl(熔融) 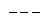 2Na+Cl2↑ B.MgO+H2
2Na+Cl2↑ B.MgO+H2 Mg+H2O
Mg+H2O
C.Fe3O4+4CO 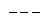 3Fe+4CO2 D.2HgO
3Fe+4CO2 D.2HgO 2Hg + O2↑
2Hg + O2↑
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com