
【题目】在三个容积均为2L的密闭容器中发生反应:2HI(g) ![]() H2(g)+I2(g),已知H2(g)和I2(g)的起始物质的量均为0,HI(g)的物质的量随反应时间和温度的变化情况如表所示:
H2(g)+I2(g),已知H2(g)和I2(g)的起始物质的量均为0,HI(g)的物质的量随反应时间和温度的变化情况如表所示:
(1)实验1和实验2中使用了催化剂的实验是(填“1”或“2”);
(2)实验1中,010min内生成H2的平均反应速率为 molL﹣1min﹣1;
(3)实验3的反应达到化学反应限度时,HI(g)转化率为。
【答案】
(1)2
(2)0.005
(3)80%
【解析】解:(1)根据表中数据可知实验1和实验2相比较起始量相同,但达到平衡的时间是实验2用时少,这说明实验2中反应速快,因此使用了催化剂的实验是2;(2)根据表中数据可知实验1中,010min内消耗碘化氢是1mol-0.8mol=0.2mol,则根据方程式可知生成氢气是0.1mol,浓度是0.1mol÷2L=0.05mol/L,所以生成H2的平均反应速率为0.05mol/L÷10min=0.005molL﹣1min﹣1;(3)根据表中数据可知实验3中平衡时消耗碘化氢是1mol-0.2mol=0.8mol,所以反应达到化学反应限度时,HI(g)转化率为 ![]() 。
。
本题考察化学反应平衡的影响、反应速率及转换率的计算。
平均速率v=△c/△t
转化率ω=n(反应)/n(总)


 轻松暑假总复习系列答案
轻松暑假总复习系列答案科目:高中化学 来源: 题型:
【题目】向含有KBr和KI的混合溶液中通入过量的Cl2充分反应后,将溶液蒸干,并灼烧所得的物质,最后剩余的固体物质是( )
A.KCl和KIB.KBrC.KClD.KCl和I2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】主族元素在周期表中的位置取决于该元素的原子的( )
A.相对原子质量和核外电子数 B.电子层数和最外层电子数
C.相对原子质量和最外层电子数 D.电子层数和次外层电子数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图装置,将溶液A逐滴加入固体B中,下列叙述中不正确的是( ) 
A.若A为浓硫酸,B为Na2SO3固体,C中盛石蕊溶液,则C中溶液先变红后褪色
B.若A为醋酸溶液,B为贝壳,C中盛过量澄清石灰水,则C中溶液变浑浊
C.若A为浓盐酸,B为MnO2 , C中盛品红溶液,则C中溶液不褪色
D.若A为浓氨水,B为生石灰,C中盛AlCl3溶液,则C中产生白色沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2015年,中国科学家屠呦呦获得了诺贝尔医学奖,因为发现青蒿素,一种用于治疗疟疾的药物,挽救了全球特别是发展中国家的数百万人的生命.
如图是青蒿素的结构,则有关青蒿素的说法中不正确的是( )
A.青蒿素分子式为C15H22O5
B.青蒿素易溶于乙醇、苯
C.青蒿素因含有﹣O﹣(醚键)而具有较强的氧化性
D.青蒿素在碱性条件下易发生水解反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硼泥主要由MgO和SiO2组成,含有少量Fe2O3、FeO、Al2O3等杂质.用硼泥生产氢氧化镁的工艺流程如图所示: 
已知某些氢氧化物沉淀的pH如下表所示:
氢氧化物 | 开始沉淀时的pH | 完全沉淀时的pH |
Mg(OH)2 | 9.3 | 10.8 |
Fe(OH)2 | 7.6 | 9.6 |
Fe(OH)3 | 2.7 | 3.7 |
(1)MgO的电子式为 .
(2)滤渣2的主要成分是 , 向滤渣2中继续加入过量的NaOH溶液,发生反应的离子方程式为 .
(3)加入NaOH调节溶液pH=12.0时,发生反应的离子方程式为 .
(4)利用Mg(OH)2与含SO2的烟气反应生成MgSO4 , 可以使烟气脱硫,该反应的化学方程式为 .
(5)若取a吨硼泥为原料,最后得到b吨Mg(OH)产品(假设生产过程中镁元素无损失),则硼泥中MgO的质量分数为(用含有a、b的代数式表示).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
(1)苯、四氯化碳、乙醇、汽油是常见的有机溶剂,能与水互溶的是 , 不溶于水,且密度比水小的是。
(2)写出下列反应的化学方程式并注明反应类型
① 用乙烷制备氯乙烷(C2H5Cl) , ;
② 乙烯与水反应制乙醇 , ;
③ 苯制取溴苯 , 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知甲、乙、丙和X是四种中学化学中常见的物质,其转化关系如下图,则甲和X不可能是( )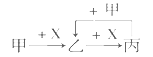
A.甲为C,X是O2
B.甲为SO2 , X是NaOH溶液
C.甲为Cl2 , X为Fe
D.甲为Al,X为NaOH溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数A<B<C<D<E.其中A、C原子都有两个未成对的单电子,D的二价阳离子与C的阴离子具有相同的电子层结构. B、C的氢化物的沸点比它们同族相邻周期元素氢化物的沸点高.E的原子序数为24,ECl3能与B、C的氢化物形成六配位的配合物,且两种配体的物质的量之比为2:1,三个氯离子位于外界.请根据以上情况,回答下列问题(答题时,A、B、C、D、E用所对应的元素符号表示)
(1)A、B、C的第一电离能由小到大的顺序为 .
(2)B的氢化物的分子空间构型是 , 其中心原子的杂化方式是 .
(3)AC2的电子式 , 是分子(填“极性”或“非极性”),一种由B、C组成的化合物与AC2互为等电子体,其化学式为
(4)E的核外电子排布式是 , ECl3与B、C的氢化物形成的配合物的化学式为 .
(5)B的最高价氧化物对应的水化物的稀溶液与D的单质反应时,B被还原到最低价,该反应的化学方程式是 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com