
Ⅰ、取少量Fe2O3粉末,向其中加入适量盐酸使其充分溶解。
(1)上述反应的化学方程式为 反应后得到的溶液呈 色。
(2)取少量上述溶液,置于试管中,滴入NaOH溶液,可观察到有 色沉淀生成,发生反应的化学方程式为:此反应属于 (填基本反应类型)反应。
Ⅱ、(3)在甲烧杯中加入20mL蒸馏水,加热至沸腾后,向沸水中滴入几滴 FeCl3 溶液,继续煮沸直至溶液呈 色,停止加热,即可以制得Fe(OH)3胶体。制备Fe(OH)3胶体的化学方程式:
(4)另取乙烧杯,加入20mL蒸馏水,向烧杯中加入1mL FeCl3溶液,震荡均匀后,将乙烧杯与甲烧杯一起置于暗处,分别用激光笔照射烧杯中的液体,可以看到 烧杯中的液体产生 ,这个实验可以用来区别 。
(5)取甲烧杯中的少量Fe(OH)3胶体于试管中,向试管中逐滴滴加稀盐酸,
现象: ,原因: ,
如果有反应,方程式为:
 走进文言文系列答案
走进文言文系列答案科目:高中化学 来源:2015-2016学年山东省淄博市高二上学期期中测试化学试卷(解析版) 题型:填空题
已知2A(g)+B(g) 2C(g),向容积为1L的密闭容器中加入0.050 mol A和0.025mol B,在500℃时充分反应,达平衡后测得c(C)=0.010 mol·L-1,放出热量Q1kJ。
2C(g),向容积为1L的密闭容器中加入0.050 mol A和0.025mol B,在500℃时充分反应,达平衡后测得c(C)=0.010 mol·L-1,放出热量Q1kJ。
(1)能说明上述反应已经达到化学平衡状态的是 (填写序号);
A.v逆(A)=2v正(B) B.容器内压强保持不变
C.v(C)=2v(B) D.容器内气体的密度保持不变
(2)若在相同的容器中加入0.100 mol A和0.050molB,500℃时充分反应达平衡后,放出热量Q2kJ,则2Q1 Q2(填“>”、“<”或“=”);
(3)500℃时,上述反应的化学平衡常数K= ;
(4)已知:K(300℃)<K(350℃),该反应是 (填“放热”或“吸热”)热反应;若反应温度升高,A的转化率 (填“增大”、“减小”或“不变”);
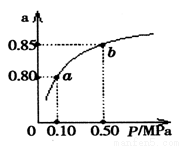
(5)某温度下,A的平衡转化率(a)与体系总压强(P)的关系如图所示,平衡状态由a变到b时,化学平衡常数K(A) K(B)(填“>”、“<”或“=”)。
查看答案和解析>>
科目:高中化学 来源:2016届湖北省襄阳市高三上学期期中测试化学试卷(解析版) 题型:选择题
工业上常用还原沉淀法处理含铬废水(Cr2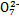 和Cr
和Cr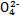 ),其流为:
),其流为:
Cr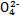
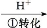 Cr2
Cr2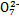
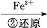 Cr3+
Cr3+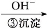 Cr(OH)3↓
Cr(OH)3↓
已知:
(1)步骤①中存在平衡:2Cr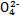 (黄色)+2H+
(黄色)+2H+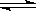 Cr2
Cr2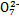 (橙色)+H2O
(橙色)+H2O
(2)步骤③生成的Cr(OH)3在溶液中存在以下沉淀溶解平衡:
Cr(OH)3(s) 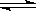 Cr3+(aq)+3OH-(aq)
Cr3+(aq)+3OH-(aq)
(3)常温下,Cr(OH)3的溶度积Ksp=10-32;且当溶液中离子浓度小于10-5 mol·L-1时可视作该离子不存在
下列有关说法中正确的是
A.步骤①中加酸,将溶液的pH调节至2,溶液显黄色,Cr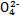 浓度增大
浓度增大
B.步骤①中当2v(Cr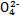 )=v(Cr2
)=v(Cr2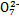 )时,说明反应2Cr
)时,说明反应2Cr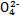 (黄色)+2H+
(黄色)+2H+  Cr2
Cr2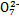 (橙色)+H2O达到平衡状态
(橙色)+H2O达到平衡状态
C.步骤②中,若要还原1 mol Cr2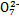 ,需要12 mol (NH4)2Fe(SO4)2·6H2O
,需要12 mol (NH4)2Fe(SO4)2·6H2O
D.步骤③中,当将溶液的pH调节至6时,则可认为废水中的铬已除尽
查看答案和解析>>
科目:高中化学 来源:2016届江苏省盐城市高三上学期期中测试化学试卷(解析版) 题型:选择题
最近美国宇航局的科研人员确认火星地表含有溶有高氯酸盐的液态水。下列有关水及高氯酸盐的说法错误的是
A.水是一种弱电解质
B.NH4ClO4溶液显酸性
C.NaClO4中含有离子键和共价键
D.NH4ClO4只有氧化性,没有还原性
查看答案和解析>>
科目:高中化学 来源:2015-2016学年黑龙江省高二上一次月考化学试卷(解析版) 题型:选择题
已知HA的酸性比HB的酸性强。现有物质的量浓度和体积均相同的NaA和NaB两种溶液,已知前者溶液中离子数目为n1,后者溶液中离子数目为n2。下列关系正确是
A. n1=n2 B. n1>n2
C. n1<n2 D.c(A—)<c(B—)
查看答案和解析>>
科目:高中化学 来源:2015-2016学年黑龙江哈尔滨六中高一10月月考化学试卷(解析版) 题型:选择题
现有三组溶液:①碘的饱和水溶液 ②汽油和氯化钠溶液 ③碳酸钙和水,分离以上各混合液的正确方法依次是
A. 萃取、分液、过滤 B. 萃取、分液、蒸馏
C. 分液、蒸馏、过滤 D. 蒸馏、萃取、过滤
查看答案和解析>>
科目:高中化学 来源:2016届山东省高三上学期10月教学质检理综化学试卷(解析版) 题型:推断题
A、B、C、D、E、X是中学常见的无机物,存在如下图转化关系(部分生成物和反应条件略去)。
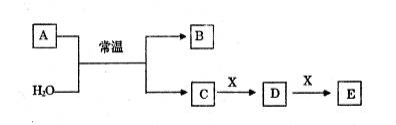
(1)若A为常见的金属单质,焰色反应呈黄色,X能使品红溶液褪色,写出C和E反应的离子方程式:_______________________。
(2)若A为短周期元素组成的单质,该元素的最高价氧化物的水化物酸性最强,则:
①组成单质A的元素在周期表中的位置为______________________。
②X可能为__________________(填代号)。
a.NaHCO3 b.Na2CO3 c.Na2SO3 d.Al(OH)3
(3)若A为淡黄色粉末,回答下列问题:
①A与H2O反应的氧化产物为_____________。
②若X为非金属单质,通常为黑色粉末,写出E的化学式______________。
③若X为一种造成温室效应的气体。则鉴别等浓度的D、E两种溶液,可选择的试剂为___________(填代号)。
a.盐酸 b.BaCl2溶液 c.NaOH溶液 d.Ca(OH)2溶液
(4)若A为氧化物,X是Fe,溶液D中加入KSCN溶液变红。
①A与H2O反应的化学反应方程式为____________________________。
②检验溶液D中还可能存在Fe2+的方法是____________________________(注明试剂、现象)。
查看答案和解析>>
科目:高中化学 来源:2016届山西省高三上学期10月月考化学试卷(解析版) 题型:选择题
化学与生活、生产密切相关,下列说法正确的是
A.碳酸钡、碳酸氢钠、氢氧化铝均可作为抗酸药物使用
B.人体内的蛋白质不断分解,最终生成水和二氧化碳排出体外
C.工业生产玻璃和水泥,均需要用纯碱为原料
D.“地沟油”的主要成分是油脂,其组成与汽油、煤油不相同
查看答案和解析>>
科目:高中化学 来源:2016届河北省保定市高三上学期摸底考试化学试卷(解析版) 题型:选择题
X、Y、Z是3种短周期元素,其中X、Z位于同一主族,X、Y处于同一周期。X原子的最外层电子数是其电子层数的3倍。X原子的核外电子数比Y原子少1。下列说法正确的是
A.元素非金属性由弱到强的顺序为Z<Y<X
B. Y元素的氢化物溶于水是一种强酸
C. 3种元素的气态氢化物中,Y的气态氢化物还原性最强
D.其对应的阴离子半径由大到小的顺序为Zn->Xn->Ym-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com