
【题目】(1)在配合物Fe(SCN)2+中提供空轨道接受孤电子对的微粒是____(填符号),配合物离子[Cu(NH3)4]2+为平面正方形结构, 画出其中的配位键_____________。
(2)配合物Co[(N3)(NH3)5]SO4中Co3+的配位数为___,Co3+与NH3之间的作用属于_____(选填“离子键”、“配位键”、“范德华力”、“氢键”)。
(3)Co(Ⅲ)的八面体配合物CoClm·nNH3,若1 mol配合物与AgNO3作用生成1 molAgCl沉淀,则m=__________, n= ___________。(填具体数值)
【答案】 Fe3+ 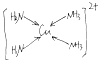 6 配位键 3 4。
6 配位键 3 4。
【解析】(1)配合物Fe(SCN)2+中,Fe3+提供空轨道,SCN-离子提供孤电子对。配合离子[Cu(NH3)4]2+中Cu2+提供空轨道,NH3分子中N原子提供孤电子对,结构是: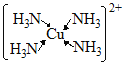 。正确答案:Fe3+、
。正确答案:Fe3+、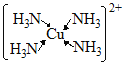 。(2)配合物Co[(N3)(NH3)5]SO4中Co3+的配位粒子包括1个N3-和5个NH3,配位数为6,Co3+与NH3之间形成配位键。正确答案:6、配位键。(3)八面体配合物配位数为6,因为NH3是电中性分子,Co为3价,则含有的Cl-数目是3,“1 mol配合物与AgNO3作用生成1 molAgCl沉淀”说明配合物外界含有1个Cl-,配位的Cl-为2,所以配位的NH3分子为4。正确答案:3、4。
。(2)配合物Co[(N3)(NH3)5]SO4中Co3+的配位粒子包括1个N3-和5个NH3,配位数为6,Co3+与NH3之间形成配位键。正确答案:6、配位键。(3)八面体配合物配位数为6,因为NH3是电中性分子,Co为3价,则含有的Cl-数目是3,“1 mol配合物与AgNO3作用生成1 molAgCl沉淀”说明配合物外界含有1个Cl-,配位的Cl-为2,所以配位的NH3分子为4。正确答案:3、4。


科目:高中化学 来源: 题型:
【题目】在四种化合物①NaHCO3、②Al(OH)3、③(NH4)2S、④NH2-CH2COOH中盐酸和氢氧化钠溶液都能反应的是
A. ①②③④ B. 只有①② C. 只有②④ D. 只有①②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学选修5:有机化学基础]由化合物A 制备一种医药合成中间体G和可降解环保塑料PHB的合成路线如下:
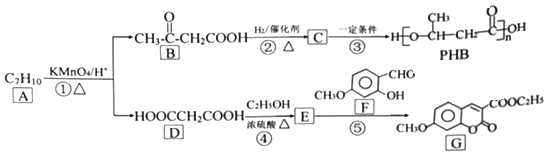
己知: ![]() (-R1、-R2、-R3 均为烃基)
(-R1、-R2、-R3 均为烃基)
回答下列问题:
(1)A的结构简式____________________,G中含氧官能团的名称____________________。
(2)反应③和④的反应类型分别是_____________________、____________________________。
(3)F的分子式为________________________。
(4)E是二元酯,其名称是__________________,反应④的化学方程式____________________。(5) C 存在多种同分异构体,其中分别与足量的NaHCO3溶液和Na反应产生气体的物质的量相同的同分异构体的数目为______种。
(6)写出用B为起始原料制备高分子化合物![]() 的合成路线(其他试剂任选)。
的合成路线(其他试剂任选)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将物质X逐渐加入(或通入)Y溶液中,其生成沉淀的量与加入X的物质的量的关系如下图所示,符合图示情况的是( )
| A | B | C | D |
X | CO2 | HCl | NaOH | AlCl3 |
Y | Ca(OH)2 | NaAlO2 | AlCl3 | NaOH |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)在BF3分子中,F—B—F的键角是________,B原子的杂化轨道类型为________,BF3和过量NaF作用可生成NaBF4,BF4-的立体构型为________。
(2)按要求写出由第二周期元素为中心原子,通过sp3杂化形成中性分子的化学式(各写一种):正四面体分子__________,三角锥形分子__________,V型分子__________。
(3)已知白磷(P4)的结构为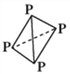 ,可知每个磷原子以___个共价键与另外的___磷原子结合成正四面体结构,它应该是________分子(填“极性”或“非极性”),在CS2中______(填“能”或“不能”)溶解,P原子的杂化方式为______________。
,可知每个磷原子以___个共价键与另外的___磷原子结合成正四面体结构,它应该是________分子(填“极性”或“非极性”),在CS2中______(填“能”或“不能”)溶解,P原子的杂化方式为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:CO(g)+H2O(g)![]() CO2(g)+H2(g) △H=-41kJ/mol,相同温度下,在体积相同的两个恒温密闭容器中,加入一定量的反应物发生反应。相关数据如下:
CO2(g)+H2(g) △H=-41kJ/mol,相同温度下,在体积相同的两个恒温密闭容器中,加入一定量的反应物发生反应。相关数据如下:
容器编号 | 起始时各物质物质的量/mol | 达平衡过程体系能量的变化 | |||
CO | H2O | CO2 | H2 | ||
① | 1 | 4 | 0 | 0 | 放出热量: 32.8 kJ |
② | 0 | 0 | 1 | 4 | 热量变化:Q |
下列说法中,不正确的是
A. 容器①中反应达平衡时,CO的转化率为80%
B. 容器①中的平衡常数等于容器②中平衡常数
C. Q=32.8
D. 容器①中CO反应速率等于H2O的反应速率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组利用下列装置进行电化学实验,下列实验操作及预期现象正确的是( )
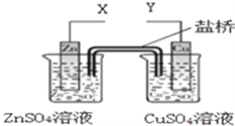
A. X和Y与电流表连接,Cu极为正极,发生氧化反应
B. X和Y与电流表连接,盐桥中的阴离子移向CuSO4溶液
C. X和Y分别与电源“﹣”、“+”极相连,Cu极质量减轻
D. X和Y分别与电源“+”、“﹣”极相连,Zn极电极反应为4OH﹣﹣4e﹣═O2↑+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一个恒温恒压的密闭容器中,有V2O5存在时发生反应:2SO2(g)+O2(g)![]() 2SO3(g)ΔH=-196.6KJ/mol。该反应过程为①SO2+V2O5
2SO3(g)ΔH=-196.6KJ/mol。该反应过程为①SO2+V2O5![]() SO3+2VO2、②……下列有关该反应的说法不正确的是
SO3+2VO2、②……下列有关该反应的说法不正确的是
A. 反应②是O2+4VO2![]() 2V2O5
2V2O5
B. V2O5降低了反应的活化能
C. 增大O2浓度时该反应的ΔH不变
D. 当2v(O2)逆=v(SO3)正时加入V2O5,等式仍然成立,v(O2)逆、v(SO3)正值不变
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com