
【题目】[化学选修5:有机化学基础]由化合物A 制备一种医药合成中间体G和可降解环保塑料PHB的合成路线如下:
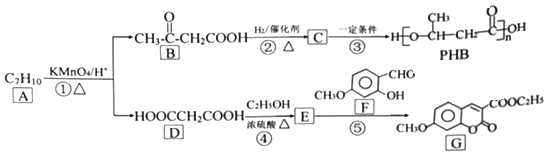
己知: ![]() (-R1、-R2、-R3 均为烃基)
(-R1、-R2、-R3 均为烃基)
回答下列问题:
(1)A的结构简式____________________,G中含氧官能团的名称____________________。
(2)反应③和④的反应类型分别是_____________________、____________________________。
(3)F的分子式为________________________。
(4)E是二元酯,其名称是__________________,反应④的化学方程式____________________。(5) C 存在多种同分异构体,其中分别与足量的NaHCO3溶液和Na反应产生气体的物质的量相同的同分异构体的数目为______种。
(6)写出用B为起始原料制备高分子化合物![]() 的合成路线(其他试剂任选)。
的合成路线(其他试剂任选)。
【答案】 ![]() ,醚键、酯基 缩聚反应、取代(酯化)反应 C8H8O3 丙二酸二乙酯 HOOC-CH2-COOH+2CH3CH2OH
,醚键、酯基 缩聚反应、取代(酯化)反应 C8H8O3 丙二酸二乙酯 HOOC-CH2-COOH+2CH3CH2OH![]() CH3CH2OOCCH2COOCH2CH3+2H2O 5
CH3CH2OOCCH2COOCH2CH3+2H2O 5 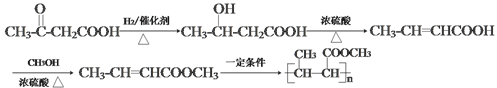
【解析】试题分析:根据![]() ,A被高锰酸钾氧化为
,A被高锰酸钾氧化为![]() 和
和![]() ,可知A是
,可知A是![]() ;
;![]() 与氢气发生加成反应生成C,C是
与氢气发生加成反应生成C,C是![]() ;
; ![]() 与乙醇反应生成E,E是二元酯
与乙醇反应生成E,E是二元酯![]() 。
。
解析:根据以上分析,(1)A的结构简式![]() ,
,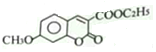 中含氧官能团的名称醚键和酯基。
中含氧官能团的名称醚键和酯基。
(2)![]()
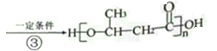 属于缩聚反应;
属于缩聚反应;![]() 与乙醇反应生成
与乙醇反应生成![]() ,属于取代反应。
,属于取代反应。
(3)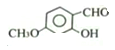 的分子式为C8H8O3。
的分子式为C8H8O3。
(4)E是二元酯![]() ,其名称是丙二酸二乙酯,
,其名称是丙二酸二乙酯,![]() 在浓硫酸作用下与乙醇反应生成
在浓硫酸作用下与乙醇反应生成![]() 的化学方程式是
的化学方程式是
HOOC-CH2-COOH+2CH3CH2OH![]() CH3CH2OOCCH2COOCH2CH3+2H2O。(5)与足量的NaHCO3溶液和Na反应产生气体的物质的量相同,说明分子中含有1个羟基、1个羧基,符合条件的
CH3CH2OOCCH2COOCH2CH3+2H2O。(5)与足量的NaHCO3溶液和Na反应产生气体的物质的量相同,说明分子中含有1个羟基、1个羧基,符合条件的的同分异构体有
![]() 、
、![]() 、
、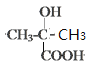 、
、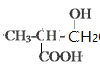 ,算上
,算上![]() 共5种;
共5种;
(6)用![]() 与氢气加成生成
与氢气加成生成![]() ,
,![]() 发生消去反应生成
发生消去反应生成![]() ,
,![]() 与甲醇发生酯化反应生成
与甲醇发生酯化反应生成![]() ,
,![]() 在一定条件下腐蚀加聚反应生成
在一定条件下腐蚀加聚反应生成![]() ,合成路线为
,合成路线为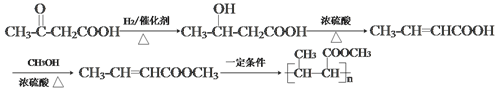 。
。


 考前必练系列答案
考前必练系列答案科目:高中化学 来源: 题型:
【题目】氮化镁(Mg3N2)在工业上具有非常广泛的应用。某化学兴趣小组用镁与氮气反应制备 Mg3N2 并进行有关实验。实验装置如下所示: (部分加热装置已略去)
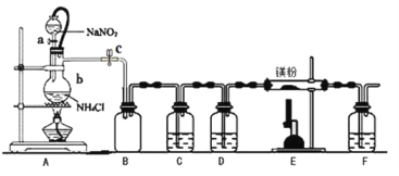
已知:①氮化镁常温下为浅黄色粉末,极易与水反应。
②亚硝酸钠和氯化铵制取氮气的反应剧烈放热,产生氮气的速度较快。
③温度较高时,亚硝酸钠会分解产生O2等。
回答下列问题:
(1)仪器 b 的名称是__________,写出装置 A 中发生反应的化学方程式___________。
(2)某同学检验装置 A 部分的气密性,关闭止水夹 c 后,开启活塞 a,水不断往下滴,直至全部流入烧瓶。试判断:
A 部分装置是否漏气? ________ (填“漏气”、“不漏气”或“无法确定”),判断理由是____________。
(3)装置 C 中为饱和硫酸亚铁溶液, 其作用是___________,装置 F 的作用是________。
(4)加热至反应开始发生,需移走 A 处酒精灯,原因是__________________。
(5)定性分析产物
操作步骤 | 实验现象 | 解释原因 |
取少量产品于试管中, 加适量蒸馏水 | 试管底部有固体不溶物,有剌激性气味的气体产生 | 反应的化学方程式为 __________________________________ |
弃去上层淸液, 加入足量稀盐酸 | 观察到固体全部溶解, 且有气泡冒出 | 气泡冒出的原因为___________________________________________________ |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列变化属于放热反应的是
①液态水汽化 ②将胆矾加热变为白色粉末 ③浓硫酸稀释
④氯酸钾分解制氧气 ⑤生石灰跟水反应生成熟石灰
A.①④B.⑤C.①④⑤D.②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮可以形成多种离子,如N3-,NH2-,N3-,NH4+,N2H5+,N2H62+等,已知N2H5+与N2H62+是由中性分子结合质子形成的,类似于NH4+,因此有类似于 NH4+的性质。
(1)N2H62+在碱性溶液中反应的离子方程式:_____________________________________。
(2)NH2-的电子式为__________________________,NH2-的构型为____________。
(3)写出一种与N3-是等电子体的微粒化学式___________。
(4)据报道,美国科学家卡尔·克里斯特于1998年11月合成了一种名为“N5”的物质,由于其具有极强的爆炸性,又称为 “盐粒炸弹”。迄今为止,人们对它的结构尚不清楚,只知道“N5”实际上是带正电荷的分子碎片,其结构是对称的,5个N排成V形。如果5个N结合后都达到8电子结构,且含有2个N![]() N键。则“N5”分子碎片所带电荷是_______。
N键。则“N5”分子碎片所带电荷是_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由二氧化硅制高纯硅的流程如下,下列判断中错误的是

A. ①②③均属于氧化还原反应 B. H2和HCl均可循环利用
C. SiO2是一种坚硬难熔的固体 D. SiHCl3摩尔质量为135.5g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过氧化钙是一种在水产养殖中广泛使用的供氧剂。某实验研究小组用下图所示的装置制取过氧化钙并测定产品的含量。
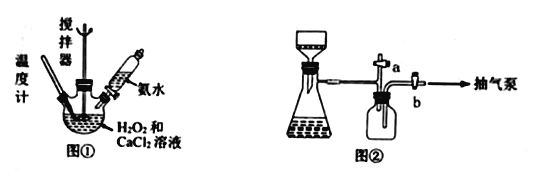
有关过氧化钙的性质如下:
外观与性状 | 溶解性 | 稳定性 | |
过氧化钙(CaO2) | 白色结晶,无臭无味, 有潮解性 | 难溶于水,且不溶于 乙醇、乙醚 | 常温下稳定,加热至 315℃时开始分解 |
回答下列问题:
I.过氧化钙的制备
称取7.5gCaCl2·H2O,用5mL水溶解,加入25mL 30%的H2O2,边搅拌边滴加由5mL 浓NH3·H2O和20mL冷水配成的溶液,保持在0-5℃下充分反应半小时后抽滤,得到粗产品CaO2·8H2O。分别用少量冷水、乙醇洗涤该产品2~3次,在150℃下烘0.5-1h,冷却得到产品无水过氧化钙。
(1)图①盛装“CaCl2和H2O2混合液”的仪器名称______________________________。
(2)写出反应生成CaO2·8H2O的化学方程式___________________________________。
(3)抽滤后得到的晶体依次使用蒸馏水、乙醇洗涤,使用乙醇洗涤的目的是_________________________。
(4)用图②装置抽滤时,使用抽气泵抽真空前,应先关闭活塞____(填“a”或“b”)。
(5)反应温度以0~5℃为宜的原因____________________________。
II.产品中CaO2含量的测定
准确称取0.15g无水过氧化钙样品于锥形瓶中,加入50mL水和15mL2mol/LHCl,振荡使之溶解,立即用0.02mol/L的KMnO4溶液滴定至溶液呈微红色且半分钟内不褪色为止,重复实验3次,平均消耗20.00mL.KMnO4溶液。
(1)产品中CaO2的质量分数为_______________________________。
(2)若滴定后仰视读数,则测得样品中CaO2的含量___________(填“偏高”“偏低”或“不变”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)在配合物Fe(SCN)2+中提供空轨道接受孤电子对的微粒是____(填符号),配合物离子[Cu(NH3)4]2+为平面正方形结构, 画出其中的配位键_____________。
(2)配合物Co[(N3)(NH3)5]SO4中Co3+的配位数为___,Co3+与NH3之间的作用属于_____(选填“离子键”、“配位键”、“范德华力”、“氢键”)。
(3)Co(Ⅲ)的八面体配合物CoClm·nNH3,若1 mol配合物与AgNO3作用生成1 molAgCl沉淀,则m=__________, n= ___________。(填具体数值)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】具有抗菌作用的白头翁素衍生物H的合成路线如图所示
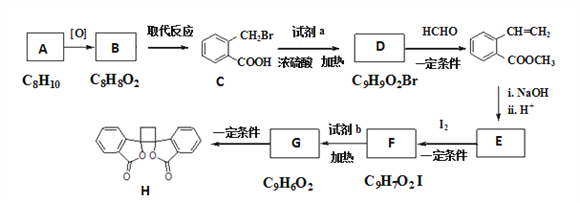
已知: ①RCH2Br ![]() R﹣HC═CH﹣R′
R﹣HC═CH﹣R′
②R﹣HC═CH﹣R′![]()
![]()
③R﹣HC═CH﹣R′![]()
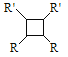 (以上R、R'、R'代表氢、烷基或芳基等)
(以上R、R'、R'代表氢、烷基或芳基等)
(1)A属于芳香烃,其名称是____;C中官能团的名称是____;由G生成H的反应类型为____;
(2)试剂a的结构简式是____,试剂b为____;由C生成D的化学方程式是____。
(3)下列说法正确的是____
A.E中含有3种官能团 B.1mol H与足量NaOH溶液反应,消耗2mol NaOH
C.由F生成G的反应是消去反应 D.1mol G最多可以与3mol H2发生加成反应
(4)与化合物C具有相同官能团且属于芳香族化合物的同分异构体共有____ 种(包括C本身)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,将浓度均为0.1mol·L-1,体积分别为Va和Vb的HA溶液与BOH溶液按不同体积比混合,保持Va+Vb=100mL,Va、Vb与混合液pH的关系如图所示,下列说法正确的是
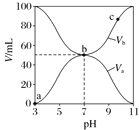
A. Ka(HA)=1×10-6
B. b点时,c(B+)=c(A-)
C. c点时,![]() 随温度升高而增大
随温度升高而增大
D. a→c过程中水的电离程度始终增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com