
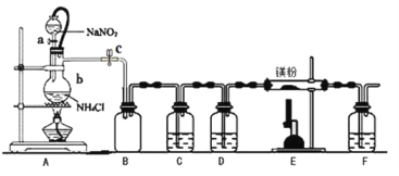
【题目】氮化镁(Mg3N2)在工业上具有非常广泛的应用。某化学兴趣小组用镁与氮气反应制备 Mg3N2 并进行有关实验。实验装置如下所示: (部分加热装置已略去)
已知:①氮化镁常温下为浅黄色粉末,极易与水反应。
②亚硝酸钠和氯化铵制取氮气的反应剧烈放热,产生氮气的速度较快。
③温度较高时,亚硝酸钠会分解产生O2等。
回答下列问题:
(1)仪器 b 的名称是__________,写出装置 A 中发生反应的化学方程式___________。
(2)某同学检验装置 A 部分的气密性,关闭止水夹 c 后,开启活塞 a,水不断往下滴,直至全部流入烧瓶。试判断:
A 部分装置是否漏气? ________ (填“漏气”、“不漏气”或“无法确定”),判断理由是____________。
(3)装置 C 中为饱和硫酸亚铁溶液, 其作用是___________,装置 F 的作用是________。
(4)加热至反应开始发生,需移走 A 处酒精灯,原因是__________________。
(5)定性分析产物
操作步骤 | 实验现象 | 解释原因 |
取少量产品于试管中, 加适量蒸馏水 | 试管底部有固体不溶物,有剌激性气味的气体产生 | 反应的化学方程式为 __________________________________ |
弃去上层淸液, 加入足量稀盐酸 | 观察到固体全部溶解, 且有气泡冒出 | 气泡冒出的原因为___________________________________________________ |
【答案】 蒸馏烧瓶 NH4Cl+NaNO2![]() N2 ↑+NaCl+2H2O 无法确定 由于分液漏斗和烧瓶间有橡皮管相连,使分液漏斗中液面上方和烧瓶中液面上方的压强相同,无论装置是否漏气,都不影响分液漏斗中的液体滴入烧瓶 除去氧气以免与镁反应 防止空气中的水蒸气进入E装置使氮化镁水解 该反应剧烈放热,产生氮气的速度快,移走A处酒精灯能避免反应物冲出,同时避免温度过高,造成NaNO2分解产生O2 Mg3N2+6H2O=3Mg(OH)2 +2NH3 未反应的镁与盐酸反应产生氢气
N2 ↑+NaCl+2H2O 无法确定 由于分液漏斗和烧瓶间有橡皮管相连,使分液漏斗中液面上方和烧瓶中液面上方的压强相同,无论装置是否漏气,都不影响分液漏斗中的液体滴入烧瓶 除去氧气以免与镁反应 防止空气中的水蒸气进入E装置使氮化镁水解 该反应剧烈放热,产生氮气的速度快,移走A处酒精灯能避免反应物冲出,同时避免温度过高,造成NaNO2分解产生O2 Mg3N2+6H2O=3Mg(OH)2 +2NH3 未反应的镁与盐酸反应产生氢气
【解析】(1)仪器 b 的名称是蒸馏烧瓶,因带有支管;A装置中发生反应的化学方程式为NH4Cl+ NaNO2 ![]() N2↑+NaCl+2H2O
N2↑+NaCl+2H2O
(2)由于分液漏斗和蒸馏烧瓶间有橡皮管相连,使分液漏斗中液面上方和烧瓶中液面上方的压强相同,无论装置是否漏气,都不影响分液漏斗中的液体流入烧瓶中,所以无法确定装置A是否漏气;
(3)当加热温度过高时,导致NaNO2分解产生氧气,会影响氮气与镁的反应,所以装置C中饱和硫酸亚铁溶液的作用是除去可能产生的氧气,防止氧气与镁反应;由于氮化镁极易与水反应,所以装置F的作用是防止空气中的水蒸气进入装置E中使氮化镁水解;
(4)因为亚硝酸钠和氯化铵的反应剧烈放热,产生氮气的速率快,所以加热至反应开始发生,即移走A处酒精灯,避免反应物冲出,使N2气流保持平稳,同时也避免温度过高,造成NaNO2分解产生O2;
(5)Mg3N2极易与水反应,反应的化学方程式为Mg3N2+6H2O=3Mg(OH)2+2NH3;产品加水反应后的固体中含有Mg(OH)2,可能有未反应的镁,所以加入盐酸后二者都能反应,且镁与盐酸反应能产生氢气。


科目:高中化学 来源: 题型:
【题目】aLCO2气体通过足量Na2O2后,所得气体再与bLNO混合时,可得到cL气体(气体体积均在相同状况下测定),下列表达式中,错误的是( )
A. 若a则c<![]() (a+b) B. 若a则c>
(a+b) B. 若a则c>![]() (a+b)
(a+b)
C. 若a>b则c=![]() (a+b) D. 若a=b则c=
(a+b) D. 若a=b则c=![]() (a+b)
(a+b)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以反应 5H2C2O4+2MnO4 -+6H+ = 10CO2↑+ 2Mn2+ + 8H2O 为例探究“外界条件对化学反应速率的影响”。实验时,分别量取 H2C2O4 溶液和酸性 KMnO4溶液,迅速混合并开始计时,通过测定溶液褪色所需时间来判断反应的快慢。
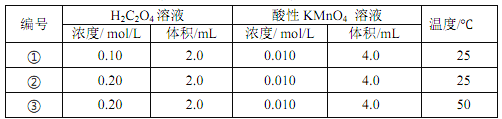
下列说法不正确的是
A. 实验①、 ②、 ③所加的H2C2O4 溶液均要过量
B. 若实验①测得 KMnO4溶液的褪色时间为 40 s, 则这段时间内平均反应速率 v(KMnO4)= 2. 5×10-4 mol/L/s
C. 实验①和实验②是探究浓度对化学反应速率的影响, 实验②和③是探究温度对化学反应速率的影响
D. 实验①和②起初反应均很慢,过了一会儿速率突然增大,可能是生成的 Mn2+对反应起催化作用
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于金属腐蚀,下列说法正确的是
A. 金属的化学腐蚀比电化学腐蚀更普遍
B. 析氢腐蚀比吸氧腐蚀更普遍
C. 析氢腐蚀后阶段会发生吸氧腐蚀
D. 牺牲阳极的阴极保护法是利用了电解原理
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用18.4mol/L的浓H2SO4配制100mL浓度为1.0mol/L的稀H2SO4,其操作可分为以下各步:
(1)A.用量简量取_____浓H2SO4缓缓注入装有约50mL蒸馏水的烧杯中,并用玻璃棒搅拌;
B.用约30mL蒸馏水,分成3次洗涤烧杯和玻棒,将每次洗涤液都注人容量瓶中;
C.将稀释后的H2SO4小心转移到100mL容量瓶里;
D.检查100mL容量瓶口部是否会发生滴漏;
E.加蒸馏水至容量瓶中液面接近刻度2cm处;
F.盖紧瓶塞,反复颠倒振荡,摇匀溶液;
G.用胶头滴管向容量瓶里逐滴滴加蒸馏水至液面最低点和刻度线相平。
(2)上述操作正确的顺序为(用字母填写)__________。
(3)进行A步操作时,应选择下列量器_______(填序号)。
a.10mL量筒 b.50mL量筒 c.100mL量筒
(4)如果对装有浓H2SO4的量筒读数如右图所示,配制的稀H2SO4的浓度将_______(偏高、偏低、无影响)。
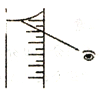
(5)进入A步操作后,必须________后才能进行C操作。
查看答案和解析>>
科目:高中化学 来源: 题型:
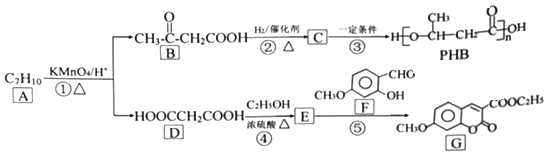
【题目】[化学选修5:有机化学基础]由化合物A 制备一种医药合成中间体G和可降解环保塑料PHB的合成路线如下:
己知: ![]() (-R1、-R2、-R3 均为烃基)
(-R1、-R2、-R3 均为烃基)
回答下列问题:
(1)A的结构简式____________________,G中含氧官能团的名称____________________。
(2)反应③和④的反应类型分别是_____________________、____________________________。
(3)F的分子式为________________________。
(4)E是二元酯,其名称是__________________,反应④的化学方程式____________________。(5) C 存在多种同分异构体,其中分别与足量的NaHCO3溶液和Na反应产生气体的物质的量相同的同分异构体的数目为______种。
(6)写出用B为起始原料制备高分子化合物![]() 的合成路线(其他试剂任选)。
的合成路线(其他试剂任选)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com