
【题目】用18.4mol/L的浓H2SO4配制100mL浓度为1.0mol/L的稀H2SO4,其操作可分为以下各步:
(1)A.用量简量取_____浓H2SO4缓缓注入装有约50mL蒸馏水的烧杯中,并用玻璃棒搅拌;
B.用约30mL蒸馏水,分成3次洗涤烧杯和玻棒,将每次洗涤液都注人容量瓶中;
C.将稀释后的H2SO4小心转移到100mL容量瓶里;
D.检查100mL容量瓶口部是否会发生滴漏;
E.加蒸馏水至容量瓶中液面接近刻度2cm处;
F.盖紧瓶塞,反复颠倒振荡,摇匀溶液;
G.用胶头滴管向容量瓶里逐滴滴加蒸馏水至液面最低点和刻度线相平。
(2)上述操作正确的顺序为(用字母填写)__________。
(3)进行A步操作时,应选择下列量器_______(填序号)。
a.10mL量筒 b.50mL量筒 c.100mL量筒
(4)如果对装有浓H2SO4的量筒读数如右图所示,配制的稀H2SO4的浓度将_______(偏高、偏低、无影响)。
(5)进入A步操作后,必须________后才能进行C操作。
【答案】5.4mL DACBEGF a 偏高 冷却至室温
【解析】
(1).设需要量取xmL的浓硫酸,根据稀释定律,x×10-3L×18.4mol/L=0.1L×1.0mol/L,解得x=5.4mL,故答案为:5.4mL;
(2).用浓溶液配制一定物质的量浓度的稀溶液,一般操作步骤为:计算、量取、稀释、冷却、移液、洗涤、定容、摇匀、装瓶等,所以正确的顺序为:DACBEGF,故答案为:DACBEGF;
(3).依据量筒选择原则可知量取5.4mL溶液,应选择10mL量筒,故答案为:a;
(4).仰视量筒读数,会导致量取的浓硫酸体积偏大,硫酸的物质的量偏大,配制的溶液浓度偏高,故答案为:偏高;
(5).容量瓶为精密仪器,不能用来配制过热或过冷的液体,所以移液前应冷却至室温,故答案为:冷却至室温。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】下列叙述不正确的是( )
A.有机物C2H6与C3H8一定是同系物B.可以用溴水鉴别甲烷和乙烯
C.用分液漏斗分离乙酸和乙醇D.蔗糖和麦芽糖互称为同分异构体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮化镁(Mg3N2)在工业上具有非常广泛的应用。某化学兴趣小组用镁与氮气反应制备 Mg3N2 并进行有关实验。实验装置如下所示: (部分加热装置已略去)
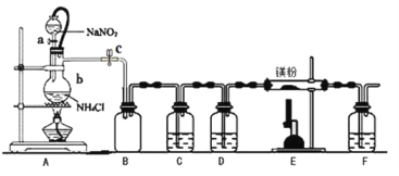
已知:①氮化镁常温下为浅黄色粉末,极易与水反应。
②亚硝酸钠和氯化铵制取氮气的反应剧烈放热,产生氮气的速度较快。
③温度较高时,亚硝酸钠会分解产生O2等。
回答下列问题:
(1)仪器 b 的名称是__________,写出装置 A 中发生反应的化学方程式___________。
(2)某同学检验装置 A 部分的气密性,关闭止水夹 c 后,开启活塞 a,水不断往下滴,直至全部流入烧瓶。试判断:
A 部分装置是否漏气? ________ (填“漏气”、“不漏气”或“无法确定”),判断理由是____________。
(3)装置 C 中为饱和硫酸亚铁溶液, 其作用是___________,装置 F 的作用是________。
(4)加热至反应开始发生,需移走 A 处酒精灯,原因是__________________。
(5)定性分析产物
操作步骤 | 实验现象 | 解释原因 |
取少量产品于试管中, 加适量蒸馏水 | 试管底部有固体不溶物,有剌激性气味的气体产生 | 反应的化学方程式为 __________________________________ |
弃去上层淸液, 加入足量稀盐酸 | 观察到固体全部溶解, 且有气泡冒出 | 气泡冒出的原因为___________________________________________________ |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图中的每一方框内表示一种反应物或生成物,其中A、C、D、E、F在通常情况下均为气体,且A与C物质的量之比为1:1,B为常见液体。
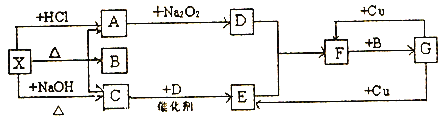
试回答下列问题:
(1)X是_____;F是____。(写化学式)
(2)写出C→E反应的化学方程式并用双线桥标出电子转移的方向和数目__________。
(3)G与Cu的反应中,G表现_______性质。
(4)写出X→A的离子方程式:__________。
(5)以C、B、D为原料可生产G,若使amolC的中心原子完全转化到G中,理论上至少需要D___mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,将一定量的A、B气体充入密闭容器,发生反应:A(g)+B(g)![]() xC(?)+3D(?)。反应平衡后,改变影响平衡的一个条件,物质A的浓度变化如下图所示。下列有关说法正确的是
xC(?)+3D(?)。反应平衡后,改变影响平衡的一个条件,物质A的浓度变化如下图所示。下列有关说法正确的是
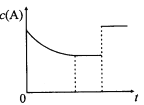
A.x=2,C为气态,D可能为气态也可能为非气态
B.改变的条件可能是使用了催化剂
C.其他条件不变,若向容器中加入少量C,A的平衡转化率不变
D.该反应的化学平衡常数K=[c(C)]2/c(A) ·c(B),且温度升高,K值增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】生活在某些山区的人,由于饮用的水和食物中缺碘,导致某些人患病,该病的主要症状是
A. 身体消瘦 B. 食欲旺盛 C. 血糖浓度升高 D. 甲状腺增生肿大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列变化属于放热反应的是
①液态水汽化 ②将胆矾加热变为白色粉末 ③浓硫酸稀释
④氯酸钾分解制氧气 ⑤生石灰跟水反应生成熟石灰
A.①④B.⑤C.①④⑤D.②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮可以形成多种离子,如N3-,NH2-,N3-,NH4+,N2H5+,N2H62+等,已知N2H5+与N2H62+是由中性分子结合质子形成的,类似于NH4+,因此有类似于 NH4+的性质。
(1)N2H62+在碱性溶液中反应的离子方程式:_____________________________________。
(2)NH2-的电子式为__________________________,NH2-的构型为____________。
(3)写出一种与N3-是等电子体的微粒化学式___________。
(4)据报道,美国科学家卡尔·克里斯特于1998年11月合成了一种名为“N5”的物质,由于其具有极强的爆炸性,又称为 “盐粒炸弹”。迄今为止,人们对它的结构尚不清楚,只知道“N5”实际上是带正电荷的分子碎片,其结构是对称的,5个N排成V形。如果5个N结合后都达到8电子结构,且含有2个N![]() N键。则“N5”分子碎片所带电荷是_______。
N键。则“N5”分子碎片所带电荷是_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】具有抗菌作用的白头翁素衍生物H的合成路线如图所示
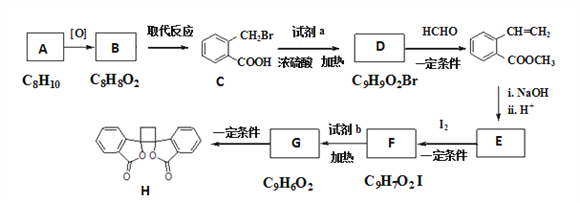
已知: ①RCH2Br ![]() R﹣HC═CH﹣R′
R﹣HC═CH﹣R′
②R﹣HC═CH﹣R′![]()
![]()
③R﹣HC═CH﹣R′![]()
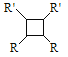 (以上R、R'、R'代表氢、烷基或芳基等)
(以上R、R'、R'代表氢、烷基或芳基等)
(1)A属于芳香烃,其名称是____;C中官能团的名称是____;由G生成H的反应类型为____;
(2)试剂a的结构简式是____,试剂b为____;由C生成D的化学方程式是____。
(3)下列说法正确的是____
A.E中含有3种官能团 B.1mol H与足量NaOH溶液反应,消耗2mol NaOH
C.由F生成G的反应是消去反应 D.1mol G最多可以与3mol H2发生加成反应
(4)与化合物C具有相同官能团且属于芳香族化合物的同分异构体共有____ 种(包括C本身)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com