
| A. | 氯化铜溶液中加入氢氧化铁 | B. | 硝酸铝溶液中加入氨水 | ||
| C. | 氢氧化钾溶液中加入硫化铜 | D. | 碳酸氨中加入氢氧化钾 |
科目:高中化学 来源: 题型:选择题
| A. | ①②③ | B. | ①②④ | C. | ②③④ | D. | ③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ③⑤ | C. | ④⑤ | D. | ①②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 植物的光合作用使得太阳能转化为了化学能 | |
| B. | 电解水生成氢气和氧气时,电能转化为化学能 | |
| C. | 生物体内的化学变化过程在能量转化上比在体外发生的一些能量转化更为合理有效 | |
| D. | 白炽灯工作时将电能全部转化为光能 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
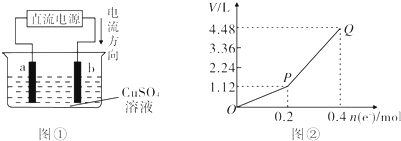
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaCl NaBr | B. | NaCl NaBr Na2SO4 | ||
| C. | NaCl | D. | Na2SO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ;NH4+的空间构型是正四面体.
;NH4+的空间构型是正四面体.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com