
����Ŀ��C��N��O��Al��Si��Cu�dz���������Ԫ�أ�
��1��Siλ��Ԫ�����ڱ������ڵ��壮
��2��Nԭ�ӵ�ԭ�ӽṹʾ��ͼΪ��Cu�ĵͼ����������ɫΪ ��
��3���á�����������գ�
ԭ�Ӱ뾶 | �縺�� | �۵� | �е� |
AlSi | NO | ���ʯ����� | CH4SiH4 |
��4�������£�����ȥ��������Ĥ��Al��CuƬ����ŨHNO3�����ԭ��أ�ͼ1�������ԭ��صĵ���ǿ�ȣ�I����ʱ�䣨t���ı仯��ͼ2��ʾ����Ӧ�������к���ɫ��������� 
0��t1ʱ��ԭ��صĸ�����AlƬ����ʱ�������ĵ缫��Ӧʽ�� �� ��Һ�е�H+�����ƶ���t1ʱ��ԭ����е��������������ı䣬��ԭ���� ��
���𰸡�
��1������IVA
��2��![]() ��ש��ɫ
��ש��ɫ
��3����������������
��4��2H++NO3��+e��=NO2��+H2O����������Ũ�����з����ۻ�������Ĥ��ֹ��Al��һ��������Ӧ��Al��������������Ũ�Ƚ�Ϊһ��Ũ��ʱ��Ϊϡ���ᣬAl��ʼ�����������������������ı�
���������⣺��1��Siԭ�Ӻ�����3�����Ӳ㡢����������Ϊ4������λ�ڵ������ڵ�IVA�壬�ʴ�Ϊ��������A����2��Nԭ�ӽṹʾ��ͼΪ ![]() ��������ͭΪש��ɫ���ʴ�Ϊ��
��������ͭΪש��ɫ���ʴ�Ϊ�� ![]() ��ש��ɫ����3��ͬһ����Ԫ��ԭ�Ӱ뾶����ԭ�������������С������ԭ�Ӱ뾶Al��Si��
��ש��ɫ����3��ͬһ����Ԫ��ԭ�Ӱ뾶����ԭ�������������С������ԭ�Ӱ뾶Al��Si��
ͬһ����Ԫ�ص縺������ԭ������������������Ե縺��N��O��ԭ�Ӿ����۷е���ԭ�Ӱ뾶�ɷ��ȣ�ԭ�Ӱ뾶C��Si�������۷е���ʯ������裻��������ķ��Ӿ����۷е�����Է������������ȣ���Է����������飼���飬�����۷е���飼���飻
ԭ�Ӱ뾶 | �縺�� | �۵� | �е� |
Al��Si | N��O | ���ʯ������� | CH4��SiH4 |
4����ԭ����У�Al�����ۻ�����Cu��ʧ���Ӷ���������Al��������������ӦʽΪ2H++NO3��+e��=NO2��+H2O����Һ���������������ƶ��������������������ƶ�����Ũ����Ũ�Ƚ��͵�һ���̶��DZ�Ϊϡ���ᣬAl��ʧ���Ӷ������������Ե��������������ı䣬�ʴ�Ϊ��2H++NO3��+e��=NO2��+H2O����������Ũ�����з����ۻ�������Ĥ��ֹ��Al��һ��������Ӧ��Al��������������Ũ�Ƚ�Ϊһ��Ũ��ʱ��Ϊϡ���ᣬAl��ʼ�����������������������ı䣮
��1������Ԫ��ԭ�Ӻ�����Ӳ���������������ȣ�����������������������ȣ���2��Nԭ�Ӻ�����7�����ӡ�������7�����ӡ��������Ӳ㣻������ͭΪש��ɫ����3��ͬһ����Ԫ��ԭ�Ӱ뾶����ԭ�������������С��ͬһ����Ԫ�ص縺������ԭ���������������ԭ�Ӿ����۷е���ԭ�Ӱ뾶�ɷ��ȣ���������ķ��Ӿ����۷е�����Է������������ȣ���4����ԭ����У�Cu��������Al����������������������ӵõ������ɶ����������������Һ���������������ƶ������������ƶ�����Ũ����Ũ�Ƚ��͵�һ���̶��DZ�Ϊϡ���ᣬAl��ʧ���Ӷ���������


 �����Ծ���Ԫ���Ծ�ϵ�д�
�����Ծ���Ԫ���Ծ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������һ���Լ��ɽ����Ȼ�̼�������ױ�������ɫҺ�����������������Լ��ǣ� ��
A.����
B.ˮ
C.��ˮ
D.���Ը��������Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ʵ������ƽ���ƶ�ԭ�����͵��ǣ�������
A. ����ơ������ĭ�ݳ�
B. ˫��ˮ�м�������������ݲ������ʼӿ�
C. �ϳɰ���ѹ������������
D. װ��NO2����ƿ������ˮ����ɫ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��A����ʹ��ˮ��ɫ��0.5 mol A��ȫȼ��ʱ���õ�1.5 mol H2O��67.2 L CO2(��״��)��
��1��ͨ������ȷ��A�Ľṹ��ʽΪ__________________��
��2��д��A��Ũ�����Ũ����Ļ������ˮԡ���������·�Ӧ����C�Ļ�ѧ����ʽ��_______________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����
A.���ȷ�Ӧ����Ҫ���ȾͿ��Է���
B.��ѧ��Ӧ��һ�������������ı仯
C.�ɱ����������մ������ȣ�����仯�����ȷ�Ӧ
D.���ȷ�Ӧ�У���������е�������С�ڷ�Ӧ����е�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������������ǵĽ���ϢϢ��أ�Ŀ�ҹ�ͨ�����6����Ⱦ�������Ũ���������������ָ����AQI����SO2��NO2����CO������3���е���Ⱦ�
��1������3������ֱ������������������������������ѧʽ����
��2�����������г�����NaClO2��Һ��Ϊ���ռ�����ͬʱ����������������������������ӦClO2��+2SO32��2SO42��+Cl�� �� �÷�Ӧ��ƽ�ⳣ��K�ı���ʽΪ��
��3�����÷�Ӧ6NO2+8NH3�T7N2+12H2O���ɵ�صķ���������ʵ����Ч��������������ŷţ����ỷ����Ⱦ�����ܳ�����û�ѧ�ܣ�װ����ͼ��ʾ��д���缫A�ĵ缫����ʽ �� ���������4.48L������ʱ��ͨ���缫B�ĵ�����Ϊ 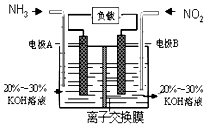
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵������ȷ����
A. ������Һ�ܹ�����
B. ˮ�����ڵ���
C. CuSO4��5H2O�ǻ�����
D. ����������˪����������������˪�����γ�������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ƹ�ҵ�����������������ж���ˮ�����뾭���ϸ�����ſ����ŷţ�ij�ֺ�A���ӣ������ӣ���ˮ���ŷ�ǰ�Ĵ����������£�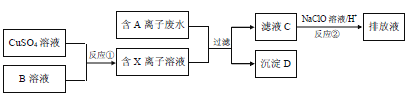
��֪��9.0g����D�����������պ���8.0g��ɫ���壬���ɵ�����ͨ����������ʯ��ˮʱ������10.0g��ɫ���������õ��Ļ�������ȥ������ʣ�������ܶ�Ϊ1.25gL��1������E 1.12L��
��1��E�Ľṹʽ
��2������D�Ļ�ѧʽ
��3��д������D�����������շ����Ļ�ѧ����ʽ
��4����ҺC�л���������A���ӣ�ͨ����Ӧ�ڣ��ɽ���ת��Ϊ�Ի����������ʣ��������ӷ���ʽ��ʾ��ԭ��
��5����Ӧ��Ϊ�Ƶ�ij��Ԫ�صĵͼ�X���ӣ��Դ�������ԭ��Ӧ�ĽǶȷ������Ƿ������Na2SO3��Һ������B��Һ��˵������ �������ʵ�鷽��֤��Na2SO3��Һ�Ƿ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ͼ��Ӳ���Թ�A�з������ྻ��ϸͭ˿���ձ��з�����ˮ���Թ�B�з���״����ҷ��Թ�C�з�����ˮ����B�в��Ϲ��������ʹ�״������Ϳ���ͨ�����ȵ����ȳ̶ȵ�ͭ˿�� 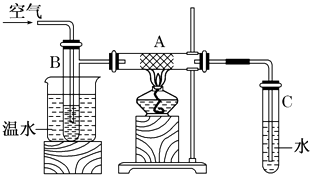
��1����ȥA���ƾ��ƺ�ͭ˿��Ȼ�ܱ��ֺ��ȵ�ԭ������
��2����Ӧ���Թ�C�е�Һ����ȴ��ȡ�����������뵽���Ƶ�Cu��OH��2����Һ�У����ȵ����ڿɹ۲쵽������ �� д����Ӧ�Ļ�ѧ����ʽ ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com