
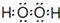 ,
,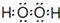 ;
;

 桃李文化快乐暑假武汉出版社系列答案
桃李文化快乐暑假武汉出版社系列答案 优秀生快乐假期每一天全新寒假作业本系列答案
优秀生快乐假期每一天全新寒假作业本系列答案 暑假接力赛新疆青少年出版社系列答案
暑假接力赛新疆青少年出版社系列答案科目:高中化学 来源: 题型:

| A、最早使用的化学电池是锌锰电池,它是一次性电池 |
| B、电池使用过程中,锌会逐渐溶解:Zn=Zn2++2e- |
| C、锌锰电池即使不用,放置过久,也会失效 |
| D、锌锰干电池内的电解质NH4Cl可以换成HCl溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:



查看答案和解析>>
科目:高中化学 来源: 题型:
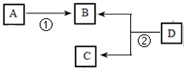 气态烃A是一种基本的有机化工原料,目前石油裂解已成为生成A的主要方法.A在标准状况下的密度为1.25g?L-1.D的分子式为C4H8O2,D在酸性条件下水解得到B和C,C的相对分子质量比B大14.四种有机物之间存在如下转化关系:
气态烃A是一种基本的有机化工原料,目前石油裂解已成为生成A的主要方法.A在标准状况下的密度为1.25g?L-1.D的分子式为C4H8O2,D在酸性条件下水解得到B和C,C的相对分子质量比B大14.四种有机物之间存在如下转化关系:查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| Na | Mg | Al | Si | P | S | Cl | Ar |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
A、 测定NaOH溶液的浓度 测定NaOH溶液的浓度 |
B、 碳酸氢钠受热分解 碳酸氢钠受热分解 |
C、 蒸干NH4Cl饱和溶液制备NH4Cl晶体 蒸干NH4Cl饱和溶液制备NH4Cl晶体 |
D、 关闭分液漏斗,向外拉动针筒活塞,松开后活塞恢复原处,证明装置气密性良好 关闭分液漏斗,向外拉动针筒活塞,松开后活塞恢复原处,证明装置气密性良好 |
查看答案和解析>>
科目:高中化学 来源: 题型:
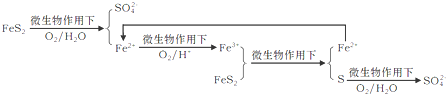
| O2/H+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com