
【题目】下列说法正确的是( )
A. ![]() 的名称为3-甲基丁烷
的名称为3-甲基丁烷
B. CH3CH2CH2CH2CH3和 ![]() 互为同素异形体
互为同素异形体
C. CH3CH2OH和 ![]() 具有相同的官能团,互为同系物
具有相同的官能团,互为同系物
D.  和
和  为同一物质
为同一物质
 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案科目:高中化学 来源: 题型:
【题目】一种新型乙醇电池用磺酸类质子作溶剂,比甲醇电池效率高出32倍。电池总反应为:C2H5OH +3O2= 2CO2 +3H2O,电池示意图如下图。下面对这种电池的说法正确的是:
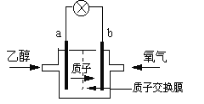
A. 标准状况下,通入5.6LO2并完全反应后,有0.5mol电子转移
B. 电池工作时电子由b极沿导线经灯泡再到a极
C. 电池正极的电极反应为:4H+ +O2 +4e- =2H2O
D. b极为电池的负极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯乙烷(![]() -C2H5)可生产塑料单体苯乙烯(
-C2H5)可生产塑料单体苯乙烯(![]() -CH=CH2),其原理反应是:
-CH=CH2),其原理反应是:![]() -C2H5(g)
-C2H5(g) ![]()
![]() -CH=CH2(g) + H2(g);△H = +125 kJ·mol-1。某温度下,将0.40 mol
-CH=CH2(g) + H2(g);△H = +125 kJ·mol-1。某温度下,将0.40 mol![]() -C2H5(g)充入2L真空密闭容器中发生反应,测定该容器内的物质,得到数据如下表:
-C2H5(g)充入2L真空密闭容器中发生反应,测定该容器内的物质,得到数据如下表:
时间/min | 0 | 10 | 20 | 30 | 40 |
n( | 0.40 | 0.30 | 0.26 | n2 | n3 |
n( | 0.00 | 0.10 | n1 | 0.16 | 0.16 |
(1)n1=__________mol,计算该反应的平衡常数,K=___________。
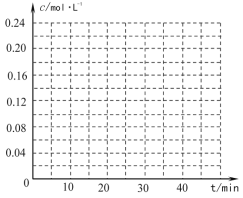
(2)工业上常以高温水蒸气作为反应体系的稀释剂(不参与反应)。![]() -C2H5(g)的平衡转化率与水蒸气的用量、体系总压强的关系如图所示。当其它条件不变时,水蒸气的用量越大,平衡转化率将_________(填“越大”、“越小”或“不变”),原因是____________。
-C2H5(g)的平衡转化率与水蒸气的用量、体系总压强的关系如图所示。当其它条件不变时,水蒸气的用量越大,平衡转化率将_________(填“越大”、“越小”或“不变”),原因是____________。

(3)副产物H2用做氢氧燃料电池。写出酸性条件下,该电池正极的电极反应式__________。
(4)在相同条件下,若最初向该容器中充入![]() -CH=CH2(g)和H2(g),假设在40min时达到上述同样的平衡状态,请在图中画出并标明该条件下
-CH=CH2(g)和H2(g),假设在40min时达到上述同样的平衡状态,请在图中画出并标明该条件下![]() -C2H5(g)和
-C2H5(g)和![]() -CH=CH2(g)的浓度c随时间t变化的曲线_____。
-CH=CH2(g)的浓度c随时间t变化的曲线_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生探究0.25mol/L Al2( SO4)3溶液与0.5mol/L Na2CO3溶液的反应,实验如下:

下列分析不正确的是
A. 实验I中,白色沉淀a是Al(OH)3
B. 实验2中,白色沉淀b含有CO32-
C. 实验l、2中,白色沉淀成分不同的原因与混合后溶液的pH无关
D. 检验白色沉淀a、b足否洗涤干净,均可用盐酸酸化的BaCl2溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从煤和石油中可以提炼出化工原料A和B,A是一种果实催熟剂,它的产量用来衡量一个国家的石油化工发展水平.B是一种比水轻的油状液体,B仅由碳氢两种元素组成,碳元素与氢元素的质量比为12:1,B的相对分子质量为78.回答下列问题:
(1)A的电子式 ______________ ,A的结构简式 _______________ .
(2)与A相邻的同系物C使溴的四氯化碳溶液褪色的化学反应方程式 ______________________,反应类型_______________。
(3)在碘水中加入B振荡静置后的现象_________________________
(4)B与浓H2SO4与浓HNO3在50-60℃反应的化学反应方程式 ________________________,反应类型______________________。
(5)等质量的A、B完全燃烧时消耗O2的物质的量______(填“A>B”或“A<B”或“A=B”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】MnSO4是制备高纯MnCO3的中间原料。实验室用如图所示装置可制备少量MnSO4溶液,反应原理为:MnO2+H2SO3=MnSO4+H2O;下列说法错误的是( )
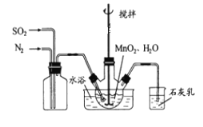
A. 缓慢通入混合气体可提高SO2的转化率
B. 若不通N2,则烧瓶中的进气管口容易被堵塞
C. 若实验中将N2换成空气,则反应液中c(Mn2+)/c(SO42-)的浓度之比变大
D. 石灰乳对尾气的吸收效果比澄清石灰水更好
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组为探究草酸亚铁(FeC2O4)的热分解产物,按下面所示装置进行实验。以下说法错误的是
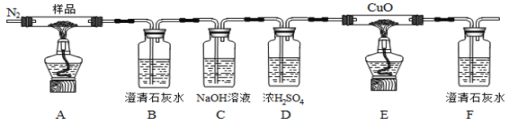
A. 实验中观察到装置B、F中石灰水变浑浊,E中固体变为红色,则证明分解产物中有CO2和CO气体
B. 反应结束后,取A中固体溶于稀硫酸,向其中滴加1~2滴KSCN溶液,溶液无颜色变化,证明分解产物中不含Fe2O3
C. 装置C的作用是除去混合气中的CO2
D. 反应结束后,应熄灭A、E处酒精灯后,持续通入N2直至温度恢复至室温
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业合成氨的反应如下:3H2+N2![]() 2NH3。某温度下,在容积恒定为2.0 L的密闭容器中充入2.0 mol N2和2.0 mol H2,一段时间后反应达平衡状态,实验数据如下表所示:
2NH3。某温度下,在容积恒定为2.0 L的密闭容器中充入2.0 mol N2和2.0 mol H2,一段时间后反应达平衡状态,实验数据如下表所示:
t/s | 0 | 50 | 150 | 250 | 350 |
n(NH3)/mol | 0 | 0.24 | 0.36 | 0.40 | 0.40 |
(1)0~50 s内的平均反应速率 v(N2)=_______________。
(2)250 s时,H2的转化率为________。
(3)已知N≡N的键能为946 kJ·mol-1,H-H的键能为436 kJ·mol-1,N-H的键能为391 kJ·mol-1,则生成1 mol NH3过程中的热量变化为_______kJ。下图能正确表示该反应中能量变化的是_____(填字母)。
A.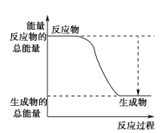 B.
B.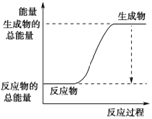
(4)为加快反应速率,可以采取的措施__________。
a.降低温度;b.增大压强;c.恒容时充入He气;d.恒压时充入He气;e.及时分离出NH3
(5)下列可判断反应已达到平衡状态的是__________。
A 气体的平均摩尔质量不变
B N2、H2的反应速率比为1:3
C 混合气体的密度不变
D 生成1mol N2的同时生成2mol NH3
E N2、H2、NH3物质的量之比等于系数比
F 混合气体的总压强不再发生改变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,可逆反应2A(g)+3B(s)![]() 2C(g)达到平衡的标志是( )
2C(g)达到平衡的标志是( )
A. A、B、C的浓度相等
B. 气体平均摩尔质量不随时间改变而改变
C. A、B、C的分子数比为1∶3∶2
D. 气体的总物质的量不随时间改变而改变
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com