
【题目】一种新型乙醇电池用磺酸类质子作溶剂,比甲醇电池效率高出32倍。电池总反应为:C2H5OH +3O2= 2CO2 +3H2O,电池示意图如下图。下面对这种电池的说法正确的是:
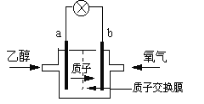
A. 标准状况下,通入5.6LO2并完全反应后,有0.5mol电子转移
B. 电池工作时电子由b极沿导线经灯泡再到a极
C. 电池正极的电极反应为:4H+ +O2 +4e- =2H2O
D. b极为电池的负极
科目:高中化学 来源: 题型:
【题目】如图所示是一种酸性燃料电池酒精检测仪,具有自动吹气流量侦测与控制的功能,非常适合进行现场酒精检测。下列说法不正确的是

A. 电流由O2所在的铂电极经外电路流向另一电极
B. O2所在的铂电极处发生还原反应
C. 该电池的负极反应式为:CH3CH2OH+3H2O-12e-="=" 2CO2↑+12H+
D. 微处理器通过检测电流大小而计算出被测气体中酒精的含量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一个密闭容器中发生如下反应:2SO2(g)+O2(g)![]() 2SO3(g),反应过程中某一时刻测得SO2、O2、SO3的浓度分别为0.2mol·L-1,0.2 mol·L-1,0.2 mol·L-1,当反应达到平衡时,可能出现的数据是( )
2SO3(g),反应过程中某一时刻测得SO2、O2、SO3的浓度分别为0.2mol·L-1,0.2 mol·L-1,0.2 mol·L-1,当反应达到平衡时,可能出现的数据是( )
A. c(SO3)=0.4 mol·L-1B. c(SO2)=c(SO3)=0.15 mol·L-1
C. c(O2)=0.1 mol·L-1D. c(SO2)+c(SO3)=0.4 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA表示阿伏加得德罗常数的数值,下列叙述中正确的是
A. 1mol NH3所含有的原子数为NA
B. 常温常压下,22.4L氧气所含的原子数为2NA
C. 常温常压下,48g O3所含的氧原子数为3NA
D. 1 L 0.1mol/LNaCl溶液中所含的Na+为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值。下列叙述不正确的是:
A. 2.7 g 金属铝分别与足量的NaOH溶液和盐酸反应转移的电子数目均为0.3NA
B. 标准状况下,2.24 L Cl2与过量NaOH溶液反应,转移的电子总数为0.1 NA
C. 1L 1 molL-1 Na2CO3溶液中阴离子数小于NA
D. 2.3 g金属钠完全反应生成Na2O与Na2O2的混合物中阴离子数为0.05 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上采用乙烯和水蒸气在催化剂(磷酸/硅藻土)表面合成乙醇,反应原理为CH2===CH2(g)+H2O(g) ![]() CH3CH2OH(g),副产物有乙醛、乙醚及乙烯的聚合物等。下图是乙烯的总转化率随温度、压强的变化关系,下列说法正确的是:
CH3CH2OH(g),副产物有乙醛、乙醚及乙烯的聚合物等。下图是乙烯的总转化率随温度、压强的变化关系,下列说法正确的是:
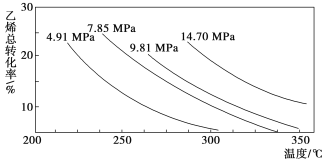
A. 合成乙醇的反应一定为吸热反应
B. 目前工业上采用250~300 ℃,主要是因为在此温度下乙烯的转化率最大
C. 目前工业上采用加压条件(7 MPa左右),目的是提高乙醇的产率和加快反应速率
D. 相同催化剂下,在300 ℃ 14.70 MPa乙醇产率反而比300 ℃ 7.85 MPa低得多,是因为加压平衡向逆反应方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设![]() 为阿伏加德罗常数值。下列有关叙述正确的是
为阿伏加德罗常数值。下列有关叙述正确的是
A. 1mol![]() 与4mol
与4mol![]() 反应生成的
反应生成的![]() 分子数为
分子数为![]()
B. 1molFe溶于过量硝酸,电子转移数为![]()
C. 14g乙烯和丙烯混合气体中的氢原子数为![]()
D. 标准状况下,2.24L![]() 含有的共价键数为0.4
含有的共价键数为0.4![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. ![]() 的名称为3-甲基丁烷
的名称为3-甲基丁烷
B. CH3CH2CH2CH2CH3和 ![]() 互为同素异形体
互为同素异形体
C. CH3CH2OH和 ![]() 具有相同的官能团,互为同系物
具有相同的官能团,互为同系物
D.  和
和  为同一物质
为同一物质
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com