
����Ŀ��ͭ������Ҫ��п��ͭ��������(Cd)����(Co)�ȵ��ʡ�ʪ����п������ͭ�����������������ӵĹ����������£�

�±��г�����ؽ������������������������pH(�������ӵ���ʼŨ��Ϊ0.1mol��L-1)
�������� | Fe(OH)3 | Fe(OH)2 | Cd(OH)2 |
��ʼ������pH | 1.5 | 6.5 | 7.2 |
������ȫ��pH | 3.3 | 9.9 | 9.5 |
(1)���ʱ����ͭ������Ŀ����_______________________��
(2)�����������������Ҫ�ɷ�Ϊ___________________(�ѧʽ)��
(3)�ٲ��������ȼ�������H2O2��������Ӧ�����ӷ���ʽΪ____________________��
���ټ���ZnO���Ʒ�ӦҺ��pH��pH��ΧΪ______________���ж�������_______________��
���������H2O2���㣬����ZnO�����õĵ��Һ�лẬ��FeԪ�ء�
�����ʵ�鷽�����Լ���___________________________��
(4)�������ӷ�ˮ���ü���̼���ʵ�ֳ���ת�����ó���ת���ķ�Ӧ����ʽΪ____________����ȥ��ҵ��ˮ�е�Cd2+ʱ������Ӧ�ﵽƽ�����Һ��c(Ca2+)=0.1mol��L-1����Һ��c(Cd2+)=_____mol��L-1 (��֪25�� ��Ksp(CdCO3)=5.6��10-12, Ksp(CaCO3)=5.6��10-9)��
���𰸡� ��������ĽӴ�������ӿ췴Ӧ���ʣ����ԭ�ϵĽ����� Cu 2Fe2++H2O2+2H+=2Fe3++2H2O 3.3��pH��7.2 ���ݱ����е���Ϣ��֪��3.3��pH<7.2ʱ����ȷ��Fe3+������ȫ����Cd2+������� ȡ�����Һ�������Թ��У������еμ�H2O2���ڵ���KSCN��Һ������Һ��죨�������еμ�K3[Fe(CN)6]��Һ��������ɫ��������������Һ�к���FeԪ�� CaCO3(s)+Cd2+(aq)![]() CdCO3(s)+Ca2+(aq) 1.0��10-4
CdCO3(s)+Ca2+(aq) 1.0��10-4
��������(1)���ʱ����ͭ������Ŀ������������ĽӴ�������ӿ췴Ӧ���ʣ����ԭ�ϵĽ����ʡ�(2)ͭ��ϡ�����Ӧ��������������������Ҫ�ɷ�ΪCu��(3)��˫��ˮ���������ԣ��ܰ�������������Ϊ�����ӣ�������Ӧ�����ӷ���ʽΪ2Fe2++H2O2+2H+��2Fe3++2H2O���ڸ��ݱ����е���Ϣ��֪��3.3��pH��7.2ʱ����ȷ��Fe3+������ȫ����Cd2+������������pH��ΧΪ3.3��pH��7.2�����������˫��ˮ���㣬��������Һ�����������Ӳ��࣬�����������Ӽ��ɣ�����Ϊ��ȡ�����Һ�������Թ��У������еμ�H2O2���ڵ���KSCN��Һ������Һ��죨�������еμ�K3[Fe(CN)6]��Һ��������ɫ��������������Һ�к���FeԪ�أ�(4)�����ܶȻ�������С��֪KspԽС���ܽ��ԽС������Խ��ȫ����˴������ӷ�ˮ���ü���̼���ʵ�ֳ���ת�����ó���ת���ķ�Ӧ����ʽΪCaCO3(s)+Cd2+(aq)![]() CdCO3(s)+Ca2+(aq)����ȥ��ҵ��ˮ�е�Cd2+ʱ������Ӧ�ﵽƽ�����Һ��c(Ca2+)��0.1mol��L-1�������̼��Ƶ��ܶȻ�������֪��Һ��̼���Ũ����5.6��10-8mol/L����˸���Ksp(CdCO3)��5.6��10-12��֪c(Cd2+)��1.0��10-4mol��L-1��
CdCO3(s)+Ca2+(aq)����ȥ��ҵ��ˮ�е�Cd2+ʱ������Ӧ�ﵽƽ�����Һ��c(Ca2+)��0.1mol��L-1�������̼��Ƶ��ܶȻ�������֪��Һ��̼���Ũ����5.6��10-8mol/L����˸���Ksp(CdCO3)��5.6��10-12��֪c(Cd2+)��1.0��10-4mol��L-1��


 ���Ǽ���С����ϵ�д�
���Ǽ���С����ϵ�д� �Ͻ�ƽ���Ȿϵ�д�
�Ͻ�ƽ���Ȿϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����в�����Ϊ��ˮ������������
A.����B.��������C.���ӽ�����D.���˷�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������98%��Ũ���ᣨ�ܶ�Ϊ1.84g��cm��3)����Ũ��Ϊ1mol��L��1��ϡ����480mL��
��1����������Ʒ�� ѡ��ʵ������Ҫ������________________����д��ţ�
A��1000mL�ձ� B��100mL�ձ� C��10mL��Ͳ D��50mL��Ͳ
E��500mL����ƿ F��1000mL����ƿ G�����ƿ H��������ƽ
��2����ѡ�����������⣬��ȱ�ٵı�Ҫ��������Ʒ��_______________________
��3����ȡ��Ũ��������Ϊ________mL (�������һλС��)
��4������ʱ��һ��ɷ�Ϊ���¼������裬�������к�����д��ȱ��������ƣ�
���㡢�������ܽ⡢��ȴ��ת�ơ�ϴ�ӡ�ת�ơ�_______��ҡ�ȡ�
��5����������У���ʹ������Һ��Ũ��ƫ�͵���________
A������Ͳ�е�Ũ����ת���ձ�����ˮϴ����Ͳ����ϴҺҲת�����ձ���
B��ϡ��Ũ���������ת������ƿ
C������ʱ��ˮ���������̶���
D������ʱ���ӿ̶���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£���20.00mL0.1000molL��1�İ�ˮ����μ���0.1000molL��1�����ᣬpH����������ı仯��ͼ��ʾ��������NH3���ݳ���������˵������ȷ���ǣ�������

A. ��Ӧ�����У�c��NH4+��+c��H+��=c��OH����+c��Cl����
B. V��HCl��=10.00mLʱ��c��NH4+����c��Cl������c��NH3H2O��
C. V��HCl����20.00mLʱ����Һһ���ʼ���
D. V��HCl��=30.00mLʱ��2c��Cl����=3c��NH4+��+3c��NH3H2O��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NAΪ�����ӵ�������ֵ������˵����ȷ����
A. 1molCl2����ˮ����Һ��Cl2��HClO��ClO-��Cl-������������Ϊ2NA
B. 6.4gCu������Ũ���ᷴӦ����NO2������ĿΪNA
C. 1mol����(C6H10O5)nˮ�������������Ƿ�����ĿΪNA
D. ��״���£�2molNa2O2��44.8LSO2��ȫ��Ӧ��ת�Ƶĵ�����ĿΪ4NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Ƭ��ϡ���ᷴӦ������ʱ�����д�ʩ����ʹ��Ӧ���ʼӿ���� ( )
A.����ϡ���ᣬ����98%��Ũ����B.����
C.�μ�����CuSO4��ҺD.������Ƭ����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1��Ԫ�����ڱ���һ���֣�

25��ʱ����Ũ��Ϊ0.1000 molL-1������������Һ�ֱ�ζ�20.00mLŨ�Ⱦ�Ϊ0.1000 molL-1��������HX��HZ����������仯����ʵ���������2�������ж���ȷ����
A. ͨ�������ɵñ�����a <7��b=7
B. ��������HZ��Һϡ��100����pH��HX��Һ��pH��
C. ����ZԪ�صķǽ����Ա�Yǿ������Z�⻯������Խ�ǿ
D. 0.1000 molL-1 Na2Y��ˮ��Һ�У�c(Y2��) + c(HY��) + c(H2Y) �� 0.1000 molL-1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ���õ�ⷨ�����������Է�ˮ���õ���������ԭ����ͼ��ʾ������˵���������
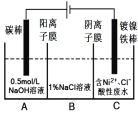
��֪����Ni2+����������Һ�з���ˮ�⣻
�������ԣ�Ni2+����Ũ�ȣ���H+��Ni2+����Ũ�ȣ�
A. ̼���Ϸ����ĵ缫��Ӧ��4OH4e= O2��+2H2O
B. Ϊ��������IJ��ʣ�����������Ҫ���Ʒ�ˮ��pH
C. �������У�B��NaCl��Һ�����ʵ���Ũ�Ƚ����ϼ���
D. ����ͼ��������Ĥȥ������A��B���Һϲ������ⷴӦ�ܷ���ʽ�����ı�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��Һ��ֻ����Ba2+ Mg2+ Ag+���������ӣ�����������NaOH��Һ��ϡ�����Na2SO4��Һ��������������һ�������룬��������ͼ��ʾ��
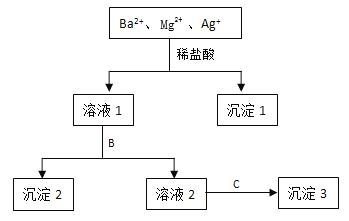
��1������1�Ļ�ѧʽΪ �����ɸó��������ӷ���ʽΪ ��
��2�����Լ�BΪNa2SO4��Һ�������2��ѧʽΪ ��
��3�����Լ�BΪNaOH��Һ�������ɳ���2�����ӷ���ʽΪ ��
��4�����ԭ��Һ��Ba2+ Mg2+ Ag+��Ũ�Ⱦ�Ϊ0.1 mol��L-1������Һ�к��е�������ֻ��NO3-������Һ��NO3- Ũ��Ϊ mol��L-1��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com