
【题目】将浓盐酸滴入高锰酸钾溶液中,产生黄绿色气体,而溶液的紫红色褪去。现有一氧化还原反应的体系,共有KCl、Cl2、浓H2SO4、H2O、KMnO4、MnSO4、K2SO4七种物质。
请完成下列填空:
(1)写出一个包含上述体系中七种物质的氧化还原反应方程式(无需配平):_________________________;上述反应中,还原产物是_____________,每转移1 mol电子,生成Cl2 _____ L(标准状况)。
(2)上述反应体系中,有些短周期元素的简单离子核外电子排布相同,它们的简单离子半径由大到小的顺序为______________(用离子符号表达)。
(3)氯原子的最外层电子排布式为_____________________,氯原子核外共有____种不同运动状态的电子。
(4)在上述反应后的溶液中加入NaBiO3(不溶于冷水),溶液又变为紫红色,BiO3-反应后变为无色的Bi3+。比较该反应中的氧化剂和氧化产物的氧化性强弱_______>________。
(5)请用原子结构理论解释上述含7种物质的氧化还原反应体系中,属于同一主族两种元素非金属性的强弱,____>______;______________________________________________________。
【答案】 2KMnO4+10KCl+8H2SO4=6K2SO4+ 2MnSO4+5Cl2↑+8H2O(无需配平) MnSO4 11.2L S2- > Cl- 3S23P5 17 BiO3— MnO4- O S 氧原子与硫原子最外层均有6个电子,前者只有两层,后者有三层电子,氧原子半径小于硫原子,氧原子得电子能力强于硫原子,所以,氧元素的非金属性强于硫元素的非金属性。
【解析】试题分析:本题主要通过浓盐酸与高锰酸钾溶液氧化还原反应的讨论,考查氧化还原反应的配平、电子转移计算、离子半径比较方法、氧化性强弱比较方法、非金属性强弱比较方法、核外电子排布等基础知识,考查考生运用化学知识解决实际问题的能力。
解析:(1)根据题干的提示,KMnO4+HCl→MnCl2+Cl2↑,本小题中HCl的成分可由KCl及H2SO4提供,配平后的总反应包含题中7中物质,既2KMnO4+10KCl+8H2SO4=6K2SO4+ 2MnSO4+5Cl2↑+8H2O,该反应中还原产物为MnSO4,生成1molCl2时转移电子数为2mol,因此每转移1mol电子生成Cl20.5mol,标准状况下体积为11.2L。正确答案:2KMnO4+10KCl+8H2SO4![]() 6K2SO4+ 2MnSO4+5Cl2↑+8H2O(无需配平)、MnSO4、11.2L。(2)上述反应体系中,短周期元素的简单离子包括O2-、Cl-、H+、S2-,其中电子排布相同的是Cl-和S2-,离子半径S2->Cl-。正确答案:S2->Cl-。(3)Cl是17号元素,核外电子排布式为1s22s22p63s23p5,最外层电子排布式为3s23p5,原子核外共有17种运动状态不同的电子。正确答案:3S23P5、17。(4)NaBiO3中Bi元素为+5价,反应生成Bi3+说明NaBiO3被还原,“溶液又变为紫红色”说明原溶液中Mn2+被氧化生成MnO4-,所以氧化剂和氧化产物的氧化性强弱为BiO3- >MnO4-。正确答案:BiO3- 、MnO4-。(5)上述(1)的反应体系中,属于同一主族的两种元素为O和S。氧原子与硫原子最外层均有6个电子,前者含有两个电子层,后者有三个电子层,氧原子半径小于硫原子,氧原子得电子能力强于硫原子,所以,氧元素的非金属性强于硫元素的非金属性。正确答案:O;S;氧原子与硫原子最外层均有6个电子,前者只有两层,后者有三层电子,氧原子半径小于硫原子,氧原子得电子能力强于硫原子,所以,氧元素的非金属性强于硫元素的非金属性。
6K2SO4+ 2MnSO4+5Cl2↑+8H2O(无需配平)、MnSO4、11.2L。(2)上述反应体系中,短周期元素的简单离子包括O2-、Cl-、H+、S2-,其中电子排布相同的是Cl-和S2-,离子半径S2->Cl-。正确答案:S2->Cl-。(3)Cl是17号元素,核外电子排布式为1s22s22p63s23p5,最外层电子排布式为3s23p5,原子核外共有17种运动状态不同的电子。正确答案:3S23P5、17。(4)NaBiO3中Bi元素为+5价,反应生成Bi3+说明NaBiO3被还原,“溶液又变为紫红色”说明原溶液中Mn2+被氧化生成MnO4-,所以氧化剂和氧化产物的氧化性强弱为BiO3- >MnO4-。正确答案:BiO3- 、MnO4-。(5)上述(1)的反应体系中,属于同一主族的两种元素为O和S。氧原子与硫原子最外层均有6个电子,前者含有两个电子层,后者有三个电子层,氧原子半径小于硫原子,氧原子得电子能力强于硫原子,所以,氧元素的非金属性强于硫元素的非金属性。正确答案:O;S;氧原子与硫原子最外层均有6个电子,前者只有两层,后者有三层电子,氧原子半径小于硫原子,氧原子得电子能力强于硫原子,所以,氧元素的非金属性强于硫元素的非金属性。


 期末1卷素质教育评估卷系列答案
期末1卷素质教育评估卷系列答案科目:高中化学 来源: 题型:
【题目】下列根据各概念图作出的判断,不正确的是
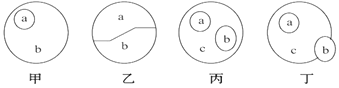
A. 甲图中a和b可以表示核糖和单糖的关系
B. 若乙中a和b分别代表DNA和RNA,则乙图可以代表原核细胞内的核酸
C. 丙图中a、b、c可分別表示磷脂、固醇和脂质之间的关系
D. 丁图a、b、c可分别表示激素、酶和蛋白质之间的关系
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由CH3CH2CH2Br制备CH3CH(OH)CH2OH,依次发生的反应类型和反应条件都正确的是
选项 | 反应类型 | 反应条件 |
A | 加成、取代、消去 | KOH醇溶液/加热、KOH水溶液/加热、常温 |
B | 消去、加成、取代 | NaOH醇溶液/加热、常温、KOH水溶液/加热 |
C | 氧化、取代、消去 | 加热、KOH醇溶液/加热、KOH水溶液/加热 |
D | 消去、加成、水解 | NaOH水溶液/加热、常温、NaOH醇溶液/加热 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关分子结构 ![]() 的下列叙述中,正确的是
的下列叙述中,正确的是
A.可能在同一平面上的原子最多有20个
B.12个碳原子不可能都在同一平面上
C.所有的原子都在同一平面上
D.除苯环外的其余碳原子有可能都在一条直线上
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A.所有的原子核内都有质子和中子
B.(H+)实质上是一个裸露的质子
C.核外电子排布相同的微粒,其化学性质也相同
D.非金属元素原子最外层电子数都大于4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物H是一种香料,存在于金橘中,可用如下路线合成:
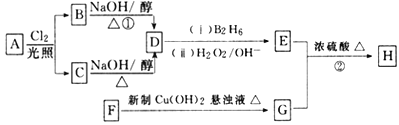
已知:R-CH=CH2![]() RCH2CH2OH (B2H6为乙硼烷)。
RCH2CH2OH (B2H6为乙硼烷)。
回答下列问题:
(1)11.2L(标准状况)的烃A在氧气中充分燃烧可以产生88gCO2和45gH2O。A的分子式是___________;
(2)B和C均为一氯代烃,它们的名称(系统命名)分别为___________________;
(3)在催化剂存在下1molF与2molH2反应,生成3-苯基-1-丙醇。F的结构简式是__________________;
(4)反应①的反应类型是____________________;
(5)反应②的化学方程式为______________________________________________;
(6)写出所有与G具有相同官能团的G的芳香类同分异构体的结构简式_________________________________。(写任何一种)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】北京航空航天大学教授偶然中发现米虫吃塑料,受此启发进行了系列实验,证实黄粉虫的肠道微生物可降解聚苯乙烯(PS),蜡虫可降解聚乙烯(PE)。聚苯乙烯在虫肠内降解的示意图如下,下列说法正确的是
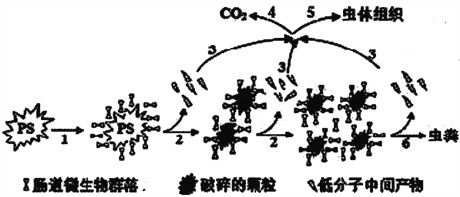
A. 在虫肠内微生物作用下,聚苯乙烯断裂碳碳双键
B. 在虫肠内微生物作用下,聚苯乙烯直接降解为CO2分子
C. 在虫肠内微生物作用下,聚苯乙烯发生降解,分子量降低
D. 聚乙烯与聚苯乙烯是同系物,具有烯烃的性质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,Na2CO3溶液存在水解平衡:CO![]() +H2O
+H2O![]() HCO
HCO![]() +OH-。下列说法正确的是( )
+OH-。下列说法正确的是( )
A. 稀释溶液,水解平衡常数增大
B. 加入少量NH4Cl固体,平衡朝正反应方向移动
C. 升高温度,![]() 减小
减小
D. 加入NaOH固体,溶液pH减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 铜在自然界中主要以单质的形式存在
B. 工业上常用电解饱和食盐水的方法制备金属钠
C. 工业上常用焦炭在高温下直接将氧化铁还原炼铁
D. 在海水中加入石灰乳可得氢氧化镁沉淀,这是从海水中富集镁的基本方法
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com