
| 实验步骤 | 实验现象及相关结论 | |
| ① | 取少量电解质溶液于试管中,用pH试纸测其pH, | 试纸呈深蓝色,经比对溶液的pH约为14,说明溶液中有残余的KOH. |
| ② | 继续加入 |
若有白色沉淀产生,则溶液中含有K2SO4. 若无白色沉淀产生,则溶液中没有K2SO4. |
| ③ | 另取少量电解质溶液于试管中,先加 1mol?L-1的H2SO4酸化,再滴入2~3滴0.01mol?L-1KMnO4酸性溶液,振荡. |
| 11.65g |
| 233g/mol |
| 20.00 |
| 100.00 |
| 56g |
| 56g/mol |
| 0.1000mol |
| 0.02000L |


科目:高中化学 来源: 题型:
| A、采取“静电除尘”、“燃煤固硫”、“汽车尾气催化净化”等方法,可提高空气质量 |
| B、采用天然石材装修家居,可减轻室内甲醛污染但会导致一定量的放射性物质的污染 |
| C、汽油中添加含铅化合物Pb(C2H5)4,可提高汽油的抗爆震性能,有利于改善大气环境 |
| D、PM2.5表示每立方米空气中直径小于或等于2.5微米的颗粒物的含量,PM2.5值越高,大气污染越严重 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 绿矾 |
| H+ |
| 石灰水 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 催化剂 |
| △ |
| 实验序号 | 时间浓度温度 | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
| 1 | 800℃ | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 | 0.50 |
| 2 | 800℃ | C2 | 0.92 | 0.75 | 0.63 | 0.60 | 0.60 | 0.60 |
| 3 | 820℃ | 1.0 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 | 0.20 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| 检测次数 | 溶液中检测出的物质 |
| 第一次 | KCl、K2SO4、Na2CO3、NaCl |
| 第二次 | KCl、BaCl2、Na2SO4、K2CO3 |
| 第三次 | Na2SO4、KCl、K2CO3、NaCl |
查看答案和解析>>
科目:高中化学 来源: 题型:
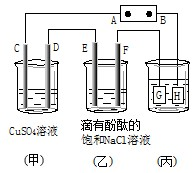 如图装置所示,C、D、E、F都是惰性电极,
如图装置所示,C、D、E、F都是惰性电极,查看答案和解析>>
科目:高中化学 来源: 题型:
 一种新型酸性乙醇电池用磺酸类质子作溶剂,比甲醇电池效率高出32倍,电池反应式为C2H5OH+3O2=2CO2+3H2O,电池构造如图.下列关于该电池的说法不正确的是
一种新型酸性乙醇电池用磺酸类质子作溶剂,比甲醇电池效率高出32倍,电池反应式为C2H5OH+3O2=2CO2+3H2O,电池构造如图.下列关于该电池的说法不正确的是| A、放电过程中,电源内部的H+从正极区向负极区迁移 |
| B、通入乙醇的电极是负极 |
| C、该电池的正极反应为:4H++O2+4e-=2H2O |
| D、用该电池做为电源,用惰性电极电解饱和NaCl的水溶液时,每消耗0.2 mol C2H5OH,阳极产生标准状况下气体的体积为26.88 L |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、标准状况下,22.4L正丁烷和异丁烷的混合物中所含共用电子对数为14NA | ||
| B、常温常压下,15.0g甲醛与葡萄糖的混合物中含有氢原子的数目为NA | ||
| C、60g SiO2晶体所含Si-O键的数目为2NA,78 g苯含有C=C双键的数目为3NA | ||
D、将CO2通过Na2O2使其增重a g时,反应中转移电子数为
|
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com