
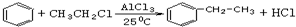
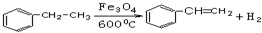 ;试以乙烯、苯、食盐、水等为原料制备苯乙醇 (
;试以乙烯、苯、食盐、水等为原料制备苯乙醇 (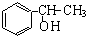 ),写出各步反应的化学方程式:
),写出各步反应的化学方程式: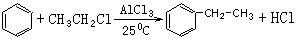 ;
;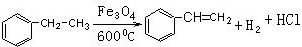 ;
;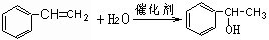 .
. 分析 以乙烯、苯、食盐、水等为原料通过6个反应可制备图4,由逆合成法可知,生成图4物质,需要苯乙烯与水加成,苯乙烷发生图2中反应生成苯乙烯,苯与氯乙烷发生取代反应生成苯乙烷,乙烯与HCl发生加成反应生成氯乙烷,然后由电解食盐水生成氢气、氯气、氢气与氯气反应生成HCl,以此来解答.
解答 解:以乙烯、苯、食盐、水等为原料通过6个反应可制备图4,由逆合成法可知,生成图4物质,需要苯乙烯与水加成,苯乙烷发生图2中反应生成苯乙烯,苯与氯乙烷发生取代反应生成苯乙烷,乙烯与HCl发生加成反应生成氯乙烷,然后由电解食盐水生成氢气、氯气、氢气与氯气反应生成HCl,则发生的6步反应为:
(1)2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+H2↑+Cl2↑,
(2)H2 +Cl2$\frac{\underline{\;点燃\;}}{\;}$2HCl;
(3)CH2=CH2 +HCl→CH3CH2Cl;
(4)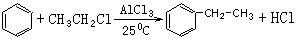 ,
,
(5)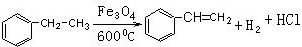 ,
,
(6)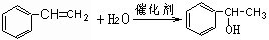 ,
,
故答案为:2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+H2↑+Cl2↑;H2 +Cl2$\frac{\underline{\;点燃\;}}{\;}$2HCl;CH2=CH2 +HCl→CH3CH2Cl;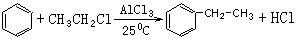 ;
;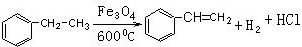 ;
;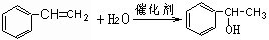 .
.
点评 本题考查有机物的合成,为高频考点,把握有机合成的逆合成法及习题中的信息为解答的关键,注意合成反应中官能团的变化及性质,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | KCl溶液和CH3COONH4溶液均显中性,两溶液中水的电离程度相同 | |
| B. | 向氟化钠溶液中加入适量氢氟酸,得到的酸性混合溶液:c(Na+)>c(F-)>c(H+)>c(OH-) | |
| C. | 25℃时,等体积pH=3的HA和HB两种酸分别与足量的锌反应,相同时间内HA与Zn反应生成的氢气更多,HA是弱酸 | |
| D. | Na2CO3溶液中加入少量Ca(OH)2固体,CO32-水解程度减小,溶液的pH减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3COOH+CH3CH2OH$?_{△}^{浓H_{2}SO_{4}}$CH3COOCH2CH3+H2O | |
| B. | 2CH3CH2OH+O2$→_{△}^{催化剂}$2CH3CHO+2H2O | |
| C. | CH3CH2Br+NaOH$\stackrel{H_{2}O}{→}$CH3CH2OH+NaBr | |
| D. | 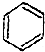 +Br2$\stackrel{FeBr_{3}}{→}$ +Br2$\stackrel{FeBr_{3}}{→}$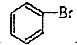 +HBr +HBr |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
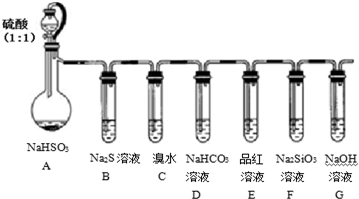
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用蒸馏法分离碘和酒精 | |
| B. | 稀硝酸除去混在铜粉中的少量镁粉和铝粉 | |
| C. | 用溶解,过滤的方法分离硝酸钾和氯化钠固体的混合物 | |
| D. | 用饱和氯化铁溶液滴入煮沸的氢氧化钠溶液中的方法制备氢氧化铁胶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
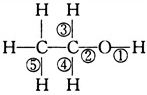 ,关于乙醇在各种不同反应中断键的说法正确的是( )
,关于乙醇在各种不同反应中断键的说法正确的是( )| A. | 和金属钠反应键②断裂 | |
| B. | 在Cu催化下和O2反应键①④断裂 | |
| C. | 和浓硫酸共热140℃时,键①或键②断裂,170℃时键②⑤断裂 | |
| D. | 和氢溴酸反应键①断裂 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com