
下列溶液中各微粒的浓度关系正确的是
A.pH=4的盐酸中:c(H+)=4.0mol·L-1
B.NH4Cl溶液中:c(Cl-)=c(NH4+)
C.NaCl溶液中:c(Na+) + c(H+)= c(Cl-)+c(OH-)
D.NaHCO3溶液中:c(HCO3-)+c(H2CO3)+ c(CO32-) =c(Na+)
 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案科目:高中化学 来源: 题型:
.A、B、C、D、E代表5种元素。请填空:
(1)A元素基态原子的最外层有3个未成对电子,次外层有2个电子,其元素符号为 ;
(2)B元素的负一价离子和C元素的正一价离子的电子层结构都与氩相同,B的元素符号为 ,C的元素符号为 ;
(3)D元素的正三价离子的3d亚层为半充满,D的元素符号为 ,其基态原子的电子排布式为 。
(4)E元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,E的元素符号为 ,其基态原子的电子排布式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
水溶液中能大量共存的一组离子是
A.Ba2+、Na+、Cl-、OH- B.Fe2+、H+、SO42-、NO3-
C.Na+、Mg2+、Cl-、CO32- D.K+、Fe3+、NO3-、SCN-
查看答案和解析>>
科目:高中化学 来源: 题型:
某密闭容器中发生如下反应:X(g)+3Y(g) 2Z(g);ΔH<0
2Z(g);ΔH<0
右图表示该反应的速率(v)随时间(t)的变化关系,t2、t3、t5时刻外界条件有所改变,但都没有改变各物质的初始加入量。下列说法中正确的是
A.t2时增大了压强
B.t3时降低了温度
C.t5时升高温度
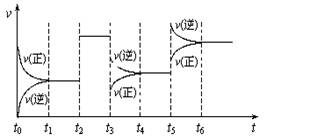 D.t6时反应物的转化率比t4时高
D.t6时反应物的转化率比t4时高
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA为阿伏伽德罗常数的数值,下列叙述正确的是
A.已知N2(g)+3H2(g) 2NH3(g) ΔH=-92.4kJ/mol,在该反
2NH3(g) ΔH=-92.4kJ/mol,在该反
应中,当有3NA电子转移时,上述热化学反应方程式的焓变变为ΔH=
46.2kJ/mol
B.1 L 0.1mol·L-1碳酸钠溶液的阴离子总数等于0.1 NA
C.室温下pH=13的NaOH溶液中含有的OH-0.1 NA
D.浓度分别为1 mol·L-1 和 0.5mol·L-1的 CH3COOH和CH3COONa 混合液共1L,含CH3COOH 和 CH3COO-共1.5 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
Zn-MnO2干电池应用广泛,其电解质溶液是ZnCl2-NH4Cl混合溶液。
 |
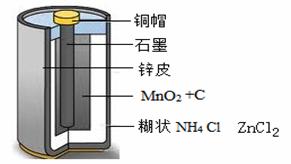
(1)该电池的负极材料是________。电池工作时,电子从Zn极流向______(填“正
极”或“负极”)。
(2)若ZnCl2-NH4Cl混合溶液中含有杂质Cu2+,会加速某电极的腐蚀,其主要原因
是 。欲除去Cu2+,最好选用下列试剂中的__________(填代号)。
A.NaOH B.Zn C.Fe D.NH3·H2O
(3)MnO2的生产方法之一是以石墨为电极,电解酸化的MnSO4溶液制取,请问MnO2
在 极产生。阴极的电极反应式是 。若电解电路中通过2 mol电子,MnO2的理论产量为__________g。(MnO2的摩尔质量为:87g/mol)
查看答案和解析>>
科目:高中化学 来源: 题型:
一定条件下硝酸铵受热分解的未配平化学方程式为NH4NO3—HNO3+N2+H2O,在反应中被氧化与被还原的氮原子数之比为
A.5∶3 B.5∶4 C.1∶1 D.3∶5
查看答案和解析>>
科目:高中化学 来源: 题型:
镁铝合金5.1 g溶于300 mL 2 mol·L-1盐酸中,标准状况下放出气体体积为5.6 L,向反应后的溶液中加入500 mL NaOH溶液充分反应,最终产生白色沉淀。下列有关说法不正确的是
A.5.1 g镁铝合金中含有镁、铝的质量分别为2.4 g、2.7 g
B.溶解5.1 g镁铝合金时,剩余盐酸的物质的量为0.1 mol
C.生成白色沉淀的最大质量为13.6 g
D.若白色沉淀只有Mg(OH)2,该NaOH溶液的物质的量浓度至少为1.2 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
下图中,a、b、c、d、e为元素周期表中前四周期的一部分元素,下列有关叙述正确的是( )
A.元素b位于ⅥA族,有+6、-2两种常见化合价
B.五种元素中,元素e的性质最稳定
C.原子半径有d>c>b
D.元素e参与形成的化合物可以作为一种半导体材料
| a | |||
| b | |||
| c | d | ||
| e |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com