
| A. | 氨气通入醋酸溶液 CH3COOH+NH3═CH3COONH4 | |
| B. | 澄清的石灰水跟盐酸反应 H++OH-═H2O | |
| C. | 碳酸钡溶于醋酸 BaCO3+2H+═Ba2++H2O+CO2↑ | |
| D. | 金属钠跟水反应 Na+H2O═Na ++OH-+H2↑ |
分析 A.醋酸铵为可溶性盐,应拆成离子形式;
B.二者反应生成氯化钙和水;
C.醋酸为弱酸应保留化学式;
D.原子个数不守恒;
解答 解:A.氨气通入醋酸溶液,离子方程式:CH3COOH+NH3═CH3COO-+NH4+,故A错误;
B.澄清的石灰水跟盐酸反应,离子方程式:H++OH-═H2O,故B正确;
C.碳酸钡溶于醋酸,离子方程式:BaCO3+2CH3COOH═Ba2++H2O+CO2↑+2CH3COO-,故C错误;
D.金属钠跟水反应,离子方程式:2Na+2H2O═2Na ++2OH-+H2↑,故D错误;
故选:B.
点评 本题考查了离子方程式的书写,明确反应实质及离子方程式书写方法是解题关键,注意化学式的拆分、电荷数、原子个数守恒,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | pH=6,显弱酸性 | B. | [H+]=10-6mo1•L-1,溶液为中性 | ||
| C. | [OH-]=10-6mo1•L-1,溶液为碱性 | D. | 温度不变稀释10倍,pH=7 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 从海水中提取溴必须通过化学反应才能实现 | |
| B. | 用侯氏制碱法制纯碱必须通过化学反应才能实现 | |
| C. | 用“地沟油”纯化生产“生物燃油”的过程发生的是化学变化 | |
| D. | 石墨在高温高压下转变为金刚石是化学变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将28.4g Na2SO4溶于水配成1000mL溶液,溶液中c (Na+)的物质的量浓度为0.2mol/L | |
| B. | 80 mL 1 mol•L-1氯化钠溶液中的c (Na+)与40 mL 1 mol•L-1碳酸钠溶液中的c (Na+) 相等 | |
| C. | 0.5 mol•L-1NaCl和0.5mol•L-1Na2SO4两溶液相比较,Na+的物质的量之比为1:2 | |
| D. | 4 mol•L-1的NaCl溶液稀释成100 mL 0.2molL-1的NaCl溶液,需4 mol•L-1的NaCl溶液的体积为5.0mL |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
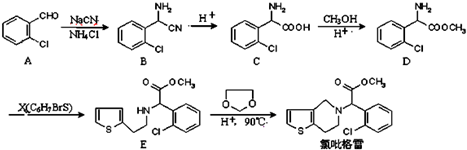
 .
. .
.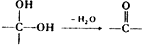 ,
,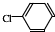 中氯原子较难水解物质A(
中氯原子较难水解物质A(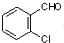 ),可由2-氯甲苯为原料制得,写出以两步制备A的化学方程式
),可由2-氯甲苯为原料制得,写出以两步制备A的化学方程式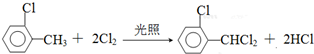 、
、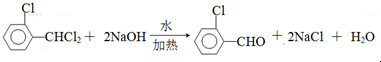 .该合成的第一步主要存在产率低的问题,请写出该步可能存在的有机物杂质的结构简式
.该合成的第一步主要存在产率低的问题,请写出该步可能存在的有机物杂质的结构简式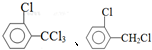 .
.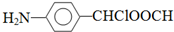 .
.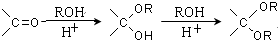 写出由乙烯、甲醇为有机原料制备化合物
写出由乙烯、甲醇为有机原料制备化合物 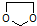 的合成路线流程图(无机试剂任选).合成路线流程图示例如下:
的合成路线流程图(无机试剂任选).合成路线流程图示例如下: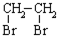
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 检验氯乙烷中的氯元素,加碱溶液加热后,用稀硫酸酸化后,再检验 | |
| B. | 为提高KMnO4溶液的氧化能力,用盐酸将KMnO4溶液酸化 | |
| C. | 抑制Fe2+的水解,用稀硝酸酸化 | |
| D. | 鉴别溶液中是否有SO42-溶液可用盐酸酸化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 一个水分子的质量为18NA g | |
| B. | 常温常压下,22.4L氯气与足量金属钠充分反应,转移的电子数为2 NA | |
| C. | 1mol•L-1 CaCl2溶液中所含Ca2+离子的数目为NA | |
| D. | 通常状况下,32g 混合气体(O2和O3 )所含的氧原子数一定为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com