
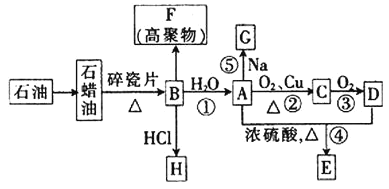
【题目】已知A是化学实验室中最常见的有机物,它易溶于水并有特殊香味;B的产量可以衡量一个国家石油化工发展的水平,有关物质的转化关系如图所示![]() 部分反应条件、产物省略
部分反应条件、产物省略![]() :
:
回答下列问题:
![]() 工业上,由石油获得石蜡油的方法称为_________,由石蜡油获得B的方法称为__________。
工业上,由石油获得石蜡油的方法称为_________,由石蜡油获得B的方法称为__________。
![]() ①决定化合物A的化学特性的原子团的名称为______________。
①决定化合物A的化学特性的原子团的名称为______________。
②![]() 到A的反应类型为_______,A到E的反应类型为____________。
到A的反应类型为_______,A到E的反应类型为____________。
③![]() 的分子式为_________;F的结构简式为___________。
的分子式为_________;F的结构简式为___________。
![]() 写出下列反应的化学方程式。
写出下列反应的化学方程式。
反应①:___________________________________________________;
反应②:___________________________________________________;
反应⑤:___________________________________________________。
【答案】石油的分馏 石油的裂解 羟基 加成反应 酯化反应 C2H4O ![]() CH2=CH2+H2O→CH3CH2OH
CH2=CH2+H2O→CH3CH2OH ![]()
![]() ;
;
【解析】
B的产量可以用来衡量一个国家的石油化工水平,则B为![]() ,石油的分馏得到石蜡油,石蜡油裂解得到乙烯,乙烯发生加聚反应生成F为
,石油的分馏得到石蜡油,石蜡油裂解得到乙烯,乙烯发生加聚反应生成F为![]() ,乙烯与水发生加成反应生成A为
,乙烯与水发生加成反应生成A为![]() ,乙醇在Cu作催化剂条件下发生氧化反应生成C为
,乙醇在Cu作催化剂条件下发生氧化反应生成C为![]() ,
,![]() 可进一步氧化生成D为
可进一步氧化生成D为![]() ,
,![]() 和
和![]() 在浓硫酸作用下反应生成乙酸乙酯,故E为
在浓硫酸作用下反应生成乙酸乙酯,故E为![]() ,乙烯与HCl发生加成反应生成H为
,乙烯与HCl发生加成反应生成H为![]() 。
。
![]() 工业上,由石油获得石蜡油的方法称为:石油的分馏,由石蜡油获得B的方法称为:石油的裂解;
工业上,由石油获得石蜡油的方法称为:石油的分馏,由石蜡油获得B的方法称为:石油的裂解;
答案为:石油的分馏;石油的裂解;
(2)①A为CH3 CH2 OH,决定化合物A的化学特性的原子团的即官能团为羟基;
答案为:羟基;
②B到A的反应为乙烯和水通过加成反应生成乙醇,A到E的反应为乙醇和乙酸生成乙酸乙酯的反应,反应类型为酯化反应;
答案为:加成反应;酯化反应;
③C为乙醛,其分子式为C2 H4O,F为聚乙烯,其结构简式为![]() ;
;
答案为:C2H4O;![]() ;
;
![]() 反应①为乙烯和水生成乙醇:CH2=CH2+H2O→CH3CH2OH;反应②为乙醇催化氧化得乙醛和水:
反应①为乙烯和水生成乙醇:CH2=CH2+H2O→CH3CH2OH;反应②为乙醇催化氧化得乙醛和水:![]() ,反应
,反应![]() 为乙醇和钠反应生成乙醇钠与氢气:
为乙醇和钠反应生成乙醇钠与氢气:![]() ;
;
答案为:CH2=CH2+H2O→![]() ;
;![]() 。
。


 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案科目:高中化学 来源: 题型:
【题目】图中装置可以用来发生、洗涤、干燥、收集(不考虑尾气处理)气体。该装置可用于 ( )

A. 锌和盐酸生成氢气
B. 二氧化锰和浓盐酸生成氯气
C. 碳酸钙和盐酸生成二氧化碳
D. 浓氨水和烧碱制取氨气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮氧化物和硫氧化物是常见的空气污染物,含氮氧化物和硫氧化物的尾气需处理后才能排放。
Ⅰ.氮氧化物的处理
(1)N2O的处理。N2O是硝酸生产中氨催化氧化的副产物,用特种催化剂能使N2O分解。NH3与O2在加热和催化剂作用下生成N2O的化学方程式为_________。
(2)NO和NO2的处理。已除去N2O的硝酸尾气可用NaOH溶液吸收,主要反应为NO+NO2+2OH=2NO2-+H2O,2NO2+2OH= NO2-+NO3-+H2O,吸收后的溶液经浓缩、结晶、过滤,得到NaNO2晶体,该晶体中的主要杂质是_________(填化学式)。
(3)NO的氧化吸收。在酸性NaClO溶液中,HClO氧化NO生成Cl和NO3-。其他条件相同,NO转化为NO3-的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如图所示。NaClO溶液的初始pH越小,NO转化率越高。其原因是_________。
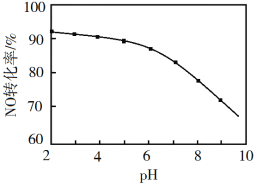
Ⅱ.煤燃烧排放的烟气中SO2和NOx的处理
采用NaClO2溶液作为吸收剂可同时对烟气进行脱硫、脱硝。在鼓泡反应器中通入含有SO2和NOx的烟气,反应温度为323K,NaClO2溶液浓度为5×103mol·L1 。反应一段时间后溶液中离子浓度的分析结果如下表。
离子 | SO42 | SO32 | NO3 | NO2 | Cl |
c/(mol·L1) | 8.35×104 | 6.87×106 | 1.5×104 | 1.2×105 | 3.4×103 |
(4)写出NaClO2溶液脱硫过程中主要反应的离子方程式________。增加压强,NO的转化率_________(填“提高”“不变”或“降低”)。
(5)由实验结果可知,脱硫反应速率大于脱硝反应速率。原因是除了SO2和NO在烟气中的初始浓度不同,还可能是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,浓度都是1mol·L-1的两种气体X2和Y2在密闭容器中反应,经过tmin后,测得物质的浓度分别为:c(X2)=0.4mol·L-1,c(Y2)=0.8mol·L-1,则该反应的方程式可表示为()
A. X2+2Y2![]() 2XY2B. 2X2+Y2
2XY2B. 2X2+Y2![]() 2X2Y
2X2Y
C. X2+3Y2![]() 2XY3D. 3X2+Y2
2XY3D. 3X2+Y2![]() 2X3Y
2X3Y
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中国古代文献中记载了大量古代化学的研究成果,《本草纲目》中记载:“(火药)乃焰消(KNO3)、硫磺、杉木炭所合,以为烽燧铳机诸药者”,反应原理为:S+2KNO3+3C=K2S+N2↑+3CO2↑。
(1)硫原子的价层电子排布图为_____,烟花燃放过程中,钾元素中的电子跃迁的方式是____,K、S、N、O四种元素第一电离能由大到小的顺序为____。上述反应涉及的元素中电负性最大的是_____(填元素符号)。
(2)碳元素除可形成常见的氧化物CO、CO2外,还可形成C2O3(结构式为![]() )。C2O3与水反应可生成草酸(HOOC—COOH)。
)。C2O3与水反应可生成草酸(HOOC—COOH)。
①C2O3中碳原子的杂化轨道类型为______,CO2分子的立体构型为_____。
②草酸与正丁酸(CH3CH2CH2COOH)的相对分子质量相差2,二者的熔点分别为101℃、-7.9℃,导致这种差异的最主要原因可能是______。
③CO分子中π键与σ键个数比为______。
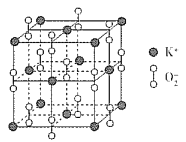
(3)超氧化钾的晶胞结构图如下,则与K+等距离且最近的O2 - 个数为_____,若晶胞参数为dpm,则该超氧化物的密度为___g·cm-3(用含d、NA的代数式表示,设NA表示阿伏加德罗常数的值)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某固体混合物中可能含有:SiO2、Na2O、CaO、CuO、Fe2O3。现将该固体进行如下实验(所加试剂均过量):
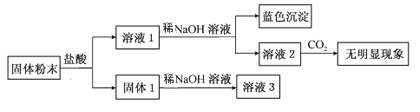
下列说法正确的是( )
A.该混合物一定含有CuO、SiO2,可能含有Na2O
B.该混合物可能含有Fe2O3
C.该混合物一定不含CaO和Na2O
D.无法确定是否含有CaO和Fe2O3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,100mL0.1mol·L-1 的H2A 溶液中滴加0.1mol·L-1NaOH溶液,含A元素相关微粒物质的量随pH的变化如图所示。下列说法正确的是
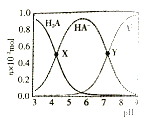
A.将等浓度等体积的Na2A与H2A溶液混合后,溶液显碱性
B.等体积等浓度的NaOH溶液与H2A溶液混合后,其溶液中水的电离程度比纯水大
C.X 点溶液中含A元素的相关离子存在以下关系:c(H2A)+c(HA-)+c(A2-)=0.1mol·L-1
D.Y点溶液中存在以下关系:c(H+) +c(Na+)=c(OH-)+3c(HA-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】物质G是制备抗癌药物吉非替尼过程中重要的中间体,某研究小组按照下列线路合成中间体G。

已知: 、
、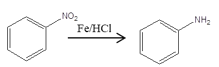 、
、 (同时还有H2O或卤化氢生成)
(同时还有H2O或卤化氢生成)
请回答:
(1)下列说法正确的是_______。
A.化合物A能够使酸性高锰酸钾溶液褪色
B.化合物A中含有4种不同的官能团
C.化合物C具有碱性
D.化合物G的分子式为C15H20N3O3
(2)上述路线中合成A的反应类型为______,化合物E的结构简式为______。
(3)写出C到D的化学反应方程式________。
(4)请设计以乙烯为原料转变为物质C的合成线路(用流程图表示,无机试剂任选)___。
(5)写出化合物B(C8H7NO2)可能的同分异构体_______。须同时满足:①能发生银镜反应;②1H—NMR谱显示分子中含有苯环,且分子中有4种不同化学环境的氢原子。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应NH4Cl+NaNO2![]() NaCl+N2↑+2H2O放热且产生气体,可用于冬天石油开采。下列表示反应中相关微粒的化学用语正确的是
NaCl+N2↑+2H2O放热且产生气体,可用于冬天石油开采。下列表示反应中相关微粒的化学用语正确的是
A. 中子数为18的氯原子:![]()
B. N2的结构式:N=N
C. Na+的结构示意图: 
D. H2O的电子式: ![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com