
| A、能生成碱的金属元素都在 IA族 |
| B、稀有气体元素原子的最外层电子数均为8 |
| C、第二周期 VIA族元素的原子核电荷数和中子数一定为8 |
| D、原子序数为14的元素位于元素周期表的第3周期ⅣA族 |


 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案科目:高中化学 来源: 题型:
| A、锌粒与稀硫酸的反应 |
| B、灼热的木炭与CO2反应 |
| C、甲烷在氧气中的燃烧反应 |
| D、Ba(OH)2?8H2O晶体与NH4Cl晶体的反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、酸性氧化物:CO2,SO2,SiO2,Cl2O7 |
| B、非电解质:乙醇、四氯化碳、氯气、葡萄糖 |
| C、同素异形体:活性炭、C60、石墨、金刚石 |
| D、混合物:铝热剂、纯净矿泉水、水玻璃、焦炉气 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 阳离子 | Na+、Ba2+、NH4+ |
| 阴离子 | CO32-、Cl-、OH-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
A、 Zn、MnO2干电池放电时MnO2被氧化 Zn、MnO2干电池放电时MnO2被氧化 |
B、 电解精炼铜时,阳极减少的质量与阴极增加的质量一定相等 电解精炼铜时,阳极减少的质量与阴极增加的质量一定相等 |
C、 K分别于M、N连接,均可保护Fe电极,且都称为“牺牲阳极的阴极保护法” K分别于M、N连接,均可保护Fe电极,且都称为“牺牲阳极的阴极保护法” |
D、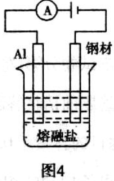 在钢材上电镀铝,熔融盐中Al和Cl元素只以AlCl4-、Al2Cl3-,形式存在,则阳极反应式为:Al-3e-+7AlCl4-=4Al2Cl3- 在钢材上电镀铝,熔融盐中Al和Cl元素只以AlCl4-、Al2Cl3-,形式存在,则阳极反应式为:Al-3e-+7AlCl4-=4Al2Cl3- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、升高温度可减小反应速率 |
| B、加入合适的催化剂可提高反应速率 |
| C、达到平衡时,v(正)=v(逆)=0 |
| D、达到平衡时,NO2转化率为100% |
查看答案和解析>>
科目:高中化学 来源: 题型:
 二氧化氯(ClO2)是目前国际上公认的第四代高效、无毒的消毒剂,是一种黄绿色的气体,易溶于水.实验室可用NH4Cl、盐酸、NaClO2(亚氯酸钠)为原料制备ClO2的流程如下:
二氧化氯(ClO2)是目前国际上公认的第四代高效、无毒的消毒剂,是一种黄绿色的气体,易溶于水.实验室可用NH4Cl、盐酸、NaClO2(亚氯酸钠)为原料制备ClO2的流程如下:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、医疗上可用硫酸钡作x射线透视肠胃的内服药,是因为硫酸钡不溶于水 |
| B、酸雨指25℃时pH值小于7的降水 |
| C、加碘食盐中添加碘酸钾而不用碘化钾,是因为碘酸钾能溶于水而碘化钾不溶于水 |
| D、发酵粉能使焙制出的糕点疏松多孔,是因为发酵粉中含有碳酸氢钠 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com