
【题目】如图是部分短周期元素化合价与原子序数的关系图,下列说法正确的是( )

A.原子半径:Z>Y>X
B.气态氢化物的热稳定性:W>R
C.WX3和水反应生成的化合物是离子化合物
D.X元素在自然界中存在同素异形现象
【答案】D
【解析】
由图中化合价可知,X的化合价为-2价,没有正化合价,故X为O元素,Y的化合价为+1价,处于IA族,原子序数大于O元素,故Y为Na元素,Z为+3价,为Al元素,W的化合价为+6、-2价,故W为S元素,R的最高正价为+7价,应为Cl元素,所以X为O, Y为Na, Z为Al, W为S,R为Cl。
A.根据分析,X为O,Y为Na, Z为Al,所以原子半径应为Na> Al>O,A错误;
B.根据分析,W为S,R为Cl,由于非金属性Cl>S,则气态氢化物的稳定性HCl>H2S,B错误;
C.根据分析,X为O,W为S,所以SO3和水反应形成的化合物是H2SO4,是共价化合物,C错误;
D.X为O,自然界中有O2和O3两种同素异形体,D正确;
答案选D


科目:高中化学 来源: 题型:
【题目】(1)下列物质N2、H2O、Na2O2、CaCl2、KOH、NaF中,既含有离了键,又含有共价键的物质是_____,属于共价化合物的是__________。
(2)用电子式表示CaCl2的形成过程:________________。
(3)氮化钠(Na3N)是科学家制备的一种重要化合物,它与水作用产生NH3。请写出NH3的电子式是____________。
(4)Na3N与盐酸反应生成两种盐,反应的化学方程式为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】资料显示:FeF3溶液接近无色。某同学据此进行以下实验,依据上述实验无法获得的结论是
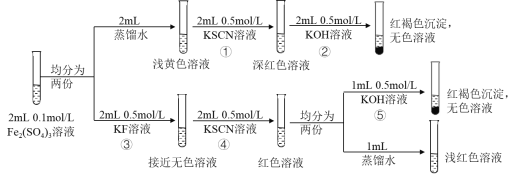
A.FeF3是弱电解质
B.④中发生的离子反应为FeF3+3SCN-Fe(SCN)3+3F-
C.相同条件下,结合Fe3+的能力:SCN->F->OH-
D.向Fe(SCN)3溶液中加入NaF固体,溶液颜色会变浅
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为原电池装置示意图:
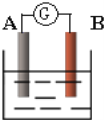
(1)若A为Zn,B为石墨棒,电解质溶液为稀硫酸,则A为_______极(填正或负),写出电极反应式:正极_______,负极_______.总反应离子方程式为:_______。
(2)若A为铜片,B为铁片,电解质为FeCl3溶液,则A为_______极(填正或负),写出电极反应式:正极_______,负极_______.总反应离子方程式为:_______。
(3)若A、B均为铂片,电解质为KOH溶液,分别从A、B两极通入H2和O2,该电池即为燃料电池,通入氧气的一极为该电池的_______极(填正或负),写出电极反应式:正极______________,负极______.总反应方程式为:______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有短周期主族元素X、Y、Z、R、T,R原子最外层电子数是电子层数的2倍;Y与Z能形成Z2Y、Z2Y2型离子化合物,Z与T形成的Z2T型化合物能破坏水的电离平衡,五种元素的原子半径与原子序数的关系如图所示。下列推断正确的是( )
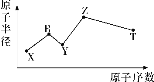
A.原子半径和离子半径均满足:Y<Z
B.简单氢化物的沸点和热稳定性均满足:Y>T
C.最高价氧化物对应的水化物的酸性:T<R
D.常温下,0.1mol·L-1由X、Y、Z、T四种元素组成的化合物的水溶液的pH一定大于1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25 ℃时,将 0.10 mol·L-1 CH3COOH 溶液滴加到 10 mL 0.10 mol·L-1 NaOH 溶液中,lg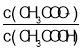 与pH 的关系如图所示,C 点坐标是(6,1.7)。下列说法不正确的是
与pH 的关系如图所示,C 点坐标是(6,1.7)。下列说法不正确的是
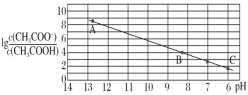
A.pH=7 时加入的醋酸溶液的体积大于 10 mL
B.C 点后继续加入醋酸溶液,水的电离程度减小
C.B 点存在 c(Na+)-c(CH3COO-)=(10-6-10-8)mol·L-1
D.Ka(CH3COOH)=10-4.3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有下列几组物质,请将序号填入下列空格内:
A C60和石墨 B 126C和136C C 冰醋酸和乙酸 D CH3CHO与![]() E 甲烷和十二烷 F 乙醇和乙二醇
E 甲烷和十二烷 F 乙醇和乙二醇
①互为同位素的是_________;
②互为同系物的是___________;
③互为同分异构体的是________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸铜是一种常见的化工产品,它在纺织、印染、医药、化工、电镀以及木材和纸张的防腐等方面有极其广泛的用途。实验室制备硫酸铜的步骤如下:
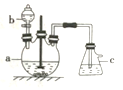
①在仪器a中先加入20g铜片、60 mL水,再缓缓加入17 mL浓硫酸:在仪器b中加入39 mL浓硝酸;在仪器c中加入20%的石灰乳150 mL。
②从仪器b中放出约5mL浓硝酸,开动搅拌器然后采用滴加的方式逐渐将浓硝酸加到仪器a中,搅拌器间歇开动。当最后滴浓硝酸加完以后,完全开动搅拌器,等反应基本停止下来时,开始用电炉加热直至仪器a中的红棕色气体完全消失,立即将导气管从仪器c中取出,再停止加热。
③将仪器a中的液体倒出,取出未反应完的铜片溶液冷却至室温.析出蓝色晶体.回答下列问题:
(1)将仪器b中液体滴入仪器a中的具体操作是__________。
(2)写出装置a中生成CuSO4的化学方程式:_______。
(3)步骤②电炉加热直至仪器a中的红棕色气体完全消失,此时会产生的气体是______,该气体无法直接被石灰乳吸收,为防止空气污染,请画出该气体的吸收装置(标明所用试剂及气流方向)______。
(4)通过本实验制取的硫酸铜晶体中常含有少量Cu(NO3)2,可来用重结晶法进行提纯,检验Cu(NO3)2是否被除净的方法是_______。
(5)工业上也常采用将铜在450 °C左右焙烧,再与一定浓度的硫酸反应制取硫酸铜的方法,对比分析本实验采用的硝酸氧化法制取CuSO4的优点是_______。
(6)用滴定法测定蓝色晶体中Cu2+的含量。取a g试样配成100 mL溶液,每次取20.00 mL用c mol·L-1EDTA(H2Y )标准溶液滴定至终点,平行滴定3次,平均消耗EDTA溶液b mL,滴定反应为Cu2++H2Y =CuY +2H+,蓝色晶体中Cu2+质量分数![]() _____%.
_____%.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中药麻黄成分中含有生物碱、黄酮、鞣质、挥发油、有机酚、多糖等许多成分,其中一种有机酚的结构简式如图。下列说法正确的是( )
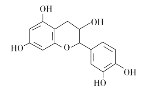
A.分子中所有碳原子可以处于同一平面
B.分子中含有2个手性原子
C.1mol该有机物跟足量浓溴水反应,最多消耗5molBr2
D.1mol该有机物与NaOH溶液反应最多消耗5molNaOH
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com