
有机物丙(C13H18O2)是一种香料,其合成路线如图所示。其中A的相对分子质量通过
质谱法测得为56,它的核磁共振氢谱显示只有两组峰;D可以发生银镜反应,在催化
剂存在条件下1 mol D与2 mol H2反应可以生成乙;丙中含有两个—CH3。
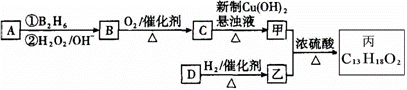

(1)A的结构简式为 ;乙的分子式为 。
(2)C与新制Cu(OH)2悬浊液反应的化学方程式_________________。
(3)D所含官能团的名称是 ;D有多种同分异构体,其中与
其所含官能团相同的同分异构体有 种(不考虑立体异构)。
(4)甲与乙反应的化学方程式为 。
(5)写出满足下列条件的有机物的结构简式
ⅰ与乙互为同分异构体;ⅱ遇FeCl3溶液显紫色;ⅲ苯环上有两个支链且苯环上的一溴代物只有两种。
【答案】(12分)(1)(CH3)2C=CH2(1分) C9H12O(1分)
(2)(CH3)2CHCHO+2Cu(OH)2+NaOH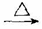 (CH3)2CHCOONa+Cu2O↓+3H2O(2分)
(CH3)2CHCOONa+Cu2O↓+3H2O(2分)
(3)碳碳双键、醛基(2分) 4(2分)
(4)(CH3)2CHCOOH + 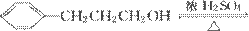
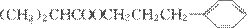 + H2O(2分)
+ H2O(2分)
(5) 
 (2分)
(2分)
【解析】
试题分析:(1)根据已知信息,A是烯烃,再根据其相对分子质量是56,可知A的分子式为C4H8,分子中有2种等效氢,则A 是2-甲基丙烯,结构简式为(CH3)2C=CH2;则甲是2-甲基丙酸,所以乙属于醇类,根据丙的分子式,可知乙的分子式=丙+H2O-甲= C9H12O;
(2)C是2-甲基丙醛,与新制Cu(OH)2悬浊液在加热条件下发生氧化反应,化学方程式为(CH3)2CHCHO+2Cu(OH)2+NaOH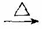 (CH3)2CHCOONa+Cu2O↓+3H2O;
(CH3)2CHCOONa+Cu2O↓+3H2O;
(3)D在催化剂存在条件下1 mol D与2 mol H2反应可以生成乙,D能发生银镜反应,所以D分子中含有碳碳双键和醛基;丙中含有两个—CH3,而甲中已有2个甲基,所以乙中不含甲基,所以D可推知D为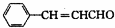 ,乙为
,乙为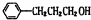 ,其中与其所含官能团相同的同分异构体(不考虑立体异构),侧链可以为-C(CHO)=CH2,也可以为-CHO、-CH=CH2,有邻、间、对三种位置关系,故符合条件的同分异构体共有4种;
,其中与其所含官能团相同的同分异构体(不考虑立体异构),侧链可以为-C(CHO)=CH2,也可以为-CHO、-CH=CH2,有邻、间、对三种位置关系,故符合条件的同分异构体共有4种;
(4)甲与乙反应的化学方程式为:(CH3)2CHCOOH + 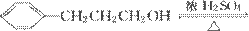
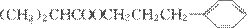 + H2O,
+ H2O,
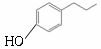
(5)乙为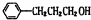 ,其同分异构体符合条件:遇FeCl3溶液显紫色,含有酚羟基;其苯环上的一溴代物只有两种,则只能有2个侧链,另外侧链为-CH2CH2CH3或-CH(CH3)2,且处于对位,故该有机物的结构简式为:
,其同分异构体符合条件:遇FeCl3溶液显紫色,含有酚羟基;其苯环上的一溴代物只有两种,则只能有2个侧链,另外侧链为-CH2CH2CH3或-CH(CH3)2,且处于对位,故该有机物的结构简式为: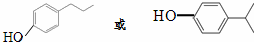 。
。
考点:考查有机物的推断,官能团的判断,化学方程式的书写,同分异构体的判断


 金版课堂课时训练系列答案
金版课堂课时训练系列答案 单元全能练考卷系列答案
单元全能练考卷系列答案 新黄冈兵法密卷系列答案
新黄冈兵法密卷系列答案科目:高中化学 来源: 题型:
下列有关说法正确的是 ( )
A.反应NH3(g)+HCl(g)= NH4Cl(s)在室温下可自发进行,则该反应的△H<0
B.当镀锡铁和镀锌铁镀层破损时,后者更易被腐蚀
C.CH3COOH溶液加水稀释后,电离平衡正向移动,溶液中的c(CH3COO-)增大
D.Na2CO3溶液中加入少量Ca(OH)2固体,CO32-水解程度减小,溶液的pH减小
查看答案和解析>>
科目:高中化学 来源: 题型:
已知25℃时,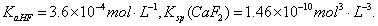 现向1L 0.2mol·L-1HF溶液中加入1L 0.2mol·L-1CaCl2溶液,则下列说法中,正确的是( )
现向1L 0.2mol·L-1HF溶液中加入1L 0.2mol·L-1CaCl2溶液,则下列说法中,正确的是( )
A.25℃时,0.1mol·L-1HF 溶液中pH=1
B.Ksp(CaF2)随温度和浓度的变化而变化
C.该体系中没有沉淀产生
D.该体系中HF与CaCl2反应产生沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
毒豇豆、毒黄瓜等毒蔬菜中含有禁用农药水胺硫磷,水胺硫磷的结构简式如图所示,对该化合物的叙述正确的是( )
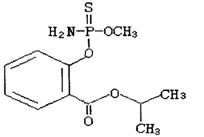
A.该化合物属于芳香烃
B.该化合物中至少有7个碳原子在同一平面
C.该化合物的分子式为C11H14O4NPS
D.该化合物能发生加聚反应、水解反应和酯化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子在给定的条件下一定能大量共存的是
A.pH=1的溶液中:Na+、 K+ 、MnO4- 、CO32-
B. 0. 1 mol/L NH4HCO3溶液中:K+、Na+、NO3-、Cl-
C. c(Fe3+) =0. 1 mol/L的溶液中:NH4+、Cl-、AlO2-、SO42-
D.室温下,水电离出的c(H+ )=1 ×10-13mo1/L的溶液中:Mg2+、K+、NO3-、Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、X、Y、Z是元素周期表前四周期中的常见元素,原子序数依次增大。A元素可形成自然界硬度最大的单质;B与A同周期,核外有三个未成对电子;X原子的第一电离能至第四电离能分别是:I1 =578kJ/mol,I2= 1817kJ/mol, I3= 2745kJ/mol,I4 =11575kJ/mol;常温常压下,Y单质是固体,其氧化物是形成酸雨的主要物质;Z的一种同位素的质量数为63,中子数为34。请回答下列问题。
(1)AY2是一种常用的溶剂,是 (填极性分子或非极性分子),分子中存在_________个σ键。
(2)X与NaOH溶液反应的离子方程式为___________。超高导热绝缘耐高温纳米XB在绝缘材料中应用广泛,晶体与金刚石类似,属于___________晶体.B的最简单氢化物容易液化,理由是___________。
(3)X、氧、B元素的电负性由大到小顺序为___________________(用元素符号作答)。
(4)Z的基态原子核外电子排布式为_____________。元素Z与人体分泌物中的盐酸以及空气反应可生成超氧酸:Z十HCl十O2 = ZCI十HO2, HO2(超氧酸)不仅是一种弱酸而且也是一种自由基,具有极高的活性。下列说法或表示不正确的是___________(填序号)。
①氧化剂是O2②HO2在碱中不能稳定存在③氧化产物是HO2, ④1 molZ参加反应有1 mol电子发生转移
已知Z的晶胞结构如下图所示,又知Z的密度为9.00g/cm3,则晶胞边长为______ ;ZYO4常作电镀液,其中YO42-的空间构型是____________ 。Y原子的杂化轨道类型是________。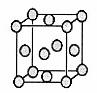
查看答案和解析>>
科目:高中化学 来源: 题型:
将标准状况下的a L氨气溶于1L水中,得到氨水的密度为b g•cm﹣3,则该氨水的物质的量浓度为( )
|
| A. |
| B. |
|
|
| C. |
| D. |
|
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com