
【题目】下列溶液加热蒸干后,能析出溶质固体的是
A. AlCl3 B. KHCO3 C. Fe2(SO4)3 D. NH4HCO3
科目:高中化学 来源: 题型:
【题目】汽车净化的主要原理为2NO(g)+2CO(g) ![]() 2CO2(g)+N2(g) △H<0。若该反应在绝热、恒容的密闭体系中进行,下列示意图正确且说明反应在进行到t1时刻达到平衡状态的是
2CO2(g)+N2(g) △H<0。若该反应在绝热、恒容的密闭体系中进行,下列示意图正确且说明反应在进行到t1时刻达到平衡状态的是
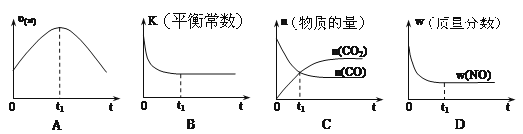
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某探究性学习实验小组做了如下实验:
实验一:利用H2C2O4 溶液和酸性KMnO4溶液之间的反应来探究“外界条件改变对化学反应速率的影响”,实验如下:
实验序号 | 试验温度/K | 溶液颜色褪至无色时所需时间/s | |||||
KMnO4溶液(含硫酸) | H2C2O4溶液 | H2O | |||||
V/mL | c/mol·L-1 | V/mL | c/mol·L-1 | V/mL | |||
A | 293 | 2 | 0.02 | 5 | 0.1 | 3 | t1 |
B | T1 | 2 | 0.02 | 3 | 0.1 | V1 | 8 |
C | 313 | 2 | 0.02 | V2 | 0.1 | 5 | t1 |
(1)通过实验A、B,可探究出_____________ (填外部因素)的改变对反应速率的影响,其中V1=__________,T1=__________;通过实验__________可探究出温度变化对化学反应速率的影响。
(2)若t1<8,则由此实验可以得出的结论是_______________;利用实验B 中数据计算,用KMnO4的浓度变化表示的反应速率为v(KMnO4span>)= __________。
实验二:探究酸的强弱对酸与镁条反应速率的影响。
实验步骤:


(a)检查装置的气密性后,添加药品;
(b)反应开始后,每隔1min记录一次生成H2的体积;
(c)将所记录的数据转化为曲线图(上图乙)。
(3)根据反应的图像(图乙)分析:0-lmin盐酸与镁反应比1-2min反应快的原因:_____________。
(4)对照实验:用20mL水代替酸进行实验。
实验现象:当水滴入锥形瓶中,注射器的活塞_________(填“会”或“不会”)向右移动。
问题分析:针对上述现象,上图中气体发生装置是否合理:_______(填“合理”或“不合理”)若合理,则忽略下问;若不合理,请改进上述装置使其变成合理的装置图:_____________ (用必要的文字或装置图进行回答)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图表示构成细胞的元素及化合物,其中工、ll、Ⅲ是生物大分子,x、y、 z代表不同的小分子。请回答下列问题:

(1)图中Ⅰ在动物细胞中是______,其基本组成单位x是______
(2)若II是染色体的主要成分,则y是______
(3)图中x,y,z共有的化学元素是_。
(4)在生物体中的z,其结构通式为______;请列举出Ⅲ的两个功能: ______、______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】温度为T1时,在三个容积均为1L的恒容密闭容器中仅发生反应:2NO2(g)![]() 2NO(g)+O2(g)相关数据如下表所示。下列说法错误的是( )
2NO(g)+O2(g)相关数据如下表所示。下列说法错误的是( )
容器 编号 | 物质的起始浓度 (mol·L-1) | 物质的平衡浓度 (mol·L-1) | ||
c(NO2) | c(NO) | c(O2) | c(O2) | |
Ⅰ | 0.6 | 0 | 0 | 0.2 |
Ⅱ | 0.3 | 0.5 | 0.2 | |
Ⅲ | 0 | 0.5 | 0.35 | |
A. 容器Ⅰ中发生反应的平衡常数为0.8 B. 容器Ⅱ中发生反应的起始阶段有v正>v逆
C. 达到平衡时,容器Ⅲ中![]() >1 D. 达到平衡时,容器Ⅰ与容器Ⅲ中的总压强之比为16∶17
>1 D. 达到平衡时,容器Ⅰ与容器Ⅲ中的总压强之比为16∶17
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】砷(As)是VA族元素,砷及其化合物被应用于农药和合金中。回答下列问题:
(1)基态砷原子的电子排布式为___________________,第四周期元素中,第一电离能低于砷原子的p区元素有____________ (填元素符号)。
(2)氮原子间能形成氮氮叁键,而砷原子间不易形成叁键的原因是____________。
(3)AsH3分子为三角锥形,键角为91.80°,小于氨分子键角107°,AsH3分子键角较小的原因是____________。
(4)亚砷酸(H3AsO3)分子中,中心原子砷的VSEPR模型是____________,砷原子杂化方式为____________。
(5)砷化镍的晶胞如图。晶胞参数a=360.2pm, c=500.9pm, γ=120°。

①镍原子配位数为____________,配原子构成的几何体是____________。
②该晶体密度的计算式为____________g·cm-3。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关自然资源的开发利用的叙述正确的是( )
A.通过催化重整,可从石油中获取环状烃
B.裂化汽油可用于萃取溴水中的溴
C.石油的裂化和裂解属于化学变化而煤的液化、气化属于物理变化
D.煤中含有大量的苯、甲苯、二甲苯等有机物,可通过煤的干馏来提取
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是通过热化学循环在较低温度下由水或硫化氢分解制备氢气的反应系统原理,下列说法不正确的是

A. 反应②为反应③提供了原料
B. 反应②也是SO2资源利用的方法之一
C. 制得等量H2所需能量较少的是系统(I)
D. 系统(I)制氢的热化学方程式为H2O(l) ![]() H2(g) + 1/2O2(g) ΔH = +286 kJ/mol
H2(g) + 1/2O2(g) ΔH = +286 kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属是重要的资源,下面有关金属及其化合物的说法错误的是( )
A.电解熔融MgCl2制备Mg
B.钛和钛合金被誉为“21世纪最有发展前景的金属材料”,主要用来制作飞机发动机部件
C.高铁对钢轨强度、韧性和易加工要求很高,适合做高铁钢轨的是中碳钢
D.因为Al2O3的硬度很大,所以可用于制造耐高温材料
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com