
【题目】现有一种以黄铜矿和硫磺为原料制取铜和其他产物的新工艺,原料的综合利用率较高.其主要流程如图: 
注:反应Ⅱ的离子方程式为Cu2++CuS+4Cl﹣=2[CuCl2]﹣+S↓
请回答下列问题:
(1)反应Ⅲ中的CuCl2﹣中铜元素的化合价为 , 传统工艺制铜是将铜矿砂与空气在高温下煅烧,使这种方
法的缺点是要消耗大量的热能以及(完成合理的一种即可).
(2)为使反应Ⅰ中充分进行,工业可采取的措施是 , 反应Ⅰ生成12gFeS2转移的电子数为 .
(3)反应Ⅲ的离子方程式为 , 一定温度下,在反应Ⅲ所得的溶液中加入稀硫酸,可以析出硫酸铜晶
体,其可能的原因是 .
(4)工业上炼钢时,可将铁红投入熔融的生铁中,炼钢时为了降低含碳量,该过程中主要反应的化学方程
式是 . 工业上可以用NaOH溶液或氨水吸收过量的SO2 , 分别生成NaHSO3、NH4HSO3 , 其水溶液均
呈酸性,相同条件下,同浓度的两种水溶液中c(SO32﹣)较小的是 .
(5)某硫酸厂为测定反应Ⅳ所得气体中SO2的体积分数,取280mL(已折算成标准状况)气体样品与足量
Fe2(SO4)3溶液完全反应后,用浓度为0.02000molL﹣1的K2Cr2O7标准溶液滴定至终点,消耗K2Cr2O7溶液25.00mL,已知Cr2O72﹣+Fe2++H+→Cr3++Fe3++H2O(未配平)反应Ⅳ所得气体中SO2的体积分数为 .
【答案】
(1)0;SO2会导致大气污染
(2)粉碎固体等;0.1NA
(3)4CuCl2﹣+O2+4H+═4Cu2++8Cl﹣+2H2O;该温度下,硫酸铜的溶解度小于氯化铜
(4)3C+Fe2O3 ![]() 2Fe+3CO;NH4HSO3溶液
2Fe+3CO;NH4HSO3溶液
(5)12.00%
【解析】解:流程中反应Ⅰ的化学化方程为CuFeS2+S═FeS2+CuS,黄铜矿与S在高温下煅烧,使其转变为FeS2、CuS,加入HCl、NaCl、CuCl2混合溶液 发生反应Cu2++CuS+4Cl﹣=2[CuCl2]﹣+S↓,过滤得到滤液中通入空气发生反应4CuCl2﹣+O2+4H+=4Cu2++8Cl﹣+2H2O,一定温度下,在反应Ⅲ所得的溶液中加入稀硫酸,可以析出硫酸铜晶体,结晶分离得到硫酸铜晶体,加入铁还原溶液得到铜;滤渣分离得到FeS和S,(1)反应Ⅲ中的CuCl2﹣中Cl是﹣1价,铜元素的化合价为0价,富铜矿砂与空气在高温下煅烧,要消耗大量的热能,生成SO2会导致大气污染,所以答案是:0;SO2会导致大气污染;(2)粉碎固体可以增大接触面积,加快反应速率,则为使反应Ⅰ充分进行,工业上可采取的措施是粉碎固体等,流程中反应Ⅰ的化学化方程为CuFeS2+S═FeS2+CuS,反应Ⅰ生成120gFeS2转移的电子1mol,所以反应Ⅰ生成12gFeS2转移的电子数为0.1NA ,
所以答案是:粉碎固体等;0.1NA;(3)反应Ⅲ中生成铜离子,则离子反应为4CuCl2﹣+O2+4H+═4Cu2++8Cl﹣+2H2O,相同条件下硫酸铜的溶解度小,则该温度下,硫酸铜的溶解度小于氯化铜,所以向反应Ⅲ所得的溶液中加入稀硫酸,可以析出硫酸铜晶体,
所以答案是:4CuCl2﹣+O2+4H+═4Cu2++8Cl﹣+2H2O;该温度下,硫酸铜的溶解度小于氯化铜;(4)炼钢时,可将铁红投入熔融的生铁中,滤液碳和氧化铁反应生成铁和一氧化碳,反应的化学方程式为:3C+Fe2O3 ![]() 2Fe+3CO↑,HSO3﹣H++SO32﹣ , 而NH4+水解:NH4++H2ONH3 . H2O+H+ , 使溶液中c(H+)增大,抑制HSO3﹣电离,故NH4HSO3溶液中SO32﹣浓度较小,
2Fe+3CO↑,HSO3﹣H++SO32﹣ , 而NH4+水解:NH4++H2ONH3 . H2O+H+ , 使溶液中c(H+)增大,抑制HSO3﹣电离,故NH4HSO3溶液中SO32﹣浓度较小,
所以答案是:3C+Fe2O3 ![]() 2Fe+3CO↑;NH4HSO3;(5)发生氧化还原反应生成硫酸亚铁,离子反应为SO2+2Fe3++2H2O=SO42﹣+2Fe2++4H+ , 利用14H++Cr2O72﹣+6Fe2+═2Cr3++6Fe3++7H2O、SO2+2Fe3++2H2O=SO42﹣+2Fe2++4H+ ,
2Fe+3CO↑;NH4HSO3;(5)发生氧化还原反应生成硫酸亚铁,离子反应为SO2+2Fe3++2H2O=SO42﹣+2Fe2++4H+ , 利用14H++Cr2O72﹣+6Fe2+═2Cr3++6Fe3++7H2O、SO2+2Fe3++2H2O=SO42﹣+2Fe2++4H+ ,
可知,3SO2~Cr2O72﹣ ,
3 1
x 0.02mol/L×0.025L
解得x=0.0015mol,
反应Ⅳ所得气体中SO2的体积分数为: ![]() ×100%=12.00%,
×100%=12.00%,
所以答案是:12.00%.


 名师点拨卷系列答案
名师点拨卷系列答案 英才计划期末调研系列答案
英才计划期末调研系列答案科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A.向某溶液中滴加KSCN溶液,溶液呈血红色,证明存在Fe3+
B.氢氧化钠溶液保存在带橡皮塞的试剂瓶中
C.漂白粉常作环境消毒剂
D.工业上用电解饱和食盐水来制取金属钠
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有铁、氧化铁、四氧化三铁的混合物3.64克,加入50mL2mol/L盐酸溶液时,恰好完全反应,并且生成气体的体积在标准状况下为0.224升,向所得溶液中滴加KSCN溶液无明显变化.若将等质量的该混合物在CO中加热并充分反应,冷却后固体的质量为( )
A.2 8克
B.1.52克
C.3.4克
D.2克
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H2O2俗称双氧水,医疗上常用3%的双氧水进行伤口或耳炎消毒。下列关于H2O2的说法正确的是( )
A. H2O2分子中含有氢离子
B. H2O2分子中既有离子键,又有共价键
C. H2O2属于共价化合物
D. H2O2属于H2和O2组成的混合
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】气化和液化是使煤变成清洁能源的有效途径。煤的气化的主要反应是:C+H2O(g) ![]() CO+H2 , CO和H2的混合气体是合成多种有机物的原料气,研究由CO、H2合成有机物的化学称为一碳化学。下图是合成某些物质的路线图:
CO+H2 , CO和H2的混合气体是合成多种有机物的原料气,研究由CO、H2合成有机物的化学称为一碳化学。下图是合成某些物质的路线图: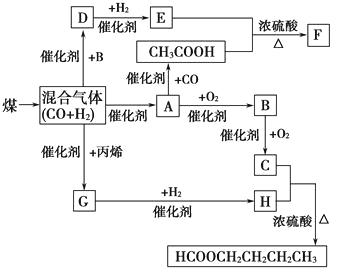
其中,D易溶于水,且与CH3COOH互为同分异构体,F分子中的碳原子数是D中的3倍,H经催化氧化可得到G。请回答下列问题:
(1)写出下列物质的结构简式:A: , H: , 指出A和H的关系。
(2)利用合成气(H2+CO)生产汽油、甲醇和氨等已经实现了工业化,合成气也可合成醛、酸、酯等多种产物,下列表述正确的是。
①以合成气为原料的反应都是化合反应
②改变合成气中CO与H2的体积比,可得到不同的产物
③合成气的转化反应需在适当的温度和压强下通过催化完成
④从合成气出发生成气态烃或醇类有机物是实现“煤变油”的有效途径
⑤以合成气为原料的反应产物中不可能有烯烃或水
A.①②④
B.②③④
C.②④⑤
D.③④⑤
(3)写出下列反应的化学方程式:
①CH3COOH+E→F:。
②D与新制氢氧化铜悬浊液加热:。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】含同一元素的常见 A、B、C,有如下转化关系(条件未标注): 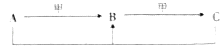
(1)当甲是KOH时,白色沉淀B为 .
(2)当甲为H2O时,气体B为 .
(3)当A为Na时,单质甲为 .
(4)当A为NH3时,气体单质B为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验是进行科学探究的主要方法.回答下列问题: 
(1)实验室利用A 发生装置制备的常见气体有 .
(2)检验装置B的气密性方法是 .
(3)收集一瓶纯净氯气,选择上图装置,按气流方向,用小写字母表示连接顺序(装置不重复使用).实验室检验氯气的方法是 .
(4)某实验小组按顺序连接adcfeg制取并收集氨气,导致实验失败,原因是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现代科技将20984Po涂于飞机表面,可以吸收和屏蔽雷达波和红外线辐射,从而达到隐形目的。下面列出该原子核内中子数与核外电子数之差的数据正确的是( )
A. 41B. 84C. 125D. 209
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com