
以NA表示阿伏伽德罗常数,下列说法正确的是
| A.分子总数为NA的NO2和CO2混合气体含有的氧原子数为2NA |
| B.标准状况下,由Na2O2制的11.2LO2反应转移的电子束为2NA |
| C.18.0g重水(D2O)与20gNe所含有的电子数都为10NA |
| D.0.5mol O3与11.2L O2所含的分子数都为0.5NA |
 优百分课时互动系列答案
优百分课时互动系列答案 开心蛙状元作业系列答案
开心蛙状元作业系列答案科目:高中化学 来源: 题型:单选题
下列选项中所涉及到的两个量的一定相等的是
| A.11. 2LCl2与4.25gNH3所含有的原子数 |
| B.18.0g重水(D2O)与20gNe所含有的电子数 |
| C.标准状况下36gH2O与1.204×1024个O2分子所占的体积 |
| D.等物质的量的Al分别与足量的盐酸、NaOH溶液反应转移的电子数 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
已知某亚铁盐的化学式可表示为(NH4)a Feb(s04)c。取一定质量的该亚铁盐样品全部溶于足量的水中,将所得溶液平均分为两份。一份溶液中加入足量的BaCl2溶液,得到白色沉淀9.32 g。另一份溶液同足量的浓NaOH溶液共热,产生的氨气用100 mL 0.5mo1·L-1稀硫酸吸收后(设产生的氨全部逸出),剩余的硫酸再用1.5 mol·L-1NaOH溶液中和,需NaOH溶液40mL。该亚铁盐样品中b:c的比值为
| A.1:1 | B.2:1 | C.1:2 | D.3:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
以下最接近阿伏加德罗常数的是
| A.2.0L 1.0mol·L—1 CH3COOH溶液中的H+离子数 |
| B.2.0L1.0 mol·L—1CH3COONa溶液中的CH3COO—离子数 |
| C.1.0L 1.0 mol·L—1NaHCO3溶液中的HCO3—离子数 |
| D.1.0L1.0 mol·L—1Na2CO3溶液中的 CO32—离子数 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
研究发现,硝酸越稀,还原产物中氮元素的化合价越低。某同学取适量的铁铝合金与足量很稀的硝酸充分反应,没有气体放出。在反应结束后的溶液中,逐滴加入5 mol/L的NaOH溶液,所加NaOH溶液的体积(mL)与产生的沉淀的物质的量(mol)的关系如图所示。下列说法正确的是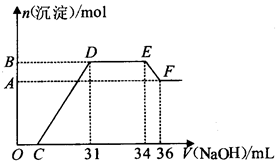
| A.溶液中结合OH-能力最强的离子是NH4+ |
| B.D点时溶液中存在:c(NH4+)+c(H+)=c(OH-)+c(NO3-) |
| C.合金中n(Fe) :n(Al)=1 :3 |
| D.C的值为7 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
(4分)已知Na2SO3易被空气氧化变质,欲用氧化还原滴定法来测定实验室里Na2SO3的纯度。取实验室里Na2SO3样品63g,溶于水配成250mL溶液。从其中取出25mL Na2SO3溶液用0.4mol·L-1酸性KMnO4溶液滴定,当溶液刚好变为紫色且半分钟不褪色时,用去40mL酸性KMnO4溶液(已知:5SO32-+2MnO4-+6H+ 5SO42-+2Mn2++3H2O)。则实验室里的Na2SO3的纯度为多少?
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
用NA表示阿伏加德罗常数的值。下列叙述正确的是
| A.0.1 mol Fe在0.1mol CL2中充分燃烧,转移的电子数为0.3NA |
| B.标准状况下,11.2 L CCl4所含分子数约为0.5NA |
| C.常温下,pH=13的NaOH溶液中,OH-的数目为0.1NA |
| D.常温、常压下,14g CO与N2的混合气含的原子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
标准状况下, 1体积水吸收560体积氨气所得氨水的密度是0.91g / mL, 该氨水的物质的量浓度约是
| A.4 mol / L | B.8 mol / L | C.10 mol /L | D.16 mol / L |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com