
【题目】高分子化合物在生产生活中有着广泛的用途。如图为合成高分子化合物G的流程。
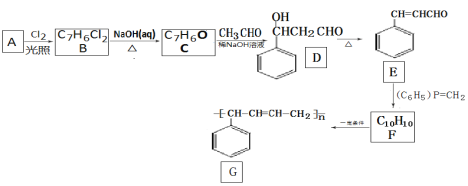
已知:①![]() →
→![]()
②![]()
![]()
![]()
请回答下列问题:
(1)A物质为烃,则A的名称为_________,物质E含有的官能团名称是_________。
(2)由C生成D的反应类型是____________。
(3)由B生成C的化学反应方程式为_________。
(4)F的结构简式为___________。
(5)M是D的同分异构体,M满足以下条件:苯环上取代基的数目不少于两个,且能够与NaHCO3反应放出CO2,共有_______种。其中核磁共振H谱为4组峰,其峰面积比为6:2:1:1的结构简式为_______。
(6)根据题中信息和有关知识,以2-丙醇为原料,选用必要的无机试剂,合成![]() ,写出合成路线 __________。
,写出合成路线 __________。
【答案】甲苯 碳碳双键、 醛基 加成反应 ![]() +2NaOH
+2NaOH![]()
![]() +2NaCl+H2O
+2NaCl+H2O 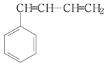 12
12 ![]()
![]()
![]() CH3COCH3
CH3COCH3![]()
![]()
![]()
![]()
![]()
![]()
【解析】
由合成流程可知,C与乙醛发生加成反应生成D,则C为![]() ,逆推可知,B为
,逆推可知,B为![]() ,A为
,A为![]() ,D发生消去反应生成E,E发生信息②中的反应生成F为
,D发生消去反应生成E,E发生信息②中的反应生成F为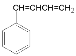 ,F再发生加聚反应得到高分子化合物G,据此可分析解答问题。
,F再发生加聚反应得到高分子化合物G,据此可分析解答问题。
(1)根据上述分析可知,A为![]() ,名称为甲苯,E物质的结构简式为
,名称为甲苯,E物质的结构简式为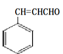 ,其中含有的官能团由碳碳双键、醛基,故答案为:甲苯;碳碳双键、醛基;
,其中含有的官能团由碳碳双键、醛基,故答案为:甲苯;碳碳双键、醛基;
(2)由上述分析知,C与乙醛发生加成反应生成D,故答案为:加成反应;
(3)由B生成C的化学反应方程式为![]()
![]()
![]() ,故答案为:
,故答案为:![]()
![]()
![]() ;
;
(4)E发生信息②中的反应生成F为 ,故答案为:
,故答案为: ;
;
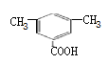
(5)M是D的同分异构体,M满足以下条件:苯环上取代基的数目不少于两个,且能够与NaHCO3反应放出CO2,说明M含有羧基,则苯环上有两个取代基的情况有—COOH、—CH2CH3或—CH2COOH、—CH3两种情况,均有邻、间、对三种位置结构,苯环上有3个取代基的情况为2个—CH3、—COOH,2个甲基有邻、间、对3种位置结构,对应的羧基分别有2种、3种、1种位置,因此,符合条件的M共有3×2+2+3+1=12种,其中核磁共振氢谱为4组峰,其峰面积比为6:2:1:1的结构简式有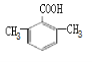 、
、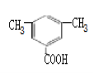 ,故答案为:12;
,故答案为:12; 、
、 ;
;
(6)由信息②实现增大碳原子数目,并引入碳碳双键,2-丙醇发生氧化反应生成![]() ,然后与(C6H5)P=CH2反应得到
,然后与(C6H5)P=CH2反应得到![]() ,再与溴发生加成反应得到
,再与溴发生加成反应得到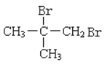 ,最后碱性条件下水解得到
,最后碱性条件下水解得到![]() ,故答案为:
,故答案为: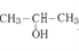
![]() CH3COCH3
CH3COCH3![]()
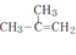
![]()
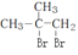
![]()
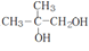 。
。


 阳光课堂课时优化作业系列答案
阳光课堂课时优化作业系列答案科目:高中化学 来源: 题型:
【题目】短周期元素A、B、D、E、G、J在周期表中的位置如下:
A | |||||||
B | D | ||||||
E | G | J |
根据上表回答问题:
(1)![]() 在周期表中的位置是______,D的原子结构示意图_____。
在周期表中的位置是______,D的原子结构示意图_____。
(2)![]() 、B、E、G的原子半径由大到小的顺序是_____
、B、E、G的原子半径由大到小的顺序是_____![]() 填元素符号
填元素符号![]() 。
。
(3)![]() 、D的气态氢化物的稳定性关系为______
、D的气态氢化物的稳定性关系为______![]() 填化学式
填化学式![]() ,它们都属于______
,它们都属于______![]() 离子化合物或共价化合物
离子化合物或共价化合物![]() 。
。
(4)第三周期元素的最高价氧化物对应的水化物中,有一种物质既能与强酸反应又能与强碱反应,写出这种物质跟氢氧化钠溶液反应的化学方程式________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,将0.1mol/L的一元酸HA溶液逐滴滴加到10mL0.1mol/LNaOH溶液中,pH的变化曲线如图所示。下列说法错误的是

A. a点所示溶液中c(Na+)>c(A-)>c(OH-)>c(HA)
B. a、b两点所示溶液中水的电离程度a点大于b点
C. pH=7时,c(Na+)=c(A-)+c(HA)
D. 一元酸HA为弱酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】柠檬烯是一种食用香料,其结构简式如图,有关柠檬烯的分析正确的是
![]()
A.一定条件下,它分别可以发生加成、取代、氧化、还原等反应
B.它的分子式为C10H18
C.它的分子中所有的碳原子一定在同一平面上
D.它和丁基苯(![]() C4H9)互为同分异构体
C4H9)互为同分异构体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】KIO3为白色结晶粉末,工业上可用电解法制备,装置如图所示,配制碱性电解质溶液(KOH+I2)时,I2发生氧化还原反应,生成KIO3和KI。下列说法错误的是

A.电解时b为阴极
B.电解过程中阴极区溶液pH降低
C.电解过程中K+由左向右通过阳离子交换膜
D.a极反应式为:I--6e-+6OH=IO3-+3H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将0.1mol/L的K2SO4溶液、0.2mol/L的Al2(SO4)3溶液和纯水混合,要使混合液中K+ 、Al3+、 SO42-的浓度分别为0.1mol/L、0.1mol/L、0.2mol/L,则所取三者的体积比是(假定混合后的体积不变)( )
A.1:1:1 B.2:1:2 C.1:1:2 D.2:1:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯酸镁[Mg(ClO3)2]常用作催熟剂、除草剂等,实验室制备少量Mg(ClO3)2·6H2O的流程如图:
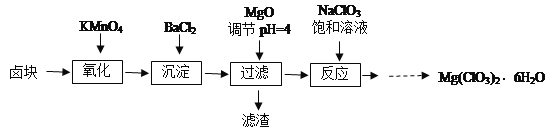
已知:①卤块主要成分为MgCl2·6H2O,含有MgSO4、FeCl2等杂质。
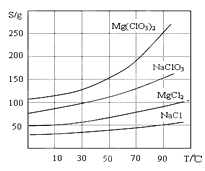
②四种化合物的溶解度(S)随温度(T )变化曲线如图所示:
(1)过滤所需要的玻璃仪器有______。
(2)如图是某学生的过滤操作示意图,其操作不规范的是______(填标号)。
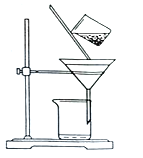
a.漏斗末端颈尖未紧靠烧杯壁
b.玻璃棒用作引流
c.将滤纸湿润,使其紧贴漏斗壁
d.滤纸边缘高出漏斗
e.用玻璃棒在漏斗中轻轻搅动以加快过滤速度
(3)加入BaCl2的目的是除去SO42-,如何检验SO42-已沉淀全?______
(4)加入NaClO3饱和溶液会发生如下反应:MgCl2+2NaClO3=Mg(ClO3)2+2NaCl↓,请利用该反应,结合图像,制取Mg(ClO3)2·6H2O的实验步骤依次为:①取样,加入NaClO3饱和溶液充分反应,②______;③______;④______;⑤过滤、洗涤,获得Mg(ClO3)2·6H2O晶体。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为铜与稀硝酸反应的有关性质实验(洗耳球:一种橡胶为材质的工具仪器,可挤压)。
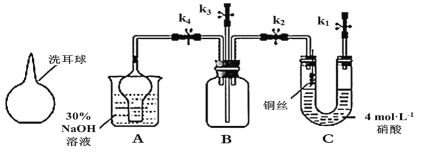
实验步骤如下:
①按照如图装置连接好仪器,关闭所有止水夹。检查装置的气密性。
②在装置A中的烧杯中加入30%的氢氧化钠溶液。在装置C的U型管中加入4.0mol·L-1的硝酸,排除U型管左端管内空气。
③塞紧连接铜丝的胶塞,打开止水夹K1,反应进行一段时间。
④进行适当的操作,使装置C中产生的气体进入装置B的广口瓶中,气体变为红棕色。气体进入烧杯中与氢氧化钠溶液反应。
回答下列问题:
(1)装置C中发生反应的离子方程式为__。反应后的溶液呈蓝色,其原因是铜离子和水分子形成了水合铜离子,1mol水合铜离子中含有σ键数目为12NA,该水合铜离子的化学式为__。
(2)装置A上面的导管口末端也可以连接__来代替干燥管,实现同样作用。
(3)加入稀硝酸,排除U型管左端管内空气的操作是__。
(4)步骤④中“使装置C中产生的气体进入装置B的广口瓶中”的操作是打开止水夹__(填写序号),并用洗耳球在U型管右端导管口挤压空气进入。
(5)步骤④中使“气体进入烧杯中与氢氧化钠溶液反应”的操作是__,尾气中主要含有NO2和空气,与NaOH溶液反应只生成一种盐,则离子方程式为有__。
(6)某同学发现,本实验结束后硝酸还有很多剩余,请你改进实验,使能达到预期实验目的,反应结束后硝酸的剩余量尽可能较少,你的改进是__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】羟基乙酸钠易溶于热水,微溶于冷水,不溶于醇、醚等有机溶剂。制备少量羟基乙酸钠的反应为
![]()
实验步骤如下:
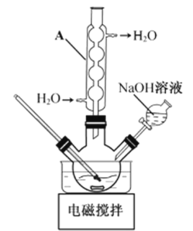
步骤1:如图所示装置的反应瓶中,加入40g氯乙酸、50mL水,搅拌。逐步加入40%NaOH溶液,在95℃继续搅拌反应2小时,反应过程中控制pH约为9。
步骤2:蒸出部分水至液面有薄膜,加少量热水,趁热过滤。滤液冷却至15℃,过滤得粗产品。
步骤3:粗产品溶解于适量热水中,加活性炭脱色,分离掉活性炭。
步骤4:将去除活性炭后的溶液加到适量乙醇中,冷却至15℃以下,结晶、过滤、干燥,得羟基乙酸钠。
(1)步骤1中,如图所示的装置中仪器A的名称是___________;逐步加入NaOH溶液的目的是____________。
(2)步骤2中,蒸馏烧瓶中加入沸石或碎瓷片的目的是_______________。
(3)步骤3中,粗产品溶解于过量水会导致产率__________(填“增大”或“减小”);去除活性炭的操作名称是_______________。
(4)步骤4中,将去除活性炭后的溶液加到适量乙醇中的目的是_______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com