
【题目】现给你一试管二氧化氮,其他药品和仪器自选。
(1)设计实验,要求尽可能多地使二氧化氮被水吸收。某化学兴趣小组实验设计如下,请你帮他们将下表补充完整。
实验步骤 | 现象 | 化学方程式(解释) | |
① | 将一支充满NO2的试管倒放在盛有水的水槽中 | ___ | ___ |
② | 制取少量氧气 | ___ | |
③ | ___ | ___ | 4NO2+2H2O+O2=4HNO3 |
(2)完成上述实验的装置图如图,请你在方框内将它补充完整(加持装置可省略),需标明所用药品的名称___。

(3)以上设计让你对工业上生产硝酸有什么启示___?(从原料的充分利用、减少污染物的排放等方面考虑)。
【答案】红棕色气体逐渐消失,水位上升,最后水充满整个试管的![]() ,无色气体充满试管上部
,无色气体充满试管上部![]() 3NO2+H2O=2HNO3+NO 2KClO3
3NO2+H2O=2HNO3+NO 2KClO3![]() 2KCl+3O2↑或2H2O2
2KCl+3O2↑或2H2O2![]() 2H2O+O2↑, 将氧气慢慢地通入步骤①的试管中 无色气体变为红棕色气体,又变为无色气体,但气体体积逐渐缩小,液面不断上升最后充满整个试管
2H2O+O2↑, 将氧气慢慢地通入步骤①的试管中 无色气体变为红棕色气体,又变为无色气体,但气体体积逐渐缩小,液面不断上升最后充满整个试管 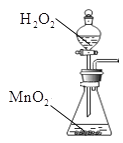 或
或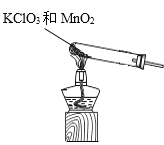 硝酸工业常在吸收反应进行过程中补充一些空气,使生成的NO再氧化为二氧化氮,从而尽可能地转化为硝酸(提高了原料的利用率,同时减少了污染性气体的排放)
硝酸工业常在吸收反应进行过程中补充一些空气,使生成的NO再氧化为二氧化氮,从而尽可能地转化为硝酸(提高了原料的利用率,同时减少了污染性气体的排放)
【解析】
(1)①二氧化氮与水的反应方程式为:3NO2+H2O=2HNO3+NO,进入试管中的液体体积占试管容积的![]() ,剩余
,剩余![]() 气体变为无色;
气体变为无色;
②实验室制取氧气是利用氯酸钾和二氧化锰固体混合加热反应生成氧气,或利用过氧化氢中加入二氧化锰催化剂反应生成氧气;
③液面不再上升时,通入氧气和一氧化氮反应生成红棕色的二氧化氮,二氧化氮溶于水又生成一氧化氮和硝酸,气体变为无色气体,液面上升,直至当试管充满液体,无气体剩余;
(2)方框内是制取氧气的装置;
(3) 工业上生产硝酸,主要反应为:4NH3+5O2![]() 4NO + 6H2O;2NO+O2=2NO2;3NO2+H2O=2HNO3+NO或4NO2+O2+2H2O=4HNO3。
4NO + 6H2O;2NO+O2=2NO2;3NO2+H2O=2HNO3+NO或4NO2+O2+2H2O=4HNO3。
(1)①尽可能多地使二氧化氮被水吸收,将一支充满NO2的试管倒放在盛有水的水槽中,NO2是红棕色气体,与水反应生成硝酸和一氧化氮,其反应方程式为:3NO2+H2O=2HNO3+NO,进入试管中的液体体积占试管容积的![]() ,剩余
,剩余![]() 气体变为无色,故答案为:红棕色气体逐渐消失,水位上升,最后水充满整个试管的
气体变为无色,故答案为:红棕色气体逐渐消失,水位上升,最后水充满整个试管的![]() ,无色气体充满试管上部
,无色气体充满试管上部![]() ;3NO2+H2O=2HNO3+NO;
;3NO2+H2O=2HNO3+NO;
②实验室制取氧气是利用氯酸钾和二氧化锰固体混合加热反应生成氧气,或利用过氧化氢中加入二氧化锰催化剂反应生成氧气,其化学反应方程式为:2KClO3![]() 2KCl+3O2↑或2H2O2
2KCl+3O2↑或2H2O2![]() 2H2O+O2↑,故答案为:2KClO3
2H2O+O2↑,故答案为:2KClO3![]() 2KCl+3O2↑或2H2O2
2KCl+3O2↑或2H2O2![]() 2H2O+O2↑;
2H2O+O2↑;
③液面不再上升时,通入氧气和一氧化氮反应生成红棕色的二氧化氮,二氧化氮溶于水又生成一氧化氮和硝酸,气体变为无色气体,液面上升,直至当试管充满液体,无气体剩余,反应为:2NO+O2=2NO2、3NO2+H2O=2HNO3+NO或4NO2+2H2O+O2=4HNO3,故答案为:将氧气慢慢地通入步骤①的试管中;无色气体变为红棕色气体又变为无色气体,但气体体积逐渐缩小,液面不断上升最后充满整个试管;
(2)方框内是制取氧气的装置,利用氯酸钾和二氧化锰固体混合加热反应生成氧气的发生装置为: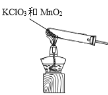 ,利用过氧化氢中加入二氧化锰催化剂反应生成氧气的发生装置为:
,利用过氧化氢中加入二氧化锰催化剂反应生成氧气的发生装置为: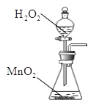 ,故答案为:
,故答案为: 或
或 ;
;
(3) 工业上生产硝酸,主要反应为:4NH3+5O2![]() 4NO + 6H2O;2NO+O2=2NO2;3NO2+H2O=2HNO3+NO或4NO2+O2+2H2O=4HNO3,硝酸工业常在吸收反应进行过程中补充一些空气,使生成的NO再氧化为二氧化氮,从而尽可能地转化为硝酸(提高了原料的利用率,同时减少了污染性气体的排放),故答案为:硝酸工业常在吸收反应进行过程中补充一些空气,使生成的NO再氧化为二氧化氮,从而尽可能地转化为硝酸(提高了原料的利用率,同时减少了污染性气体的排放)。
4NO + 6H2O;2NO+O2=2NO2;3NO2+H2O=2HNO3+NO或4NO2+O2+2H2O=4HNO3,硝酸工业常在吸收反应进行过程中补充一些空气,使生成的NO再氧化为二氧化氮,从而尽可能地转化为硝酸(提高了原料的利用率,同时减少了污染性气体的排放),故答案为:硝酸工业常在吸收反应进行过程中补充一些空气,使生成的NO再氧化为二氧化氮,从而尽可能地转化为硝酸(提高了原料的利用率,同时减少了污染性气体的排放)。


科目:高中化学 来源: 题型:
【题目】一定温度下,水存在H2O![]() H++OH-ΔH=Q(Q>0)的平衡,下列叙述一定正确的是
H++OH-ΔH=Q(Q>0)的平衡,下列叙述一定正确的是
A. 向水中滴入少量稀盐酸,平衡逆向移动,Kw减小
B. 将水加热,Kw增大,pH减小
C. 向水中加入少量固体CH3COONa,平衡逆向移动,c(H+)降低
D. 向水中加入少量固体硫酸钠,c(H+)=10-7mol·L-1,Kw不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ni2+在氨性溶液中和镍试剂(丁二酮肟)反应生成鲜红色的螯合物沉淀,在定性分析中用于鉴定![]() 。该反应可表示为
。该反应可表示为

(1)Ni在元素周期表中的位置是_______,其基态原子的未成对电子数是_______。
(2)与Ni同周期,基态原子最外层电子数为1的元素有________(填元素符号)。其中原子序数最大的元素,其基态原子核外电子排布不符合________(填选项字母)。
A.构造原理 B.泡利不相容原理 C.洪特规则
(3)已知丁二酮肟(物质A)通常情况下是白色粉末,熔点238~240℃,溶于乙醇、乙醚,几乎不溶于水。则丁二酮肟的晶体类型是________。
(4)丁二酮肟的组成元素电负性由大到小的顺序是________。
(5)物质B中含有的微粒间作用力类型有________。
A.离子键 B.共价键 C.氢键 D.配位键
(6)物质B中C原子的杂化方式是________。
(7)氧化镍(NiO)的晶体结构为立方晶系,其晶胞结构与氯化钠相似。氧化镍晶胞中,与一个Ni2+紧邻且距离相等的O2-以线段相连,构成的几何图形为________。
(8)某种氧化镍晶体中存在如图所示的缺陷:一个Ni2+空缺,另有两个Ni2+被两个Ni3+取代,晶体仍显电中性。实验测得该氧化镍晶体的化学式为Ni0.90O,其晶胞参数为acm,NA代表阿伏加德罗常数的值,则该晶体的密度为________(用含a和NA的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】色氨酸是植物体内生长素生物合成重要的前体物质,普遍存在于高等植物中。纯净的色氨酸为白色或微黄色结晶,微溶于水易溶于盐酸或氢氧化钠,其结构如图所示,下列关于色氨酸的说法不正确的是
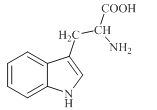
A.色氨酸的分子式为C11H12N2O2
B.色氨酸能发生取代、加成、酯化、中和反应
C.色氨酸微溶于水而易溶于酸或碱溶液是因为其与酸、碱都能反应生成盐
D.将色氨酸与甘氨酸(NH2CH2COOH)混合,在一定条件下最多可形成三种二肽
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CH4—CO2催化重整不仅可以得到合成气(CO和H2),还对温室气体的减排具有重要意义,该反应为:CH4(g)+CO2(g)![]() 2CO(g)+2H2(g)。某温度下,在体积为2L的恒容密闭容器中加入2molCH4、1molCO2以及催化剂进行重整反应,5min时达到平衡,测得CO的浓度为0.5mol/L。
2CO(g)+2H2(g)。某温度下,在体积为2L的恒容密闭容器中加入2molCH4、1molCO2以及催化剂进行重整反应,5min时达到平衡,测得CO的浓度为0.5mol/L。
回答下列问题:
(1)0~5min时间内用H2表示的化学反应速率为___mol/(L·min)。
(2)达平衡时CH4的物质的量分数为___,CO2的转化率是___。
(3)反应前后混合气体的压强之比为___。
(4)为了加快反应速率,可采取什么措施___(写两条)。
(5)下表中的数据是破坏1mol物质中的化学键所消耗的能量:
物质 | CH4 | CO2 | CO | H2 |
能量/kJ | 1660 | 1490 | 1072 | 436 |
该催化重整反应中反应物的总能量___生成物的总能量(填“大于”或“小于”)。
(6)下列能表示该反应已经达到化学平衡状态的是___。
A.v逆(CH4)=2v正(CO)
B.CO2的浓度保持恒定
C.混合气体平均相对分子质量不变
D.混合气体密度保持不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阿魏酸在食品、医药等方面有着广泛用途。一种合成阿魏酸的反应可表示为


香兰素 丙二酸 阿魏酸
下列说法正确的是( )
A.可用酸性KMnO4溶液检测上述反应是否有阿魏酸生成
B.香兰素、阿魏酸均可与Na2CO3、NaOH溶液反应
C.通常条件下,香兰素、阿魏酸都能发生取代、加成、消去反应
D.与香兰素互为同分异构体,分子中有5种不同化学环境的氢,且能发生银镜反应的酚类化合物共有3种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】白磷与氧可发生如下反应:P4+5O2=P4O10。已知断裂下列化学键需要吸收的能量分别为:P—P akJ·mol—1、P—O bkJ·mol—1、P="O" ckJ·mol—1、O="O " dkJ·mol—1。

根据图示的分子结构和有关数据估算该反应的△H,其中正确的是( )
A. (6a+5d-4c-12b)kJ·mol—1B(4c+12b-6a-5d)kJ·mol—1 B. (4c+12b-4a-5d)kJ·mol—1
C. (4a+5d-4c-12b)kJ·mol—1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制备溴苯的反应装置如下图所示,关于实验操作或叙述错误的是
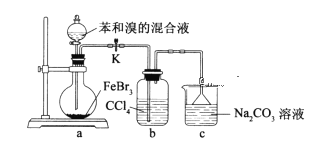
A.实验中装置b中的液体逐渐变为浅红色
B.装置c中的碳酸钠溶液的作用是吸收溴化氢
C.向圆底烧瓶中滴加苯和溴的混合液前需先打开K
D.反应后的混合液经稀碱溶液洗涤、结晶,得到溴苯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W是原子序数依次增大的四种短周期元素,A、B、C、D、F是由其中的两种或三种元素组成的化合物,E是由Z元素形成的单质,0.1molL-1 D溶液的pH为13(25℃)。它们满足如图转化关系,则下列说法正确的是

A. 由X、Y、Z、W四种元素组成的盐溶液pH小于7
B. 化合物F中含有共价键和离子键
C. 0.1molB与足量C完全反应共转移电子数为0.2NA
D. Z元素的最高正价为+6
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com