
【题目】右图三条曲线表示C、Si和P元素的四级电离能变化趋势。下列说法正确的是( )

A. 电负性:c>b>a B. 最简单氢化物的稳定性:c>a>b
C. I5:a>c>b D. 最简单氢化物的沸点:a>b>c
【答案】C
【解析】试题分析:A.根据碳、硅、磷元素的原子核外电子排布规律,结合其第一电离能可知:a是碳;b是磷;c是硅。A.元素的非金属越强,其电负性就越小,由于元素的非金属性:P>C>Si,所以元素的电负性:c<b<a,错误;B.元素的非金属性越强,其最简单氢化物的稳定性就越强。由于元素的非金属性:P>C>Si,所以最简单氢化物的稳定性c< a < b,错误;C.当碳原子失去第5个电子时形成的是1s1半充满的稳定结构,P元素形成的是2s22p6的全充满的稳定结构,而硅元素形成的是2s22p5的不稳定结构,所以元素的I5:a>c>b,正确;D.对于结构相似的物质来说,相对分子质量越大,分子间作用力越大,物质的熔点、沸点就越高。由于相对分子质量PH3>SiH4>CH4,所以最简单氢化物的沸点:b>c >a,错误。


 计算高手系列答案
计算高手系列答案科目:高中化学 来源: 题型:
【题目】判断下列有关化学基本概念的依据正确的是( )
A. 氧化还原反应:元素化合价是否变化.
B. 纯净物与混合物:是否仅含有一种元素
C. 电解质:溶液是否能导电
D. 溶液与胶体:本质不同的原因是能否发生丁达尔效应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下的5L的密闭固定容积容器中,通入10molNH3,发生了如下反应:N2+3H2![]() 2NH3,反应进行到2min时达到平衡状态,测得容器内有2molN2,求:
2NH3,反应进行到2min时达到平衡状态,测得容器内有2molN2,求:
(1)2min内的平均速率υ(NH3)?
(2)反应前后容器中气体压强之比?
(3)NH3的分解率?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碱性锌锰电池是日常生活中消耗量最大的电池, 其构造如图所示。放电时总反应为:Zn + 2H2O + 2MnO2==Zn(OH)2 + 2MnOOH 从废旧碱性锌锰电池中回收Zn和MnO2的工艺如下:
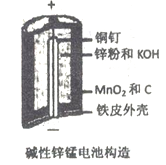
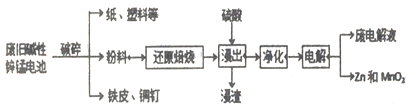
回答下列问题:
(1)“还原焙烧”过程中,高价金属化合物被还原为低价氧化物或金属单质(其中MnOOH、MnO2被还原成MnO),碳作为还原剂生成CO2,则CO2的电子式为___________。
(2)“净化”是为了除去浸出液中的Fe2+,方法是:加入______(填化学式)溶液将Fe2+氧化为Fe3+,再调节pH使Fe3+完全沉淀。己知浸出液中Mn2+、Zn2+的浓度约为0.1mol·L-1,根据下列数据计算,调节pH的合理范围是____至_______。
化合物 | Mn(OH)2 | Zn(OH)2 | Fe(OH)3 |
Ksp近似值 | 10-13 | 10-17 | 10-38 |
(离子浓度小于1×10-5 mol·L-1即为沉淀完全)
(3)“电解”时,阳极的电极反应式为______________。
本工艺中应循环利用的物质是____________(填化学式)。
(4)若将“粉料”直接与盐酸共热反应后过滤,滤液的主要成分是ZnCl2和MnCl2。“粉料”中的MnOOH与盐酸反应的化学方程式为___________________。
(5)某碱性锌锰电池维持电流强度0.5A (相当于毎秒通过5×10-6mol电子),连续工作80分钟即接近失效。如果制造一节电池所需的锌粉为6 g,则电池失效时仍有________%的金属锌未参加反应。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应:2CH3COCH3(l)![]() CH3COCH2COH(CH3)2(l)。取等量CH3COCH3,分别在0℃和20℃下,测得其转化分数(反应物已转化为产物的物质的量和反应物总物质的量的比)随时间变化的关系曲线(Y-t)如下图所示。下列说法正确的是
CH3COCH2COH(CH3)2(l)。取等量CH3COCH3,分别在0℃和20℃下,测得其转化分数(反应物已转化为产物的物质的量和反应物总物质的量的比)随时间变化的关系曲线(Y-t)如下图所示。下列说法正确的是

A. b代表0℃下CH3COCH3的Y-t曲线
B. 反应进行到20min末,CH3COCH3的v (0℃)/v(20℃)的比值大于1
C. 升高温度可以缩短反应达到平衡的时间并能提高反应物转化为生成物的物质的量
D. 从Y=0到Y=0.113,CH3COCH2COH(CH3)2的Δn(0℃)/Δn(20℃)的比值等于1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【2015上海卷】实验室回收废水中苯酚的过程如右图所示。下列分析错误的是( )
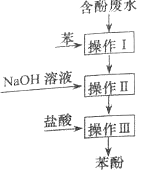
A.操作I中苯作萃取剂
B.苯酚钠在苯中的溶解度比在水中的大
C.通过操作II苯可循环使用
D.三步操作均需要分液漏斗
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【陕西省西安市长安区第一中学大学区2017届高三第三次联考理综】镍及其化合物用途广泛。某矿渣的主要成分是NiFe2O4(铁酸镍)、NiO、FeO、CaO、SiO2等,以下是从该矿渣中回收NiSO4的工艺路线:
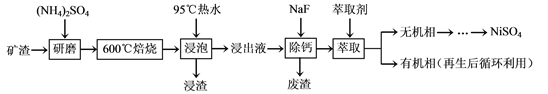
已知:(NH4)2SO4在350℃以上会分解生成NH3和H2SO4。NiFe2O4在焙烧过程中生成
NiSO4、Fe2(SO4)3。
锡(Sn)位于第五周期第ⅣA族。
(1)焙烧前将矿渣与(NH4)2SO4混合研磨,混合研磨的目的是__________________。
(2)“浸泡”过程中Fe2(SO4)3生成FeO(OH)的离子方程式为____________________。
“浸渣”的成分除Fe2O3、FeO(OH)外还含有________(填化学式)。
(3)为保证产品纯度,要检测“浸出液”的总铁量:取一定体积的浸出液,用盐酸酸化后,
加入SnCl2将Fe3+还原为Fe2+,所需SnCl2的物质的量不少于Fe3+物质的量的_______倍;
除去过量的SnCl2后,再用酸性K2Cr2O7标准溶液滴定溶液中的Fe2+,还原产物为Cr3+,滴定时反应的离子方程式为________________________。
(4)“浸出液”中c(Ca2+) = 1.0×10-3mol·L-1,当除钙率达到99%时,溶液中c(F-) = ________ mol·L-1。[已知Ksp (CaF2)=4.0×10-11]
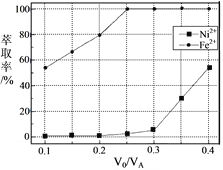
(5)本工艺中,萃取剂与溶液的体积比(V0/VA)对溶液中Ni2+、Fe2+的萃取率影响如下图所示,V0/VA的最佳取值是______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com