
����Ŀ���ԷϾ�Ǧ�����еĺ�Ǧ���ϣ�Pb��PbO��PbO2��PbSO4��̿�ڵȣ���H2SO4Ϊԭ�ϣ��Ʊ��ߴ�PbO��ʵ��Ǧ���������á��乤���������£�
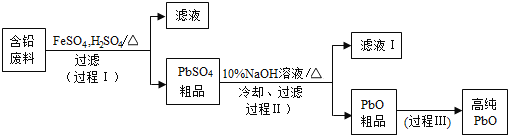
��1���������У���Fe2+���£�Pb��PbO2��Ӧ����PbSO4�Ļ�ѧ����ʽ��_________��
��2���������У�Fe2+�����̿ɱ�ʾΪ��
i��2Fe2++PbO2+4H++SO42-�T2Fe3++PbSO4+2H2O
ii������
��д��ii�����ӷ���ʽ��______________________��
������ʵ�鷽������֤���������̣���ʵ�鷽������������
a�����ữ��FeSO4��Һ�м���KSCN��Һ����Һ������ɫ���ټ�������PbO2����Һ��졣
b��____________��
��3��PbO�ܽ���NaOH��Һ�У����ܽ��������ͼ1��ʾ��

����������Ŀ����������Һ1����������ڹ��������ظ�ʹ�ã���Ŀ����___��ѡ����ţ���
A����СPbO����ʧ����߲�Ʒ�IJ���
B���ظ�����NaOH�����ԭ�ϵ�������
C������Na2SO4Ũ�ȣ��������Ч��
����������Ŀ�����ᴿ����������ܽ�����ߣ������������IJ�����_________��
���𰸡�Pb + PbO2+ 2H2SO4= 2PbSO4+ 2H2O2Fe3++Pb+SO42-�TPbSO4+2Fe2+ȡa�к�ɫ��Һ�������������Pb����ַ�Ӧ��ɫ��ȥA��B����PbO�ܽ���һ����35%NaOH��Һ�У�������110�棬����ܽ���ȹ��ˣ���ȴ�ᾧ�����ˣ�ϴ�ӣ�����õ�PbO����
��������
��1����Ϲ�������ͼ���������У���Fe2+���£�Pb��PbO2��Ӧ����PbSO4��ˮ����ѧ����ʽΪ�� Pb + PbO2+ 2H2SO4= 2PbSO4+ 2H2O ���𰸣� (1). Pb + PbO2+ 2H2SO4= 2PbSO4+ 2H2O
��2���������μӷ�Ӧ���ı䷴Ӧ���̣����ͷ�Ӧ��ܣ��ӿ췴Ӧ���ʣ��������������ͻ�ѧ�����ڷ�Ӧǰ�ֲ��䣬i��Fe2�� ������ΪFe3�� ��ii��Fe3������ԭ��Fe2�� �����ӷ���ʽ��2Fe3++Pb+SO42-�TPbSO4+2Fe2+ ���𰸣� (2). 2Fe3++Pb+SO42-�TPbSO4+2Fe2+
��ȡa�к�ɫ��Һ��������Һ�д���ƽ�⣬Fe3����SCN�D=Fe(SCN)3 �������Pb��Fe3�� ����ԭ��Fe2�� ��ƽ�������ƶ�����ַ�Ӧ��ɫ��ȥ ���𰸣� (3). ȡa�к�ɫ��Һ�������������Pb����ַ�Ӧ��ɫ��ȥ
��3������������������з����ķ�ӦΪPSO4��2NaOH=PbO��Na2SO4��H2O������PbO���ܽ���NaOH��Һ�������ҺI�к���PbԪ�أ��ظ�ʹ����ҺI�ɼ���PbO����ʧ������ҺI�й�����NaOH�����������ã����ԭ�ϵ������ʣ���ѡAB���𰸣�AB��
������PbO���ܽ�����ߣ��ᴿ��Pb�ķ����ǽ���PbO�ܽ���NaOH��Һ�У�����ܽ�����ߣ�NaOHŨ�ȸߡ��¶ȸߣ�PbO�ܽ�ȸߣ�����PbO�ܽ���һ����35%NaOH��Һ�У�������110�棬����ܽ���ȹ��ˣ���ȴ�ᾧ�����ˣ�ϴ�ӣ�����õ�PbO���壬�𰸣�����PbO�ܽ���һ����35%NaOH��Һ�У�������110�棬����ܽ���ȹ��ˣ���ȴ�ᾧ�����ˣ�ϴ�ӣ�����õ�PbO����



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����϶�һ�š�̽�³ɹ���ʵ�����й��˱��µ�����
��1�����϶�һ�š�ʹ�õ��ƽ�����Һ���Һ���������ƽ������ŵ��������������֮�⣬�����е��ŵ���_______________________��
��2��������298Kʱ��������H2����̼��C����������C8H18����������CH4��ȼ�յ��Ȼ�ѧ����ʽ��
H2��g����1/2O2��g��=H2O��l�� ��H����285.8 kJ/mol
C��g����O2��g��=CO2��g�� ��H����393.5 kJ/mol
C8H18��l����25/2O2��g��=8CO2��g����9H2O��l�� ��H����5518 kJ/mol
CH4��g����2O2��g��=CO2��g����2H2O��l�� ��H����890.3 kJ/mol
��ͬ������H2��C��C8H18��CH4��ȫȼ��ʱ���ų�����������________________��
��3����֪��H2��g��=H2��l�� ��H����0.92 kJ/mol
O2��g��=O2��l�� ��H����6.84 kJ/mol
H2O��l��=H2O��g�� ��H����44.0 kJ/mol
��д��Һ���Һ��������̬ˮ���Ȼ�ѧ����ʽ_______________������˴Ρ��϶�һ�š���Я����ȼ��Ϊ1.08�֣�Һ�⡢Һ��ǡ����ȫ��Ӧ������̬ˮ���ܹ��ͷ�����___________kJ������3λ��Ч��������
��4����������������ȼ��ʱ���ͷ����ܣ������γɵ�ԭ��ػ����ṩ���ܣ�������̽�·ɴ��������š�ʹ�õľ�������ȼ�ϵ�أ����ҺΪKOH��Һ�����ط�ӦΪ�������ŵ������Ϊ__________________��������__________________���ܷ�Ӧʽ��__________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʽΪC5H10O���ܷ���������Ӧ�����ʿ��ܵĽṹ��( )
A. 3�� B. 4�� C. 5�� D. 8��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ϡ�����Ũ������ķ����ǣ� ��
A.�ӷ�̪��Һ
B.��ͭƬ��Ӧ
C.��BaCl2��Һ������
D.�ò�������պһ�����ֽ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵������ȷ���� ( )
A��ʯ���ѽ����֬���������ɸ߷�������С���ӵĹ���
B����ϩ����������ԭ�Ӳ�������ͬһƽ����
C����CH3��3CCH2CH3��һ�ȴ�����3��
D���ױ�������������������ˮ����ɿ���ȡ����Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������ᷢչ�ij�Զǰ;��������Դ������õİ취�ǣ� ��
A.������̽�Ϳ���ʯ��
B.��������Ȼ����ʹ��ʯ��
C.��Ϊú�Ĵ�����ʯ�ͷḻ��Ӧ��ʹ��ú����Դ
D.������չ���ܡ����ܲ��������̫����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���߾����CH2��CH2��CH2�����������к������ʾۺϳɵģ� ��
A. CH3��CH3 B. CH3��CH2��CH3
C. CH2=CH2 D. CH2=CH��CH3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й��ڸ�ͼ��������ȷ����
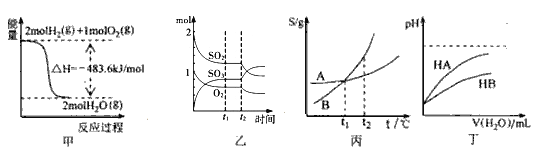
A. ͼ�ױ�ʾH2��O2������Ӧ�����е������仯����H2��ȼ����Ϊ241.8 kJmol-1
B. ͼ�ұ�ʾһ�������½��еķ�Ӧ2SO2+O2![]() 2SO3���ɷֵ����ʵ����仯��t2ʱ�̸ı������һ������С�������
2SO3���ɷֵ����ʵ����仯��t2ʱ�̸ı������һ������С�������
C. ͼ����ʾA��B�����ʵ��ܽ�����¶ȱ仯�������t1��ʱA��B�ı�����Һ�ֱ�������t2��ʱ�����ʵ�����������(B)>��(A)
D. ͼ����ʾ�����£�ϡ��HA��HB�������ϡ��Һʱ����ҺpH���ˮ���ı仯����NaA��Һ��pHС��ͬŨ�ȵ�NaB��Һ��pH
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ͬ����Ԫ�أ���ԭ�ӽṹ��֮ͬ���ǣ� ��
A.����������
B.�˵����
C.���Ӳ���
D.���������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com