
 2Z��g�� ��H<0��һ��ʱ���ﵽƽ�⣬��Ӧ�����вⶨ���������±���
2Z��g�� ��H<0��һ��ʱ���ﵽƽ�⣬��Ӧ�����вⶨ���������±���| t��min | 2 | 4 | 7 | 9 |
| n�� Y����mol | 0.12 | 0.11 | 0.10 | 0.10 |
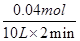 =0.002mol/��L��min��������֮�ȵ��ڻ�ѧ������֮�ȣ���v��Z��=2v��Y��=2��0.002mol/��L��min��=0.004mol/��L��min������A���÷�Ӧ����Ӧ�Ƿ��ȷ�Ӧ�������¶�ƽ��������Ӧ�ƶ�����Ӧ�ﵽ��ƽ��ǰv���棩��v����������B�����ɱ������ݿ�֪7minʱ����Ӧ����ƽ�⣬ƽ��ʱY�����ʵ���Ϊ0.10mol����
=0.002mol/��L��min��������֮�ȵ��ڻ�ѧ������֮�ȣ���v��Z��=2v��Y��=2��0.002mol/��L��min��=0.004mol/��L��min������A���÷�Ӧ����Ӧ�Ƿ��ȷ�Ӧ�������¶�ƽ��������Ӧ�ƶ�����Ӧ�ﵽ��ƽ��ǰv���棩��v����������B�����ɱ������ݿ�֪7minʱ����Ӧ����ƽ�⣬ƽ��ʱY�����ʵ���Ϊ0.10mol���� 2Z��g��
2Z��g��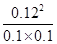 =1.44����C��ȷ����ͨ��0.2 mol Z����ЧΪ��ԭƽ�����������ѹǿ����Ӧǰ�������������䣬ƽ�ⲻ�ƶ���X������������䣬��D��������ѡC��
=1.44����C��ȷ����ͨ��0.2 mol Z����ЧΪ��ԭƽ�����������ѹǿ����Ӧǰ�������������䣬ƽ�ⲻ�ƶ���X������������䣬��D��������ѡC��

 ���Ŀ��ּ�����ҵ�����ҵ����������ϵ�д�
���Ŀ��ּ�����ҵ�����ҵ����������ϵ�д� ����ѵ��ϵ�д�
����ѵ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��������A��ʾ2s�ڵ�ƽ����Ӧ����Ϊ0.3mol/��L?s�� |
| B��������B��ʾ2 s�ڵ�ƽ����Ӧ����Ϊ0.6mol/��L?s�� |
| C��2s������A��ת����Ϊ70% |
| D��2s������B��Ũ��Ϊ0.35mol/L |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
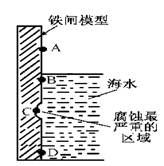
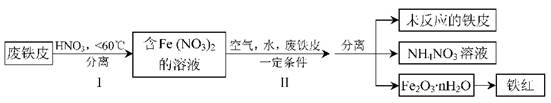
 Fe(s)��CO2(g)��ƽ�ⳣ��K��0.25��
Fe(s)��CO2(g)��ƽ�ⳣ��K��0.25���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��

A��ͼ1��ʾ���º�ѹ����������2HI  H2 + I2 ��H>0�ķ�Ӧ�ﵽƽ��������г���HI���ױ�ʾ����Ӧ���ʣ��ұ�ʾ�淴Ӧ���� H2 + I2 ��H>0�ķ�Ӧ�ﵽƽ��������г���HI���ױ�ʾ����Ӧ���ʣ��ұ�ʾ�淴Ӧ���� |
B��ͼ1��ʾ��������������2HI  H2 + I2 ��H>0�� ��Ӧ�ﵽƽ����������ȣ��ױ�ʾ����Ӧ���ʣ��ұ�ʾ�淴Ӧ���� H2 + I2 ��H>0�� ��Ӧ�ﵽƽ����������ȣ��ױ�ʾ����Ӧ���ʣ��ұ�ʾ�淴Ӧ���� |
C��ͼ2��ʾ���������£�ѹ��2SO3(g) 2SO2(g)��O2(g) ��H>0ƽ�ⷴӦ��ϵ���ױ�ʾ��SO3���ʵ����ı仯���ұ�ʾ��SO3���ʵ���Ũ�ȵı仯 2SO2(g)��O2(g) ��H>0ƽ�ⷴӦ��ϵ���ױ�ʾ��SO3���ʵ����ı仯���ұ�ʾ��SO3���ʵ���Ũ�ȵı仯 |
D��ͼ2��ʾ���������£�����2SO3(g) 2SO2(g)��O2(g) ��H>0��Ӧƽ����ϵ���ױ�ʾ�����¶�SO3���ʵ����ı仯���ұ�ʾ����O2��SO3���ʵ����仯 2SO2(g)��O2(g) ��H>0��Ӧƽ����ϵ���ױ�ʾ�����¶�SO3���ʵ����ı仯���ұ�ʾ����O2��SO3���ʵ����仯 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2SO3��g�����Ʊ��������Ҫ��Ӧ������������ȷ���ǣ� ��
2SO3��g�����Ʊ��������Ҫ��Ӧ������������ȷ���ǣ� ��| A������V2O5���ı�÷�Ӧ���淴Ӧ���� |
| B�����߷�Ӧ��ϵ���¶ȣ���Ӧ����һ������ |
| C����÷�Ӧ�Ƿ��ȷ�Ӧ�����Խ����¶Ƚ����̷�Ӧ�ﵽƽ���ʱ�� |
D����t1��t2ʱ�̣�O2��g����Ũ�ȷֱ���c1��c2����ʱ����t1��t2�ڣ�SO3��g�����ɵ�ƽ������Ϊv�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 H2��+I2
H2��+I2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2SO3��g������H<0��n��SO2����ʱ��ı仯�����
2SO3��g������H<0��n��SO2����ʱ��ı仯�����| ʱ��/min | 0 | 1 | 2 | 3 | 4 | 5 |
| n��SO2��/mol | 0.20 | 0.16 | 0.13 | 0.11 | 0.08 | 0.08 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 CO2 (g) + H2(g) ��H��Q kJ/mol ����֪�÷�Ӧ��ƽ�ⳣ��K���¶�T�Ĺ�ϵ��ͼ��ʾ������һ�̶����ܱ������У� 850�� ʱ����������Ӧ����������ڸ����ʵ�Ũ�� (mol/L)��ʱ��ı仯��ϵ���±���
CO2 (g) + H2(g) ��H��Q kJ/mol ����֪�÷�Ӧ��ƽ�ⳣ��K���¶�T�Ĺ�ϵ��ͼ��ʾ������һ�̶����ܱ������У� 850�� ʱ����������Ӧ����������ڸ����ʵ�Ũ�� (mol/L)��ʱ��ı仯��ϵ���±���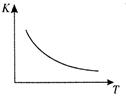

| A����λʱ���ڼ��� CO(g)��Ũ�ȵ������� CO2 (g)��Ũ�� |
| B����Ӧ�����ڵ�ѹǿ�������仯 |
| C����������� H2 (g)��Ũ�Ȳ��ٷ����ı� |
| D���������������ʵ���ˮ���������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2C(g) ��H < 0��t1ʱ�̴ﵽƽ�����t2ʱ�̸ı�ijһ�������䷴Ӧ������ͼ������˵����ȷ����
2C(g) ��H < 0��t1ʱ�̴ﵽƽ�����t2ʱ�̸ı�ijһ�������䷴Ӧ������ͼ������˵����ȷ����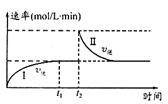
| A��0��t2ʱ��v��>v�� |
| B���������̴ﵽƽ��ʱ��A�����������>�� |
| C��t2ʱ�̸ı���������������ܱ������м�C |
| D���������̴ﵽƽ��ʱ��ƽ�ⳣ��I<�� |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com