
【题目】下列依据实验方案和现象对浓硫酸性质做出的判断合理的是
实验方案 | 实验I: | 实验II: |
实验现象 | 试纸中心区域变黑,边缘变红 | 黑色固体溶解,溶液接近无色(溶液中锰元素仅以 |
A.由I可知,浓硫酸具有脱水性B.由I可知,浓硫酸具有弱酸性
C.由II可知,浓硫酸具有强氧化性D.由II可知,浓硫酸具有吸水性
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】干洗衣服的干洗剂主要成分是四氯乙烯,家用不粘锅内侧涂覆物质的主要成分是聚四氟乙烯(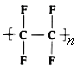 )。下列关于四氯乙烯和聚四氟乙烯的说法正确的是
)。下列关于四氯乙烯和聚四氟乙烯的说法正确的是
A.均为纯净物
B.都能发生加成反应,都能使酸性高锰酸钾溶液褪色
C.都属于不饱和烃,分子中都不含氢原子
D.四氯乙烯对油脂有较好的溶解作用,聚四氟乙烯的化学性质比较稳定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,相同pH的盐酸和醋酸溶液分别加水稀释,平衡时pH随溶液体积变化的曲线如图所示。据图判断不正确的是( )
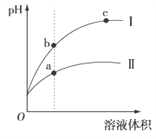
A. I是盐酸,Ⅱ是醋酸
B. 稀释前等体积的I、Ⅱ溶液中和氢氧化钠的能力相同
C. a、b、c三点KW的数值相同
D. 溶液的导电性a>b>c
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把1 mol CH4 和一定量Cl2组成的混合气体通入大试管中,将此试管倒立在盛有饱和食盐水的水槽中,放在光亮处,回答下列问题:

(1)片刻后试管中的现象为:
①试管内气体的颜色变浅,②试管壁上出现_________________________、③试管内__________________、____________________。
(2)在反应结束后,试管内的产物最多的是___________,空间构型呈正四面体的产物为___________。
(3)若(2)中生成的四种有机产物的物质的量相同,则反应消耗的Cl2的物质的量为________mol。
(4)与CH4相邻同系物的结构简式为_______________该同系物与Cl2发生一氯取代反应的化学方程式为__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】相对分子质量为Mr的气态化合物V L(标准状况)溶于mg水中,得到溶液的质量分数为w%,物质的量浓度为cmol·L-1,密度为ρg·cm-3,则下列说法不正确的是( )
A.溶液密度ρ可表示为![]()
B.物质的量浓度c可表示为![]()
C.溶液的质量分数w%可表示为![]()
D.相对分子质量Mr可表示为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)已知反应2HI(g)=H2(g)+I2(g)的△H=+11kJ·mol-1,1molH2(g)、1molI2(g)分子中化学键断裂时分别需要吸收436kJ、151kJ的能量,则1molHI(g)分子中化学键断裂时需吸收的能量为______________kJ。
(2)已知某密闭容器中存在下列平衡:CO(g)+H2O(g)![]() CO2(g)+H2(g),CO的平衡物质的量浓度c(CO)与温度T的关系如图所示。
CO2(g)+H2(g),CO的平衡物质的量浓度c(CO)与温度T的关系如图所示。
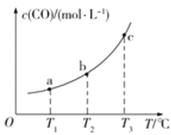
①该反应△H_____________0(填“>”或“<”)
②若T1、T2时的平衡常数分别为K1、K2,则K1_____________K2(填“>”、“<”或“=”)。
(3)在恒容密闭容器中,加入足量的MoS2和O2,仅发生反应:2MoS2(s)+7O2(g)![]() 2MoO3(s)+4SO2(g)ΔH。测得氧气的平衡转化率与起始压强、温度的关系如图所示:
2MoO3(s)+4SO2(g)ΔH。测得氧气的平衡转化率与起始压强、温度的关系如图所示:
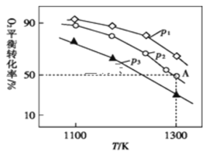
①p1、p2、p3的大小:___________。
②若初始时通入7.0molO2,p2为7.0kPa,则A点平衡常数Kp=___________(用气体平衡分压代替气体平衡浓度计算,分压=总压×气体的物质的量分数,写出计算式即可)。
(4)中科院兰州化学物理研究所用Fe3(CO)12/ZSM-5催化CO2加氢合成低碳烯烃反应,所得产物含CH4、C3H6、C4H8等副产物,反应过程如图。
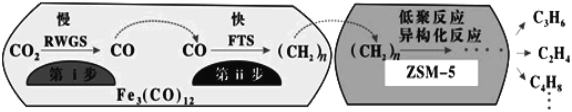
催化剂中添加Na、K、Cu助剂后(助剂也起催化作用)可改变反应的选择性,在其他条件相同时,添加不同助剂,经过相同时间后测得CO2转化率和各产物的物质的量分数如表。
助剂 | CO2转化率(%) | 各产物在所有产物中的占比(%) | ||
C2H4 | C3H6 | 其他 | ||
Na | 42.5 | 35.9 | 39.6 | 24.5 |
K | 27.2 | 75.6 | 22.8 | 1.6 |
Cu | 9.8 | 80.7 | 12.5 | 6.8 |
①欲提高单位时间内乙烯的产量,在Fe3(CO)12/ZSM-5中添加_______助剂效果最好;加入助剂能提高单位时间内乙烯产量的根本原因是:___________
②下列说法正确的是______;
a.第ⅰ步的反应为:CO2+H2![]() CO+H2O
CO+H2O
b.第ⅰ步反应的活化能低于第ⅱ步
c.催化剂助剂主要在低聚反应、异构化反应环节起作用
d.Fe3(CO)12/ZSM-5使CO2加氢合成低碳烯烃的ΔH减小
e.添加不同助剂后,反应的平衡常数各不相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A.电解水时氢气与氧气的体积比为2:1,原因是气体的体积主要取决于分子间距,而同温同压时气体的间距基本相等
B.碳酸分步电离以第一步为主,第二步为次,原因之一是第二步电离时碳酸氢根带负电荷,而电离出的氢离子为正电荷
C.苯酚显弱酸性可与氢氧化钠溶液反应,是因为羟基活化了苯环
D.可通过如图(比例模型)判定醋酸是弱电解质
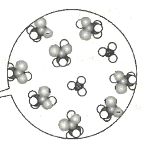
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向两只分别盛有50 mL0.100 mol/L盐酸的烧杯中各自匀速滴加50 mL蒸馏水、50 mL0.100 mol/L醋酸铵溶液,装置如图所示(夹持仪器等已略)。
已知:常温下,CH3COONH4溶液pH约为7。
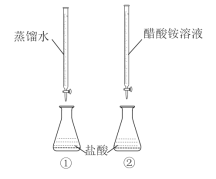
下列说法正确的是( )
A.实验①滴加过程中溶液所有离子浓度都减小
B.实验②滴至pH=2时,溶液中c(Cl-)+c(CH3COO-)+c(OH-)=0.01 mol/L
C.实验②滴加过程中,溶液中均存在c(CH3COO-)<c(NH4+)
D.滴定结束后,①中水的电离程度比②中大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是___(填序号)。
①将1 mol NaCl溶解在1 L水中,可得1 mol·L-1NaCl的溶液
②将11.2 L HCl气体通入水配成0.5 L溶液,得到1 mol·L-1的盐酸
③1 L 10 mol·L-1的盐酸与9 L水混合,得到1 mol·L-1的盐酸
④将0.4 g NaOH溶解水中形成100 mL溶液,从中取出10 mL,所取溶液物质的量浓度为0.1 mol·L-1(不考虑溶液体积的变化)
⑤将1 mol Na2O溶于水配成1 L溶液,所得溶质的物质的量浓度为1 mol·L-1(不考虑溶液体积的变化)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com