
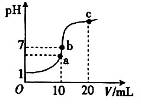
| A.在b点,盐酸与氨水恰好完全中和 |
| B.在b点:c(H+)=c(OH-),c(NH4+)=c(Cl-) |
| C.在a点:c(Cl-)> c(NH4+)> c(H+)> c(OH-) |
| D.在c点:c(NH4+)+ c(NH3·H2O)="2" c(Cl-) |
 计算高手系列答案
计算高手系列答案科目:高中化学 来源:不详 题型:单选题
| A.含有H+离子的溶液 | B.c(OH-)=1×10-8mol/L的溶液 |
| C.c(OH-)<c(H+)的溶液 | D.pH小于7的溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.a=b | B.a>b | C.c(A-)= c(Na+) | D.c (A-)< c(Na+) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.将pH=2的盐酸和pH=2的醋酸等体积混合,混合后溶液的pH=2 |
| B.HA-比HB-更难电离,则NaHA溶液的pH一定比NaHB溶液的大 |
| C.在饱和氨水中加入同浓度的氨水,平衡正向移动 |
| D.某温度下,Ba(OH)2溶液中,Kw=10-12,pH=8的该溶液中加入等体积pH=4的盐酸,混合溶液的pH=7 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.H2O2的电子式为 |
| B.4℃时,纯水的pH<7,溶液呈中性 |
| C.0℃、101kPa,水分子间距:固态>液态 |
| D.101kPa,不同状态水的能量:固态>液态>气态 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
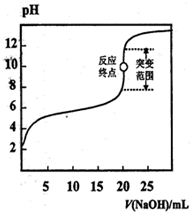
| A.可用甲基橙作滴定指示剂 |
| B.指示剂指示的滴定终点就是反应终点 |
| C.突变范围的大小与酸的强弱及酸的浓度有关 |
| D.滴定时氢氧化钠溶液盛放在带活塞的滴定管中 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.c(H+)+c(NH4+)=c(OH-) |
| B.与等体积等浓度的氯化铵溶液混合c(NH4+)+c(NH3· H2O)="0.02" mol·L-1 |
| C.与等体积等浓度的盐酸混合后所得溶液显酸性 |
| D.由H2O电离出的c(H+)=1.0×10-12 mol·L-1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.Ⅱ为氯化铵稀释时pH值变化曲线,a点水的电离程度大于c点水的电离程度 |
| B.b点溶液中水的电离程度比c点溶液中水的电离程度大,且两点的KW相同 |
| C.a点时,等体积的两溶液与NaOH反应消耗的NaOH量相同 |
| D.加入足量NaOH,b点溶液消耗的NaOH比d点溶液消耗的多 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.在25℃和80℃时纯水中的c(H+)浓度 |
| B.室温时,浓度均为 0.1mol/L的(NH4)2SO4(aq)、(NH4) 2CO3 (aq)的c(NH4+) |
| C.25℃时,pH均为3的HCl和NH4Cl溶液中水的电离程度 |
| D.1 L饱和氯化铵溶液中NH4+和Cl- 的个数 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com