
【题目】将氯化铜、氯化铝、氯化亚铁、氯化铁、氯化镁五种无色溶液,通过一种试剂就能鉴别,这种试剂是( )
A.KSCN
B.BaCl2
C.HCl
D.NaOH
 口算能手系列答案
口算能手系列答案科目:高中化学 来源: 题型:
【题目】已知常温下:Ksp(AgCl)=1.6×10-10,下列叙述正确的是 ( )
A.AgCl在饱和NaCl溶液中的Ksp比在纯水中的小
B.AgCl的悬浊液中c(Cl-)=4×10-5.5mol/L
C.将0.001 mol·L-1AgNO3溶液滴入0.001 mol·L-1的KCl,无沉淀析出
D.向AgCl的悬浊液中加入NaBr溶液,白色沉淀转化为淡黄色,说明Ksp(AgCl)<Ksp(AgBr)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解质溶液的电导率越大,导电能力越强。用0.100mol·L-1的NaOH溶液分别滴定10.00mL 浓度均为0.100mol·L-1的盐酸和CH3COOH溶液。利用传感器测得滴定过程中溶液电导率如图所示。下列说法不正确的是( )
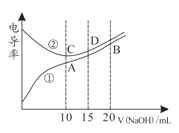
A.曲线①代表滴定CH3COOH溶液的曲线
B.在相同温度下,A、B、C 三点溶液中水电离的 c(H+):B<A=C
C.D点溶液中:c(Cl-)=2c(OH-)-2c(H+)
D.A点溶液中:c(CH3COO-)+c(OH-)-c(H+) = 0.05mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CaS可用于制备发光漆、用作脱毛剂、杀虫剂、硫脲等,还用于医药工业、重金属处理及环保中。某化学探究小组在实验室中利用反应:
CaSO4+C![]() CaS+CaO+SO2↑+CO↑+CO2↑制备硫化钙并检验产物,可选用的装置如下。回答下列问题:
CaS+CaO+SO2↑+CO↑+CO2↑制备硫化钙并检验产物,可选用的装置如下。回答下列问题:

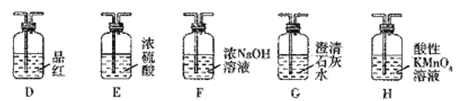
已知:①C及E ~ H中的试剂均为足量。
②酸性KMnO4溶液作氧化剂时,锰元素被还原成Mn2+
③CaS与H2O反应生成Ca(OH)2和H2S。
(1)实验1:若只检验生成物中是否含有CO,可采用的装置组合为______(按气流方向,填字母组合),生成物中存在CO的现象是________________________。
(2)实验2:若只检验生成物中是否含有CO2,可釆用的最简单的装置组合为______(按气流方向,填字母组合),除去SO2的离子方程式为__________________________。
(3)实验3:若同时检验CO2和SO2,采用的装置组合为_______ (按气流方向,填字母组合)。
(4)若制备反应的条件完全相同,将产生的气体全部通入上述实验装置中,得到的有关数据如下表:
实验前 | 实验后 | |
实验1 | 装置C硬质玻璃管连同CuO质量为26.80 g | 装置C硬质玻璃管连同反应后固体质量为26.64 g |
实验2 | 装置G连同溶液质量为187.50g | 装置G连同反应后溶液及沉淀的质量为188.38 g |
实验3 | 装置D、H连同溶液质量和为373.60g | 装置D、H连同溶液质量和为374.24 g |
写出CaSO4和焦炭在高温条件下反应生成CaS的化学方程式:_______________。
(5)为了证明硫化钙的化学式设计如下实验:将一定质量(m1)的样品溶于足量的饱和Na2CO3溶液中,通过____操作,称得固体质量为m2,则表示硫化钙组成的计算式为n(Ca):n(S)=__________(用含m1 、m2的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一学生用如图装置研究原电池原理,下列说法错误的是:

A. (3)图中Zn片增重质量与Cu棒减轻质量的比值为65:64
B. (2)图中如果两极上都有气体产生,则说明Zn片不纯
C. (1)图中铜棒上没有气体产生
D. (2)图与(3)图中正极生成物质质量比为1:32时,Zn棒减轻的质量相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,容积为 1L 的密闭容器中发生反应: SiF4(g)+2H2O(g) ![]() SiO2(s)+4HF(g)。下列各项中不能说明该反应已达化学平衡状态的是( )
SiO2(s)+4HF(g)。下列各项中不能说明该反应已达化学平衡状态的是( )
A.v(SiF4)消耗=4v(HF)生成 B.HF 的体积分数不再变化
C.容器内气体压强不再变化 D.容器内气体总质量不再变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三盐(3PbO·PbSO4·H2O)可用作聚氯乙烯的热稳定剂,200℃以上开始失去结晶水,不溶于水及有机溶剂。以200.0t铅泥(主要成分为PbO、Pb及PbSO4等)为原料制备三盐的工艺流程如图所示。

已知:PbSO4和PbCO3的溶解度和溶度积Ksp如下表。

(1)步骤①转化的目的是_______,滤液1中的溶质为Na2CO3和_______(填化学式)。
(2)步骤③酸溶时,为提高酸溶速率,可采取的措施是_________(任写一条)。其中铅与硝酸反应生成Pb(NO3)2和NO的离子方程式为__________________。
(3)滤液2中可循环利用的溶质的化学式为_______。若步骤④沉铅后的滤液中c(Pb2+)=1.82×10-5mol/L,则此时c(SO42-)=______mol/L。
(4)步骤⑦洗涤操作时,检验沉淀是否洗涤完全的方法是________________。
(5)步骤⑥合成三盐的化学方程式为____________,若得到纯净干燥的三盐99.Ot,假设铅泥中的铅元素有80%转化为三盐,则铅泥中铅元素的质量分数为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、X、Y和Z是原子序数依次递增的短周期元素,其中A与Y同主族,X与Z同主族,A与B和X均可形成10个电子的化合物;B与Z的最外层电子数之比为 2:3,常见化合物Y2X2与水反应生成X的单质,其水溶液可使酚酞试液变红。请回答下列问题:
(1)Z的原子结构示意图为___________________________;
(2)化合物Y2X2中含有的化学键类型有____________(填序号)。
A.离子键 B.极性共价键 C.非极性键 D.氢键
(3)A与X和A与Z均能形成18个电子的化合物,此两种化合物发生反应的化学方程式为: ______________________________________________。
(4)将Z与X形成的气态化合物ZX2通入Ba(NO3)2溶液中,有白色沉淀和一氧化氮气体生成,发生反应的离子方程式为:___________________________________________。
(5)由BA4、X2、YXA溶液可以组成原电池,则组成该原电池的负极反应式为:_____________________,
原电池工作一段时间后,整个溶液的pH将__________(填“增大”、“不变”或“减小”)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com