
【题目】氧化亚铜常用于制船底防污漆。用CuO与Cu高温烧结也可制取Cu2O。已知反应:
①2Cu(s) + O2(g) = 2CuO(s) ΔH = 314 kJ/mol
②2Cu2O(s) + O2(g) = 4CuO(s) ΔH = 292 kJ/mol
则反应CuO(s) 与Cu(s) 反应生成Cu2O(s) 的热化学方程式是( )
A.CuO(s) + Cu(s) = Cu2O(s) ΔH = 22 kJ/mol
B.CuO(s) + Cu(s) = Cu2O(s) ΔH = +22 kJ/mol
C.CuO(s) + Cu(s) = Cu2O(s) ΔH = 11 kJ/mol
D.CuO(s) + Cu(s) = Cu2O(s) ΔH = +11 kJ/mol
 优生乐园系列答案
优生乐园系列答案科目:高中化学 来源: 题型:
【题目】(1)已知NaHA水溶液呈碱性。
①用离子方程式表示NaHA水溶液呈碱性的原因__________________(用离子方程式和相应的文字叙述)。
②在NaHA水溶液中各离子浓度的大小关系是_______________________________
(2)实验室在配制AlCl3的溶液时,为了抑制AlCl3的水解可加入少量的_____(填写物质的名称)。把AlCl3溶液蒸干,灼烧,最后得到的主要固体产物是________(填化学式)。
(3)常温下,物质的量浓度相同的下列溶液:①NH4Cl、②(NH4)2SO4、③NH3·H2O、④(NH4)2CO3、⑤NH4HSO4。溶液中c(![]() )从大到小顺序为__________________(填序号)。
)从大到小顺序为__________________(填序号)。
(4)常温下,pH=5的盐酸和pH=9的氢氧化钠溶液等体积混合,则混合液的pH=_________。
(5)毒重石的主要成分BaCO3(含Ca2+、Mg2+、Fe3+等杂质),实验室利用毒重石制备BaCl2·2H2O的流程如下:

已知:
Ca2+ | Mg2+ | Fe3+ | |
开始沉淀时的pH | 11.9 | 9.1 | 1.9 |
完全沉淀时的pH | 13.9 | 11.1 | 3.2 |
已知:Ksp(BaC2O4)=1.6×10-7,Ksp(CaC2O4)=2.3×10-9
加入NH3·H2O调pH=8可除去______(填离子符号),滤渣Ⅱ中含________(填化学式)。加入H2C2O4时应避免过量,原因是__________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】不同温度下,水溶液中c(H+)与 c(OH+)的关系如图所示,下列说法正确的是

A.若从a点到c点,可采用在水中加入酸的方法
B.b点对应的醋酸中由水电离的c(H+)=10-6mol·L-1
C.T ℃时,0.05 mol·L-1的Ba(OH)2溶液的pH=11
D.c点对应溶液的Kw大于d点对应溶液的Kw
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某矿石主要成分有磁铁矿(Fe3O4)、锰矿(MnO2和MnCO3)、氧化铝(Al2O3)、石棉Mg3Si3O7(OH)4等。其中锰矿含量大于磁铁矿含量。工业上将该矿石处理后提取铝的工业流程如下:

已知:二氧化锰难溶于水、稀硫酸,溶于热浓盐酸。碳酸锰不溶于水,溶于稀硫酸。
(1)MnO2和MnCO3中,Mn元素的化合价分别是_________。
(2)石棉化学式为Mg3Si3O7(OH)4,它与硫酸反应的化学方程式为_________。
(3)滤渣A为____________(填化学式)
(4)步骤②中加入氢氧化钠的作用是_________。
(5)已知不同金属离子生成氢氧化物沉淀所需的pH如表:
离子 | Fe3+ | Al3+ | Fe2+ | Mg2+ | Mn2+ |
开始沉淀的pH | 2.7 | 3.7 | 7.0 | 9.3 | 7.8 |
完全沉淀的pH | 3.7 | 4.7 | 9.6 | 10.8 | 9.8 |
步骤②中加入氢氧化钠调节溶液的pH等于11,则滤渣B的成份是________。
(6)步骤③是往滤液中加入一种物质后过滤,这种物质是__________,过滤操作中使用的玻璃仪器有漏斗、_________;由D电解制备铝的化学方程式为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知乙醇在浓硫酸作用下迅速加热到170 ℃时分子内脱水可制备乙烯,反应如下:

加热到140 ℃时产生一种副产物乙醚.反应装置如图所示,试回答下列问题:

(1)检查装置气密性的方法是________________,A仪器的名称是________.
(2)A中加入试剂的顺序是_____________________,A中加入碎瓷片的作用是___________.
(3)反应中除产生副产物乙醚外,在收集到的乙烯气体中混有SO2,设计实验除去SO2:___________.
(4)乙烯能被酸性高锰酸钾溶液氧化成甲酸(HCOOH),写出反应的化学方程式:__________________;若反应中有0.42 g乙烯被氧化,则反应中转移电子的数目为_____________________________.
(5)乙烯在农业生产实践中的应用是_________________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】依据氧化还原反应:2Ag+(aq)+Cu(s)![]() Cu2+(aq)+2Ag(s)设计的原电池如图所示。
Cu2+(aq)+2Ag(s)设计的原电池如图所示。
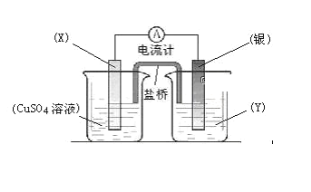
请回答下列问题:
(1)电极X的材料是_______;电解质溶液Y是____________;
(2)银电极为电池的___极,发生的电极反应为_____________;X电极上发生的电极反应为___________;
(3)外电路中的电子是从_______电极流向___________电极;
(4)如图所示,a、b、c均为石墨电极,d为碳钢电极,通电进行电解。假设在电解过程中产生的气体全部逸出,则
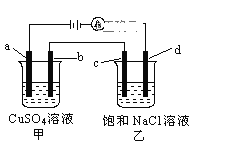
①a电极反应式为_________________________________;
②乙中的总反应为__________________________________;
③若整个电路中有2NA 个电子转移,则d电极产生__________L气体 (标准状况)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究表明,氮氧化物和二氧化硫在形成雾霾时与大气中的氨有关(如下图所示)。下列叙述错误的是

A. 雾和霾的分散剂相同
B. 雾霾中含有硝酸铵和硫酸铵
C. NH3是形成无机颗粒物的催化剂
D. 雾霾的形成与过度施用氮肥有关
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】秸秆(含多糖类物质)的综合利用具有重要的意义。下面是以秸秆为原料合成聚酯类高分子化合物的路线:

回答下列问题:
(1)下列关于糖类的说法正确的是___。(填标号)
a.糖类都有甜味,具有CnH2mOm的通式
b.麦芽糖水解生成互为同分异构体的葡萄糖和果糖
c.用银镜反应不能判断淀粉水解是否完全
d.淀粉和纤维素都属于多糖类天然高分子化合物
(2)B生成C的反应类型为___。
(3)D中的官能团名称为___,D生成E的反应类型为___。
(4)F 的化学名称是___,由F生成G的化学方程式为____。
(5)具有一种官能团的二取代芳香化合物W是E的同分异构体,0.5molW与足量碳酸氢钠溶液反应生成44gCO2,W共有____种(不含立体异构),其中核磁共振氢谱为三组峰的结构简式为____。
(6)参照上述合成路线,以(反,反)2,4己二烯和C2H4为原料(无机试剂任选),设计制备对苯二甲酸的合成路线____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氯化二硫(S2Cl2)是一种重要的化工原料,常用作橡胶硫化剂,改变生橡胶受热发粘、遇冷变硬的性质。查阅资料可知S2Cl2具有下列性质:
物理性质 | 毒性 | 色态 | 挥发性 | 熔点 | 沸点 |
剧毒 | 金黄色液体 | 易挥发 | -76℃ | 138℃ | |
化学性质 | ①300℃以上完全分解; ②S2Cl2+Cl2 ③遇高热或与明火接触,有引起燃烧的危险; ④受热或遇水分解放热,放出腐蚀性烟气; | ||||
(1)制取少量S2Cl2
实验室可利用硫与少量氯气在110~140℃反应制得S2Cl2粗品。
①仪器m的名称为___,装置F中试剂的作用是___。
②装置连接顺序:A→___→E→D。
③实验前打开K1,通入一段时间的氮气排尽装置内空气。实验结束停止加热后,再通入一段时间的氮气,其目的是___。
④为了提高S2Cl2的纯度,实验的关键是控制好温度和___。
(2)①S2Cl2遇水强烈反应产生烟雾,其产物中有一种气体X能使品红溶液褪色,加热后又恢复原状,且反应过程中只有一种元素化合价发生变化,写出该反应的化学方程式___。
②甲同学为了验证两种气体产物,将水解生成的气体依次通过硝酸银与稀硝酸的混合溶液、品红溶液、NaOH 溶液,该方案___(填“可行”或“不可行”),原因是___。
(3)某同学为了测定S2Cl2与水反应后生成的气体X在混合气体中的体积分数,设计了如下实验方案:

①W溶液可以是___(填标号)。
a.H2O2溶液 b.KMnO4溶液(硫酸酸化) c.氯水
②该混合气体中气体X的体积分数为____(用含V、m的式子表示)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com