
【题目】已知乙醇在浓硫酸作用下迅速加热到170 ℃时分子内脱水可制备乙烯,反应如下:

加热到140 ℃时产生一种副产物乙醚.反应装置如图所示,试回答下列问题:

(1)检查装置气密性的方法是________________,A仪器的名称是________.
(2)A中加入试剂的顺序是_____________________,A中加入碎瓷片的作用是___________.
(3)反应中除产生副产物乙醚外,在收集到的乙烯气体中混有SO2,设计实验除去SO2:___________.
(4)乙烯能被酸性高锰酸钾溶液氧化成甲酸(HCOOH),写出反应的化学方程式:__________________;若反应中有0.42 g乙烯被氧化,则反应中转移电子的数目为_____________________________.
(5)乙烯在农业生产实践中的应用是_________________________.
【答案】将长导管末端插入水中,用热毛巾包住圆底烧瓶底部,若导管口产生气泡,撤去热毛巾会有一段液柱倒吸入导管中,说明装置气密性良好 圆底烧瓶 先加入乙醇再加入浓硫酸 防止暴沸 收集乙烯装置之前连接盛氢氧化钠溶液的洗气瓶 5CH2=CH2+8KMnO4+12H2SO4=10HCOOH+8MnSO4+4K2SO4+12H2O 0.12NA 水果的催熟剂或植物生长调节剂
【解析】
(1)将导管的另一端插入水中,然后用热毛巾捂住圆底烧瓶底部,观察是否有气泡产生;根据仪器A的构造完成A的命名;
(2)浓硫酸稀释过程中放出热量,浓硫酸密度大于水的密度,据此进行分析加入试剂顺序;根据混合液体在加热时容易发生暴沸进行分析;
(3)根据乙烯与二氧化硫的性质选用试剂除去二氧化硫;
(4)根据化合价升降相等配平乙烯与酸性高锰酸钾溶液的反应方程式,根据配平的方程式及化合价变化计算出转移的电子数;
(5)根据乙烯在农业生产实践中的应用进行解答。
(1)检查装置气密性的方法为将长导管末端插入水中,用热毛巾包住圆底烧瓶底部,若导管口产生气泡,拿开热毛巾一段时间后导管内有一段水柱,说明装置气密性良好;
根据仪器的构造可知,A仪器的名称是圆底烧瓶;
(2)浓硫酸密度较大,稀释过程中放出大量的热量,所以应该将浓硫酸慢慢加入乙醇中;反应混合液加热过程中容易发生暴沸,可以加入碎瓷片防止暴沸;
(3)二氧化硫能够与氢氧化钠溶液反应,而乙烯不反应,可以在收集装置之前接一个盛氢氧化钠溶液的洗气瓶,洗去SO2;
(4)乙烯中含有碳碳双键,能被酸性高锰酸钾溶液氧化,根据化合价升降相等配平乙烯与酸性高锰酸钾溶液反应的化学方程式:5CH2=CH2+8KMnO4+12H2SO4=10HCOOH+8MnSO4+4K2SO4+12H2O;0.42 g乙烯的物质的量为:![]() ,参加反应的高锰酸钾的物质的量为:0.015mol×
,参加反应的高锰酸钾的物质的量为:0.015mol×![]() =0.024mol,则转移电子的数目为:0.024mol×(7-2)×NA=0.12NA;
=0.024mol,则转移电子的数目为:0.024mol×(7-2)×NA=0.12NA;
(5)乙烯在农业生产实践中常用作水果的催熟剂或植物生长调节剂。


科目:高中化学 来源: 题型:
【题目】下列说法或表示方法不正确的是
A.盖斯定律实质上是能量守恒定律的体现
B.在加热条件下进行的反应不一定是吸热反应
C.由3O2(g)=2O3(g)H=+284.2kJ/mol,可知O2比O3稳定
D.已知,H2(g)的燃烧热是H=-285.8kJ/mol,则2H2O(l)=2H2(g)+O2(g) H=+285.8kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钡在氧气中燃烧时得到一种钡的氧化物晶体,结构如图所示,有关说法不正确的是( )

A. 该晶体属于离子晶体
B. 晶体的化学式为Ba2O2
C. 该晶体晶胞结构与NaCl相似
D. 与每个Ba2+距离相等且最近的Ba2+共有12个
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知(CH3)2C=CH2,可表示为![]() ,脱落酸(如图)可用作植物生长抑制剂,下列对该物质的叙述正确的是( )
,脱落酸(如图)可用作植物生长抑制剂,下列对该物质的叙述正确的是( )
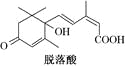
A.其分子式为C15H22O4
B.其属于芳香族化合物
C.1 mol该物质最多可与3 mol H2发生反应
D.该物质在一定条件下可发生自身取代反应生成含七元环的物质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知在1×105 Pa、298 K条件下,2 mol氢气燃烧生成水蒸气放出484 kJ热量,下列热化学方程式正确的是( )
A.2H2(g)+O2(g)===2H2O(g) ΔH=+484 kJ·mol-1
B.H2O(g)===H2(g)+1/2O2(g) ΔH=+242 kJ·mol-1
C.H2(g)+1/2O2(g)===H2O(g) ΔH=+242 kJ·mol-1
D.2H2(g)+O2(g)===2H2O(l) ΔH=-484 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧化亚铜常用于制船底防污漆。用CuO与Cu高温烧结也可制取Cu2O。已知反应:
①2Cu(s) + O2(g) = 2CuO(s) ΔH = 314 kJ/mol
②2Cu2O(s) + O2(g) = 4CuO(s) ΔH = 292 kJ/mol
则反应CuO(s) 与Cu(s) 反应生成Cu2O(s) 的热化学方程式是( )
A.CuO(s) + Cu(s) = Cu2O(s) ΔH = 22 kJ/mol
B.CuO(s) + Cu(s) = Cu2O(s) ΔH = +22 kJ/mol
C.CuO(s) + Cu(s) = Cu2O(s) ΔH = 11 kJ/mol
D.CuO(s) + Cu(s) = Cu2O(s) ΔH = +11 kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种形状像蝴蝶结的有机分子Bowtiediene,其形状和结构如图所示,下列有关该分子的说法中错误的是

A. 生成1 mol C5 H12至少需要4 mol H2
B. 该分子中所有碳原子在同一平面内
C. 三氯代物只有一种
D. 与其互为同分异构体,且只含碳碳三键的链烃有两种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各表述与示意图一致的是
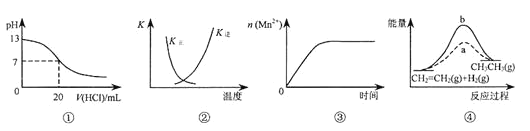
A. 图①表示25℃时,用0.1 mol·L-1盐酸滴定20 mL 0.1 mol·L-1NaOH溶液,溶液的pH随加入酸体积的变化
B. 图②中曲线表示反应2SO2(g) + O2(g)![]() 2SO3(g);ΔH < 0 正、逆反应的平衡常数K随温度的变化
2SO3(g);ΔH < 0 正、逆反应的平衡常数K随温度的变化
C. 图③表示10 mL 0.01 mol·L-1KMnO4酸性溶液与过量的0.1 mol·L-1H2C2O4溶液混合时,n(Mn2+) 随时间的变化
D. 图④中a、b曲线分别表示反应CH2=CH2(g) + H2(g)![]() CH3CH3(g);ΔH< 0使用和未使用催化剂时,反应过程中的能量变化
CH3CH3(g);ΔH< 0使用和未使用催化剂时,反应过程中的能量变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)有①甲烷、②乙烷、③丙烷、④丁烷4种烷烃,试回答下列各题(填序号):
a.上述气态烃中,其一氯取代物的同分异构体只有两种的是___。
b.等物质的量上述气态烃充分燃烧,消耗O2的量最多的是___。
c.等质量的上述气态烃,在充分燃烧时,消耗O2的量最多的是__。
(2)有4种无色液态物质: a.1-庚烯[CH3(CH2)4CH=CH2]、b.戊烷[ CH3(CH2)3CH3]、c.苯(![]() )、d.甲苯(
)、d.甲苯(![]() ),
),
请回答下列问题:
①能与溴水和酸性KMnO4溶液反应的是__(写编号),
②不能与溴水反应但能与酸性KMnO4溶液反应的是___(写编号)。
③不能与溴水和酸性KMnO4溶液反应,但在铁屑作用下能与液溴反应的是___(写编号),反应的化学方程式为___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com