
| A、2 I--2e-=I2 碘遇淀粉变蓝 |
| B、Cu-2e-=Cu2+ Cu2+ 显蓝色 |
| C、2Cu+4I--4e-=2CuI↓+I2 碘遇淀粉变蓝 |
| D、4OH--4e-=2H2O+O2 O2将I-氧化为I2,碘遇淀粉变蓝 |


科目:高中化学 来源: 题型:
| A、此条件下,可认为NO分解产生O2的反应完全 |
| B、此条件下,2H2O(g)=2H2 (g)+O2(g),此时平衡常数的数值约为5×10-10 |
| C、此条件下,NO、H2O、CO2三种物质分解放出O2的倾向由大到小的顺序为H2O>NO>CO2 |
| D、以上说法都不正确 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 500℃ |
| 催化剂 |
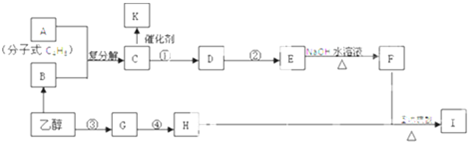
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、将铜粉与硫粉混合均匀加热以制取CuS |
| B、向Cu与过量浓硫酸反应后的试管中加水以观察CuSO4溶液的颜色 |
| C、向CuSO4溶液中加入过量的NaOH,过滤洗涤并收集沉淀充分灼烧以制取CuO |
| D、在淀粉溶液中加入适量稀H2SO4微热,再加少量新制Cu(OH)2悬溶液并加热,产生红色沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN | Na2SO4 |
| pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 | 7.0 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、该弱酸溶液的pH=4 |
| B、加入NaOH溶液后,弱酸的电离平衡向右移动,但Ka不变 |
| C、加入等体积的0.01mol?L-1NaOH溶液后,所得的溶液的pH<7 |
| D、该弱酸的钠盐溶液一定会发生水解,常温下,其水解平衡常数Kh=10-8 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 实验目的 | 操作或现象 |
| A | 制备Fe(OH)3胶体 | 向25mL沸水中逐滴滴加饱和FeCl3溶液5~6滴,并加热至溶液呈红褐色时停止加热 |
| B | 证明蛋白质在某些无机盐溶液作用下发生变性 | 向鸡蛋清溶液中加入饱和硫酸钠溶液,有沉淀析出;再把沉淀加入蒸馏水中 |
| C | 测定氯水的pH | 用玻璃棒蘸 取氯水滴在pH试纸上,观察 |
| D | 证明溶液中存在平衡: Fe3++3SCN-?Fe(SCN)3 | 将1 mL KSCN溶液与1 mL 同浓度 FeCl3溶液充分混合;再滴加KSCN溶液,溶液颜色加深 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com