
 常温下,Ksp(CaSO4)=9×l0-6,常温下CaSO4在水中的沉淀溶解平衡曲线如图.下列判断错误的是( )
常温下,Ksp(CaSO4)=9×l0-6,常温下CaSO4在水中的沉淀溶解平衡曲线如图.下列判断错误的是( )| A、a、c两点均可以表示常温下CaS04溶于水所形成的饱和溶液 |
| B、a点对应的Ksp不等于c点对应的Ksp |
| C、b点将有沉淀生成 |
| D、向d点溶液中加入适量CaCl2固体可以变到c点 |


科目:高中化学 来源: 题型:
| A、加入过量CaO(s) |
| B、加入少量NaOH(s) |
| C、通入过量HCl(g) |
| D、加入少量H2O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、铝溶于NaOH溶液:Al+2OH-=AlO2-+H2↑ |
| B、过量CO2通入NaOH溶液中:CO2+2OH-=CO32-+H2O |
| C、钠与水反应:2Na+2H2O=2Na++2OHˉ+H2↑ |
| D、稀硫酸中滴加氢氧化钡溶液:H++OH-=H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 容器编号 | 各物质物质量/ | 达到平衡时体系能量变化 | ||
| A | B | C | ||
| ① | 1 | 3 | 0 | 放热46.3kJ |
| ② | 0.3 | 0.9 | 1.4 | |
| A、达平衡时,两个容器中C的物质的量浓度均为1.0mol?L-1 |
| B、容器①达平衡A转化率是50% |
| C、容器②中达平衡时吸收的热量为18.52kJ |
| D、若起始容器中A、B、C各为0.5mol,则达平衡前υ(正)<υ(逆) |
查看答案和解析>>
科目:高中化学 来源: 题型:

| n(SO3) |
| n(SO2) |
| t1-t2 | t3-t4 | t5-t6 | t6-t7 |
| K1 | K2 | K3 | K4 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
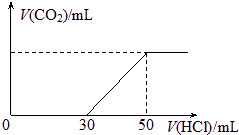 标况下,在100 mL 0.1mol?L-1某NaOH溶液中通入一定量CO2后,再向所得溶液中滴加某浓度的稀盐酸,滴加盐酸的体积与生成气体的情况如图所示.(假设生成的CO2全部逸出).求:
标况下,在100 mL 0.1mol?L-1某NaOH溶液中通入一定量CO2后,再向所得溶液中滴加某浓度的稀盐酸,滴加盐酸的体积与生成气体的情况如图所示.(假设生成的CO2全部逸出).求:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com