
【题目】下列叙述正确的是
A.常温下,浓硝酸和浓硫酸都不与铁、铝反应
B.氨易液化,液氨常用作制冷剂
C.活泼金属和稀硝酸反应时置换出氢气
D.与金属反应时,稀硝酸可能被还原为更低价态,稀硝酸氧化性强于浓硝酸
科目:高中化学 来源: 题型:
【题目】偏二甲肼(C2H8N2)与N2O4反应放出的能量能把火箭送入太空。该化学方程式为C2H8N2 + 2N2O4=2X↑+ 3N2↑+ 4H2O↑。下列说法正确的是( )
A. X的化学式为CO B. 偏二甲肼中碳的质量分数为40%
C. 该反应属于分解反应 D. 生成N2和H2O的质量比为14:9
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A. 甲烷分子的比例模型为![]() ,其二氯取代物有1种结构
,其二氯取代物有1种结构
B. 苯和乙烯都能使溴水褪色,其褪色原理相同
C. 相同质量的乙炔与苯分别在足量的氧气中完全燃烧,消耗氧气的物质的量相同
D. 在一定条件下,苯与氯气生成氯苯的反应类型是取代反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】煤干馏后可得到焦炭、煤焦油、粗氨水和焦炉气等。焦炭可通过以下途径制取聚氯乙烯等化工产品。

完成下列填空:
(1)上述乙炔转化为HC≡C-CH=CH2的反应类型是___________________。
(2)HC≡C-CH=CH2与正四面体烷![]() 的关系是______________________。
的关系是______________________。
(3)若分别完全燃烧等质量的HC≡C-CH=CH2和乙炔,所需氧气的量____________________ (选填“前者多”“后者多”“一样多”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设阿伏加德罗常数的值为NA,下列有关叙述正确的是( )
A. 室温下,1LpH=13的Ba(OH)2溶液中含有OH-的数目为0.2NA
B. 密闭容器中0.2molNO和0.1molO2充分反应后,分子总数为0.2NA
C. 7.8gNa2S和7.8gNa2O2中含有阴、阳离子总数均为0.3NA
D. 0.02molNa与0.1mol/L的盐酸充分反应,转移的电子数为0.01NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】物质结构与性质]单质铁、锂、砷及它们的化合物广泛应用于超导体材料等领域,回答下列问题:
(1)Fe原子的核外电子排布式为[Ar]_________,Li原子核外占据最高能层电子的电子云轮廓图形状为_________。
(2)As 的卤化物的熔点如下:
AsCl3 | AsBr3 | AsI3 | |
熔点/K | 256.8 | 304 | 413 |
表中卤化物熔点差异的原因是_________,AsCl3分子的立体构型为_________。
(3)铁、锂、砷形成的化合物LiFeAs是一种超导体,其晶胞结构如图1所示,已知立方晶胞参数acm,则该晶休的密度是_________g/cm3(用含a、NA的式子表示)。


(4)向FeCl3溶液中滴入EDTA试剂可得配合物A,其结构如图2所示,图中M代表Fe3+。则1号碳原子有_______个σ键,2号碳原子采取_________杂化方式;Fe3+与氮原子之间形成的化学键是_________,Fe3+的配位数为_________;该配合物中,第二周期的三种元素的第一电离能由大到小的顺序为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分枝酸可用于生化研究。其结构简式如图。下列关于分枝酸的叙述正确的是
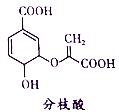
A. 分子中含有2种官能团
B. 可与乙醇、乙酸反应,且反应类型相同
C. 1mol分枝酸最多可与3molNaOH发生中和反应
D. 可使溴的四氯化碳溶液、酸性高锰酸钾溶液褪色,且原理相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com