


 ��У��������ĩ��̾�ϵ�д�
��У��������ĩ��̾�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ��ʴ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 Li2FeSiO4��Li2SO4��SiO2��
Li2FeSiO4��Li2SO4��SiO2�� ����
���� ������
������ Li2FeSiO4��
Li2FeSiO4�� Li2FeSiO4����õ�صĸ�����________�����ʱ��������Ӧ�ĵ缫��ӦʽΪ________��
Li2FeSiO4����õ�صĸ�����________�����ʱ��������Ӧ�ĵ缫��ӦʽΪ________���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��Pb������PbO2���� |
| B�������缫��ӦʽΪPbO2 + SO4 2- + 2H+ =PbSO4 + H2O |
| C��������Һ�У�H+���� |
| D���ŵ�һ��ʱ���SO4 2-Ũ�ȼ�С |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��Li�Ǹ������缫��ӦΪLi��e-��Li+ | B��Li���������缫��ӦΪLi��e-��Li- |
| C��MnO2�Ǹ������缫��ӦΪMnO2��e-��MnO2- | D��﮵�ع������̣���ѧ��ת��Ϊ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
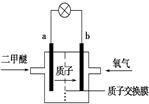
| A��a��Ϊ��صĸ��� |
| B����ع���ʱ������b���ص��߾����ݵ�a�� |
| C����������ĵ缫��ӦʽΪ4H����O2��4e��===2H2O |
| D����ع���ʱ��1 mol�����ѱ�����ʱ��6 mol���ӷ���ת�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
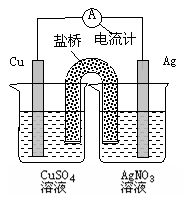
| A�����缫�Ǹ��� |
| B��ͭ�缫�Ϸ����ķ�ӦΪCu-2e-=Cu2�� |
| C�����·�еĵ����Ǵ����缫����ͭ�缫�� |
| D����װ���ܽ�����ת��Ϊ��ѧ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
| �� | ���볣��(Ka) | �� | ���볣��(Ka) |
| CH3COOH | 1.8��10-5 | HCN | 5��10-10 |
| H2CO3 | Ka1 = 4.2��10-7 | HClO | 3��10-8 |
| Ka2 = 5.6��10-11 |
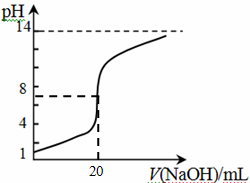
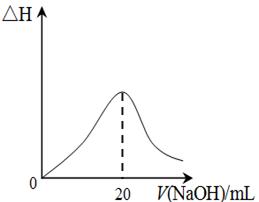
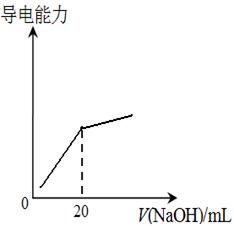
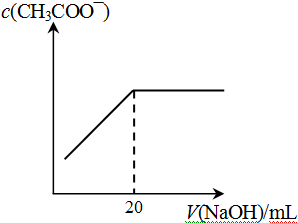
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com